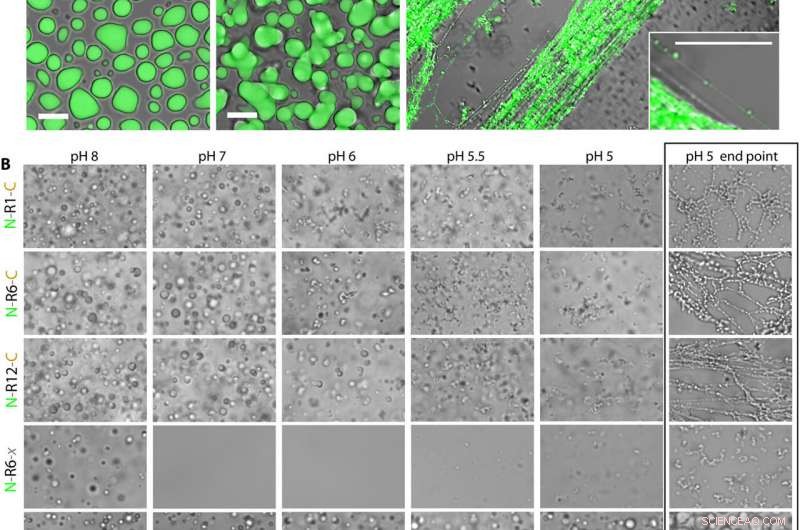
Försurning utlöser snabb självmontering av MaSp2 nanofibriller. (A) N-R12-C märkt med DyLight 488 (10 till 20 mg ml-1 slutkoncentration) blandades i 0,5 M KPi vid de angivna pH-värdena och visualiserades med konfokal laserskanningsmikroskopi. Vid blandning av komponenterna, MaSp2 separerade snabbt från den vattenhaltiga fraktionen (gröna strukturer), lägger sig så småningom på glasytan. Vid pH 7 och 8, MaSp2-kondensatet visas som LLPS-droppar som genomgår dynamisk fusion, vid pH 6, de resulterande strukturerna är statiska med ett halvfast utseende. Reaktionen vid pH 5 leder till snabb självmontering av MaSp2 till ofta inriktade, utökade fibrillnätverk. Insättningen visar en individuell fibrill vid pH 5 med en diameter på ~100 nm. Skala staplar, 10 μm. (B) Olika MaSp2-konstruktioner utvärderades för deras förmåga att genomgå fosfatinducerad LLPS och pH-inducerad fibrillsjälvmontering. Renad MaSp2 (150 μM slutkoncentration) blandades till en droppe av 0,5 M KPi vid de angivna pH-värdena på en glasskiva. Alla bilder i den oboxade regionen (vänster) togs inom 30 s efter blandning. Det inrutade området till höger visar slutpunkten för pH 5-reaktionerna, tas 30 minuter efter initiering. Alla bilder togs i samma skala; skala bar, 10 μm. Kreditera: Vetenskapens framsteg (2020). DOI:10.1126/sciadv.abb6030
Ett team av forskare från RIKEN Center for Sustainable Resource Science, Keio University och Kyoto University, har funnit att vätske-vätskefasseparation (LLPS) driver processen att omvandla spidroinproteiner till spindelnätsfibrer. I deras papper publicerad i tidskriften Vetenskapens framsteg , gruppen beskriver hur man replikerar processen att omvandla ett internt protein till spindelnätsfibrer i deras labb och hur de gjorde det möjligt för dem att skapa silkessträngar.
Forskare har studerat spindlar och näten de skapar i många år, med målet att replikera processen och därigenom industrialisera produktionen av siden. Tyvärr, trots mycket ansträngning, forskare vet fortfarande inte hur spindlar gör det. De vet att spindlar skapar spidroinproteiner, som de förvarar i en påse tills de är redo att göra en väv. Sedan, när de stöter ut de flytande proteinerna, materialet formas på något sätt automatiskt till fibrer för att skapa trådar. I denna nya ansträngning, forskarna har hittat ett sätt att replikera en del av denna process.
Arbetet involverade ingenjörsbakterier för att producera den typ av spidroinproteiner som normalt produceras av Joro-spindeln. När man studerar proteinet, de upptäckte att det blev grumligt när det utsätts för varma temperaturer. En närmare titt visade att proteinet koalescerade och smälte samman, ett troligt första steg mot fiberbildningsprocessen. De fann också att processen involverade LLPS.
Teamet försökte sedan exponera proteinet för olika material tills de träffade fosfat - och tillade att det också gjorde proteinet grumligt. Teamet började sedan trimma proteinblandningen genom att ändra pH-nivåerna tills blandningen började skapa fibrer. De fann sedan att för att göra en tråd, allt de behövde göra var att sträcka det fiberbelastade materialet. På så sätt kunde de skapa en sträng som var 10 centimeter lång. Att studera strängen under ett mikroskop visade att den hade samma struktur som strängar som produceras naturligt av spindlarna.
Forskarna noterar att deras arbete bara är ett trevande steg mot att helt förstå processen genom vilken spindlar skapar silke. De planerar att driva vidare med sin forskning med det slutliga målet att utveckla ett sätt att producera silke i ett labb, eller en fabrik.
© 2020 Science X Network