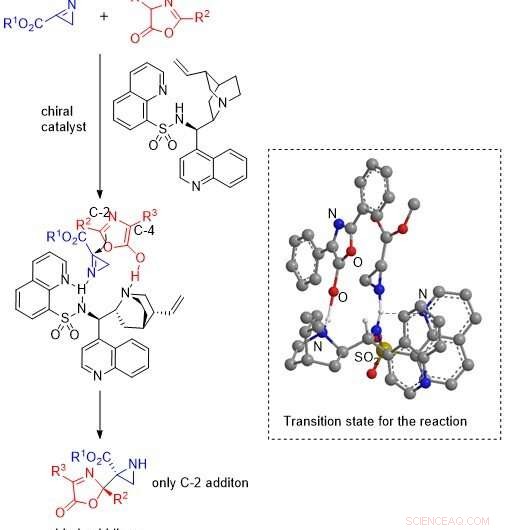
Produktion av aziridiner med högt utbyte och hög renhet med hjälp av ny katalysator. Forskare från Japan föreslog nyligen ett möjligt övergångstillstånd för reaktionen mellan aziridiner och oxazoloner i närvaro av en cinchona alkaloid sulfonamidkatalysator, framställning av önskvärda aziridin-oxazolonföreningar med höga utbyten och enantioselektivitet eller renhet. Upphovsman:Shuichi Nakamura från NITech
Om du inte har studerat kemi på college, det är osannolikt att du har stött på namnet aziridin. En organisk förening med molekylformeln, C 2 H 4 NH, aziridiner är välkända bland medicinska kemister, som använder föreningen för att framställa farmaceutiska läkemedel såsom Mitomycin C, ett kemoterapeutiskt medel som är känt för sin antitumöraktivitet. Specifikt, aziridiner är vad kemister kallar enantiomerer - molekyler som är spegelbilder av varandra och inte kan läggas över varandra. En särart med enantiomerer är att den biologiska aktiviteten hos en skiljer sig från dess spegelbild och endast en av dem är önskvärd för tillverkning av läkemedel. Apotek, därför, väljer regelbundet asymmetriska eller enantioselektiva syntestekniker som ger den önskade enantiomeren i större mängder.
En sådan teknik som nyligen har uppmärksammats ur farmaceutisk syntes innebär användning av oxazoloner - kemiska föreningar med molekylformeln C 3 H 3 NEJ 2 - att framställa aziridiner. "Oxazoloner är kända för sin mångsidighet i att ge biologiskt aktiva föreningar, "förklarar professor Shuichi Nakamura från Nagoya Institute of Technology (NITech), Japan, som studerar asymmetriska reaktioner, "Dock, de enantioselektiva reaktionerna av 2H-aziriner med oxazoloner har inte varit särskilt givande, Trots att han framhålls som en av de mest effektiva metoderna för att syntetisera aziridiner. "
I en ny studie som nyligen publicerades i Organiska bokstäver , Prof. Nakamura tillsammans med sina kollegor från NITech och Osaka University, Japan, utforskade denna fråga och i ett betydande genombrott, lyckades erhålla aziridin-oxazolonföreningar i höga utbyten (99%) samt hög enantioselektivitet eller renhet (98%). Dessutom, laget använde en original katalysator som de utvecklade för att katalysera reaktionerna de studerade.
Teamet började med att värma a-azideakrylater vid 150 ° C i ett organiskt lösningsmedel tetrahydrofuran (THF) för att framställa 2H-aziriner och reagerade sedan med oxazoloner i närvaro av olika organokatalysatorer för att producera olika aziridin-oxazolonföreningar. Särskilt, teamet undersökte effekten av katalysatorn cinchonin och olika heteroarenkarbonyl- och heteroarenesulfonylgrupper i organokatalysatorer härledda från cinchona-alkaloider och fann att reaktioner med hjälp av katalysatorer med antingen en 2-pyridinesulfonylgrupp eller en 8-kinolinesulfonylgrupp gav både ett högt utbyte (81-99% ) samt hög enantiopurity (93-98%). Dessutom, forskare observerade att reaktionen mellan en 2H-azirin innehållande en etylestergrupp och en oxazolon med en 3, 5-dimetoxifenylgrupp i närvaro av katalysatorn med 8-kinolinsulfonylgrupp gav också höga utbyten (98-99%) samt enantiopurity (97-98%).
Teamet fortsatte sedan med att utforska reaktionen mellan 2H-azirin med etylestergrupp och en större mängd oxazoloner i närvaro av katalysatorn med 8-kinolinsulfonylgrupp. I alla reaktionerna observerade de höga utbyten (77-99%) och enantiopurities (94-99%) utom en för en oxazolon som bär en bensylgrupp och katalysatorn med 2-pyridylsulfonylgrupp som endast gav ett måttligt utbyte ( 61%) och renhet (86%). Dessutom, de kunde omvandla de erhållna aziridinerna till olika andra enantiomerer utan förlust av renhet.
Till sist, laget föreslog en katalytisk mekanism och ett övergångstillstånd för reaktionen av 2H-aziriner med oxazoloner där katalysatorn aktiverar både oxazolon och 2H-azirin, som sedan reagerar för att ge en tilläggsprodukt som, i tur och ordning, ger aziridinet med regenerering av katalysatorn.
Även om den detaljerade mekanismen ännu inte har klargjorts, forskare är glada över sina resultat och ser fram emot metodens tillämpning inom medicin och farmakologi. "Det har potential att förse människor med nya läkemedel och skapa nya läkemedel samt läkemedelskandidater som för närvarande är svåra att syntetisera. Dessutom har katalysatorn som används i denna studie kan användas för många andra stereoselektiva syntetiska reaktioner, "konstaterar en optimistisk professor Nakamura.
Några fascinerande konsekvenser att tänka på!