Upphovsman:Wiley
Både kväveoxid (NO) och vätesulfid (H 2 S) fungerar som gasformiga signalmolekyler med liknande fysiologiska effekter. Många av de kritiska frågorna om samspelet mellan dessa två gastransmitter beror på deras kemiska reaktivitet och den flyktiga existensen av HSNO, en nyckelprodukt av reaktionen mellan dem. Ett team av forskare har kunnat stabilisera, isolera, och karakterisera två av de arter som är bundna till dessa signalvägar genom bindning till ett zinkkomplex, enligt tidningen, Angewandte Chemie .
NO är en central signalmolekyl i biologin som reglerar många fysiologiska funktioner som inkluderar kärlvidgning, överföring av nervimpulser, och cellskydd. Intressant, H 2 S uppvisar liknande effekter, avslappnande glatta muskelceller involverade i vasodilatation. HSNO kan således spela en nyckelroll i överlappningen av dessa signalvägar. Denna extremt reaktiva art är så instabil, dock, att dess biokemi och diskreta reaktionsvägar är mycket svåra att bestämma. HSNO passerar lätt genom cellmembran och kan nitrosylera proteiner, överföra sin nitrosylgrupp (–N =O) till andra rester, särskilt cystein, vilket representerar ett viktigt steg i ett antal cellulära regleringsmekanismer. Vid biologiskt pH, HSNO existerar troligen som tionitritanjon SNO - som är instabil mot konvertering till perthionitrit -anjonen SSNO - .
Doktorand Valiallah Hosseininasab i teamet som leds av Timothy H. Warren vid Georgetown University (Washington, D.C., USA) stabiliserade SNO - och SSNO - anjoner genom bindning till ett speciellt zinkkomplex inspirerat av en gemensam miljö för zink i biologin. Zink är en fysiologiskt viktig metall som är involverad i otaliga processer som inkluderar reglering av blodets pH genom enzymet kolsyraanhydras. Dessutom, molekyler involverade i kväveoxidsignalering, som H. 2 S- och S-nitrosotioler (molekyler med en –S – N =O-grupp), reagerar lätt med zink -svavelbindningar som bildar viktiga strukturella enheter vars modifiering i proteiner leder till funktionell förändring.
Georgetown -teamet avslöjade att zinkkomplex som innehåller SNO
-
och SSNO
-
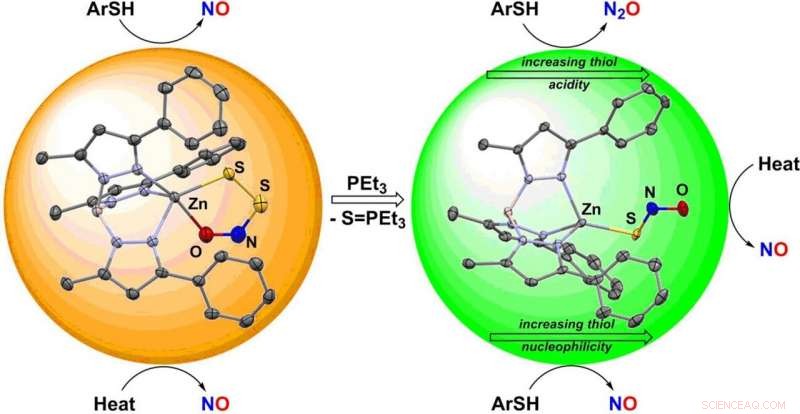
anjoner kan isoleras och karakteriseras. Undersökning av deras reaktivitetsmönster visade intressanta skillnader i deras reaktioner med tioler (ämnen med en sulfidgrupp,
-
SH), allestädes närvarande antioxidanter som hjälper till att skydda celler från skador. Medan reaktioner med perthionitrit bildar NO, tionitrit bildar antingen dinitrogenoxid (skrattgas) N 2 O- eller S-nitrosotioler, som representerar färdiga reservoarer av NO. Dessa resultat tyder på att de minsta skillnaderna i fysiologiska signalvägar kan leda till olika utsignaler som slutligen kommer från samspelet mellan NO och H 2 S.