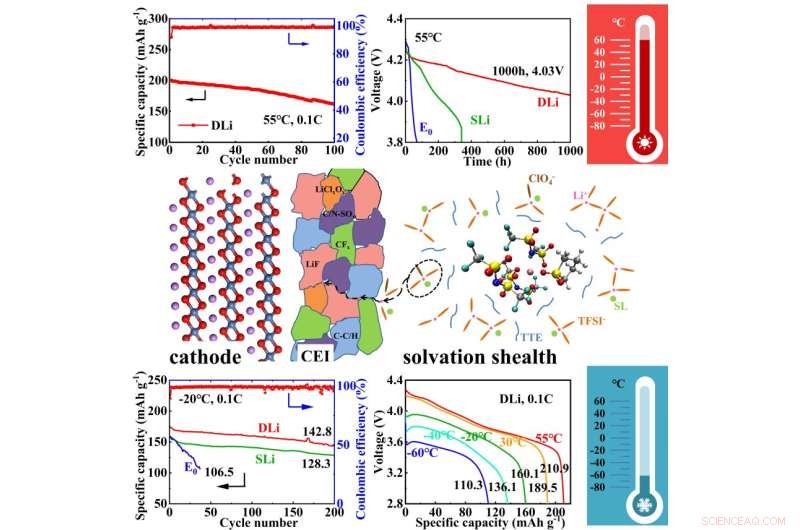
Diagrammen i denna bild visar katodens sammansättning, hur katoden och elektrolyten interagerar (CEI) och solvatiseringsmanteln, vilket är hur de olika kemiska molekylerna i lösningsmedlet interagerar med varandra. Graferna visar hur elektrolyten reagerade vid höga och låga temperaturer, inklusive en graf för att visa kapacitet över tid och kapacitet vid olika spänningar. Kredit:Nano Research
Eftersom vårt behov av högdensitetsbatterier ökar med en utbredd användning av elbilar och alternativa energikällor, är det en nödvändighet att förbättra stabiliteten och kapaciteten hos litiumjonbatterier. Nuvarande litiumjonbatteriteknik, som ofta använder nickel, är mindre stabil vid extrema temperaturer, vilket leder till överhettning på grund av både temperatur och höga spänningar. Dessa batterier tenderar också att försämras snabbt.
För att lösa detta problem studerar forskare nya kemiska kombinationer som kan åtgärda dessa nackdelar. I en nyligen genomförd studie visade forskare hur ett lösningsmedel och en oorganisk föreningstillsats kan förbättra stabiliteten och prestandan hos litiumjonbatterier med nickelkatoder.
De publicerade sina resultat den 12 september i Nano Research .
Grunderna i hur batterier fungerar är desamma, oavsett om du funderar på ett industriellt litiumjonbatteri eller ett genomsnittligt AA-batteri för hushåll. Katoden är den positiva elektroden, anoden är den negativa elektroden, och mellan dem inuti batteriet finns en lösning som kallas elektrolyten. Positivt och negativt laddade joner strömmar genom elektrolyten och en kemisk reaktion genererar elektrisk energi. I denna studie identifierade forskare en sulfolanbaserad flytande elektrolyt med litiumperklorat tillsatt som en potentiell lösning på vanliga nackdelar med litiumjonbatterier.
"För nickelbaserade katoder uppnås vanligtvis god elektrokemisk prestanda vid låg temperatur på bekostnad av egendom och säkerhet vid rumstemperatur. Detta beror på att elektrolyter med lågsmältande lösningsmedel försämras dramatiskt. Den höga flyktigheten och brandfarligheten hos dessa elektrolyter begränsar också deras användning vid höga temperaturer", säger professor Fang Lian vid School of Materials Science and Engineering vid University of Science and Technology Beijing i Peking, Kina. Genom att tillsätta litiumperklorat till sulfolanet fann forskare att de kunde förbättra många av dessa nackdelar.
Sulfolan är ett lösningsmedel som ursprungligen skapades för användning i olje- och gasindustrin, men det används nu i många olika industriella miljöer eftersom det håller sig stabilt vid förhöjda temperaturer. Litiumperklorat är en oorganisk förening som kombineras med sulfolanet för att bibehålla elektrolytens stabilitet. En tredje kemikalie tillsätts för att späda ut elektrolyten och hjälpa elektrolytens stabilitet vid ett brett temperaturområde.
För att testa hur väl den föreslagna elektrolyten fungerade skapade forskarna ett batteri med hjälp av elektrolyten och utförde en serie tester och teoretiska beräkningar.
De fann att lösningsmedlet kunde upprätthålla ledningsförmåga vid ett brett temperaturområde, varierande från –60 till 55 grader Celsius. I jämförelse tenderar traditionella elektrolyter att stelna vid temperaturer under -20 grader Celsius. Att tillsätta litiumperklorat till elektrolyten stärker hur de olika kemikalierna i elektrolyten interagerar med varandra och minskar mängden energi som krävs, vilket gör det lättare för elektrolyten att arbeta vid lägre temperaturer.
"Den utspädda högkoncentrerade sulfolanbaserade elektrolyten med litiumperklorattillsats förverkligar användningen av breda temperaturer i högspänningsceller. Denna kombination förbättrar litiumjonöverföringen och minskar desolvationsenergin, samtidigt som den hämmar den kontinuerliga nedbrytningen av elektrolyten och den akuta försämringen av katoden vid höga temperaturer," sa Lian. "Vårt arbete ger en omfattande förståelse för elektrolytens molekylära design, vilket underlättar utvecklingen av litiumbatterier med hög energidensitet." + Utforska vidare