
Rice University doktorand Kang-Jie (Harry) Bian sätter upp ljuskänsliga molekyler för ett experiment i kemisten Julian Wests labb. Bian är huvudförfattare till en studie inspirerad av naturliga processer för att möjliggöra modulär difunktionalisering av alkenmolekyler för läkemedels- och materialdesign. Kredit:Rice University
Inspirerad av din lever och aktiverad av ljus visar en kemisk process som utvecklats i labb vid Rice University och i Kina lovande för läkemedelsdesign och utveckling av unika material.
Forskare under ledning av riskemisten Julian West och Xi-Sheng Wang vid University of Science and Technology of China, Hefei, rapporterar sin framgångsrika katalytiska process för att samtidigt lägga till två distinkta funktionella grupper till enstaka alkener, organiska molekyler framtagna från petrokemikalier som innehåller minst en kol-kol dubbelbindning kombinerad med väteatomer.
Ännu bättre, säger de, är att dessa alkener är "oaktiverade" – det vill säga de saknar reaktiva atomer nära dubbelbindningen – och fram till nu har de visat sig vara svåra att förbättra.
Den kemiska vägen som beskrivs i Journal of the American Chemical Society skulle kunna förenkla skapandet av ett bibliotek av prekursorer för läkemedelsindustrin och förbättra tillverkningen av polymerer.
West, vars labb designar syntetiska kemiska processer, sa att den första inspirationen kom från ett enzym, cytokrom P450, som levern använder för att eliminera potentiellt skadliga molekyler.
"Dessa enzymer är typ av buzzsaws som maler upp molekyler innan de kan få dig i problem," sa han. "De gör detta genom en intressant mekanism som kallas radikal rebound."
West sa att P450 hittar kol-vätebindningar och tar bort vätet, vilket lämnar en kolcentrerad radikal som inkluderar en oparad elektron.
"Den elektronen vill verkligen hitta en partner, så P450 kommer omedelbart att ge tillbaka en syreatom ("rebound"), vilket oxiderar molekylen," sa han. "I kroppen hjälper det till att deaktivera dessa molekyler så att du kan bli av med dem.
"Den här typen av rebound är kraftfull," sa West. "Och Harry (huvudförfattaren Kang-Jie Bian, en Rice-student) undrade om vi kunde göra något liknande för att överföra olika fragment till den radikalen."
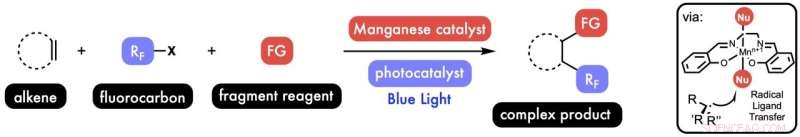
Rice University kemister utvecklade en metod för att lägga till två fragment till en alkenmolekyl i en enda process. Upptäckten kan förenkla läkemedels- och materialdesign. Kredit:West Research Group/Rice University
Deras lösning var att möjliggöra vad de kallar radikal ligandöverföring, en allmän metod som använder mangan för att katalysera den "radikala återhämtningen".
West sa att medan P450 använder det närliggande elementet, järn, för att katalysera den biologiska reaktionen, visade tidigare experiment på rislabbet och på andra ställen att mangan hade potential.
"Mangan hjälpte processen att bli mer selektiv och lite mer aktiv, samt mycket billigare och enklare," förklarade han. "Den kan överföra en massa olika atomer - som klor, kväve och svavel - bara genom att ändra vilken kommersiell ingrediens du lägger till i reaktionen."
Den reaktionen stod för en funktionalisering. Varför inte gå för två?
West sa att Bian också kom på idén att lägga till en fotokatalysator till blandningen. "När du lyser ljus på den blir den upphetsad och du kan göra saker som skulle vara omöjliga i grundtillståndet, som att aktivera små fluorkolmolekyler för att göra radikala fragment som har kol-fluorbindningar, vilket är viktigt för läkemedels- och materialvetenskap, " han sa. "Nu kan vi koppla dessa till vår molekyl av intresse."
Slutresultatet är en mild och modulär process för att lägga till två funktionella grupper till en enda alken i ett steg.
"Först har vi kol-kol dubbelbindningen av en molekyl av intresse, alkenen," sa West och summerade. "Sedan lägger vi till detta värdefulla fluorkol, och sedan simmar mangankatalysatorn upp och överför denna radikala ligand för att tillsätta en klor- eller kväve- eller svavelatom."
Han noterade att samarbetet mellan Rice och Wangs labb var ett naturligt resultat av Bians flytt till Rice från Hefei, där han tog sin magisterexamen. "Vi fokuserade verkligen på manganaspekten av detta arbete, och Wangs grupp tog inte bara med sig expertis inom fotokatalys utan också utvecklade och testade kol-fluor-fragment, och visade att de skulle fungera riktigt bra i det här systemet," sa West.
Han sa att tillsammans med läkemedels- och materialvetenskap kan kemisk biologi också dra nytta av processen, särskilt för dess affinitet till pClick, en metod som upptäckts av riskemisten Han Xiao för att fästa läkemedel eller andra ämnen till antikroppar.
Medförfattare är Rice undergraduate David Nemoto Jr. och doktorand Shih-Chieh Kao, och Yan He och Yan Li från Hefei. Wang är professor vid Hefei. West är Norman Hackerman-Welch Young Investigator och biträdande professor i kemi. + Utforska vidare