Forskare vid Rice University har framgångsrikt syntetiserat en grupp naturliga föreningar som kallas fusicoccaner. Molekylerna som finns i olika levande organismer uppvisar olika biologiska aktiviteter, inklusive förmågan att modulera protein-proteininteraktioner inom biologiska system.
Studien ledd av Hans Renata, docent i kemi, markerar ett betydande framsteg inom kemisk syntesteknik, som utnyttjar modern organisk kemi och konstruerade enzymer. Forskningen är publicerad i tidskriften Nature Chemistry .
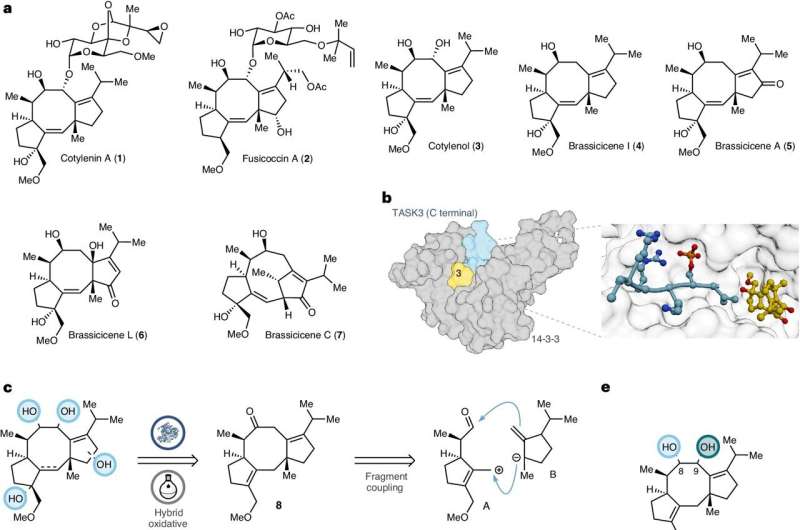
Teamet syntetiserade 10 distinkta fusicoccaner genom en ny strategi som kombinerar syntesen av föreningarnas kärnstrukturer genom organisk kemi med den exakta dekorationen av funktionella grupper med hjälp av enzymer.
"Vårt tillvägagångssätt representerar en fusion av traditionella syntetiska metoder med banbrytande enzymatisk katalys," sa Renata. "Genom att utnyttja kraften hos konstruerade enzymer har vi uppnått syntesen av dessa komplexa molekyler och även banat väg för ytterligare kemiska modifieringar."
Forskarna stötte på utmaningar under den enzymatiska fasen av syntesen eftersom de valda enzymerna initialt var instabila och ledde till oönskade biprodukter. Men genom rigorösa experiment och enzymteknik identifierade de förbättrade enzymvarianter som var skräddarsydda för syntesprocessen.
"Detta arbete visar vikten av enzymteknik för att möjliggöra syntesen av biologiskt relevanta föreningar," sa Renata. "Våra resultat belyser potentialen hos en hybridsyntetisk strategi för utveckling av nya molekyler med olika tillämpningar."
Förutom deras direkta tillämpning som modulatorer av protein-proteininteraktioner, öppnar de syntetiserade föreningarna vägar för att utforska nya läkemedelskandidater och förstå biologiska processer, sa huvudförfattaren och postdoktorn Yanlong Jiang.
"Vår metodik kan inspirera till liknande innovationer i syntesen av andra värdefulla molekyler, vilket driver framsteg inom olika områden," sa Jiang.
Mer information: Yanlong Jiang et al, Modulär kemoenzymatisk syntes av tio fusicoccan-diterpenoider, Nature Chemistry (2024). DOI:10.1038/s41557-024-01533-w
Journalinformation: Naturkemi
Tillhandahålls av Rice University