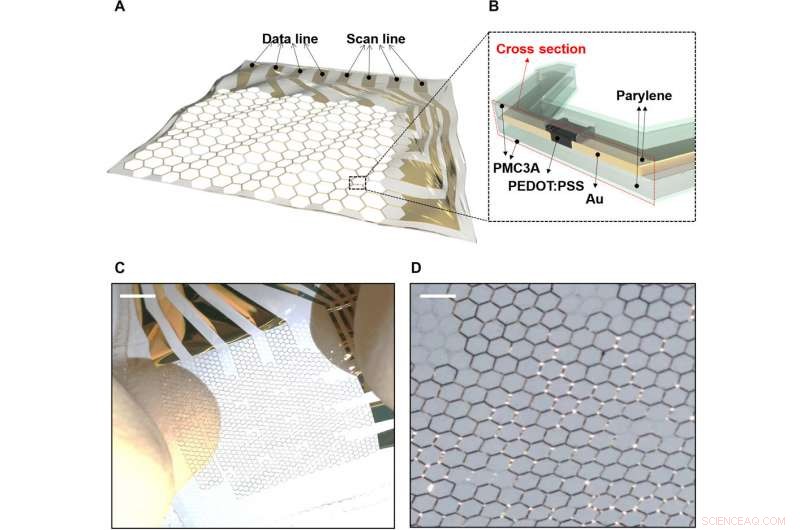
Sträckbar OECT-array på bikakestruktur. A) Den töjbara elektrofysiologiska OECT-arrayen på ett parylensubstrat med bikakenät. B) Tvärsnitt av den töjbara OECT-matrisen. C) En 4 x 4 töjbar OECT-matris när den är utsträckt. D) Förstorad bild av 4 x 4 töjbar OECT-array när den är sträckt. Upphovsman:Science Advances, doi:10.1126/sciadv.aau2426
För att utvärdera in vivo fysiologiska funktioner, elektrofysiologiska signaler måste övervakas med hög precision och hög rumslig eller tidsmässig upplösning. Ultraflexibel, multielectrode arrays (MEA) tillverkades nyligen för att etablera konform kontakt på organens ytor och för att mäta elektrofysiologisk signalutbredning vid hög rums-temporal upplösning. Dock, plastsubstrat med en hög Youngs modul inkorporerad i processen orsakade svårigheter under implantation på grund av dynamisk rörelsebaserad hemodynamik vid hjärtats yta. I en ny studie publicerad i Vetenskapens framsteg , Wonryung Lee och kollegor har utvecklat en aktiv MEA tillverkad för att visa icke-trombogenicitet, töjbarhet och stabilitet. Arrayerna möjliggjorde långvarig elektrokardiografisk (EKG) övervakning i råttornas bankande hjärtan, även med kapillärblödning. De uppmätta EKG-signalerna uppvisade ett högt signal-brusförhållande (SNR) på 52 dB som ett resultat av den aktiva dataavläsningen.
I studien, den nya töjbara MEA designades noggrant med hjälp av toppmoderna ingenjörstekniker. Metoderna kombinerade organiska elektrokemiska transistorer med utomordentligt hög förstärkning (OECT) bearbetade på mikronätsubstrat med en poly(3-metoxipropylacetat) (PMC3A) beläggning. Processen underlättade betydande antitrombotiska egenskaper samtidigt som den bibehöll utmärkt jonledningsförmåga.
Vanligtvis, multielectrode arrays (MEA) används för att undersöka positionen för aktiva/inaktiva celler, spridning av neurala signaler och nätverk mellan flera neuroner. Matriserna kan också användas för att diagnostisera och behandla sjukdomar genom att mäta biologiska signaler på flera punkter. Den första rapporterade in vitro MEA tillverkades på platt glas för att mäta cellulär excitation i odlat myokardium, neuronala celler och spridning av signal från hjärta och hjärna skivor. De nyligen utvecklade icke-invasiva in vivo MEA-matriserna tillverkades på flexibel plastfolie med förmågan att komma i kontakt med mjuka och rörliga levande vävnader. Under ingenjörsprocessen, enhetens flexibilitet bör ökas för att underlätta MEAs på komplexa strukturer i kroppen under implantation.
Konform kontakt på skrynkliga hjärnytor, till exempel, kan uppnås genom att minska anordningens tjocklek under två µm. Liknande, EKG-mätningar kan utföras på huden nära hjärtat via passiva MEA på 3 µm polyimidsubstrat. De ultraflexibla egenskaperna hos aktiva MEAs demonstrerades genom smidig kontakt med muskelceller, cerebral cortex samt elektromyografi (EMG) och elektrokortikografi (ECoG) mätningar. En töjbar och blodkompatibel aktiv MEA har ännu inte realiserats på grund av två huvudsakliga begränsningar. I början, enhetsnedbrytning på grund av blodproppar från kirurgisk blödning som ett resultat av en hög Youngs modul sågs med polyimid- eller parylenpolymerer trots deras höga kompatibilitet. Därefter, det är också svårt att konstruera högpresterande aktiva element med töjbarhet för att mäta biologiska signaler. De aktiva elementen krävde också höga förstärkningsfaktorer och låga drivspänningar.
I studien, Lee et al. konstruerade en ultratunn, töjbar rutmönstermönstrad aktiv OECT-matris (organisk elektrokemisk transistor) för att mäta fördelningen av EKG-signaler med ett signal-brusförhållande (SNR) på 52 dB via direktkontakt på råtthjärtat som slår. Den aktiva 4 x 4 OECT-matrisen tillverkades med en total tjocklek på 2,6 µm och hög transkonduktans. Anordningen var helt belagd med 100 nm tjock poly(3-metoxipropylacetat) (PMC3A) för att ge antitrombotiska egenskaper samtidigt som utmärkt jonledningsförmåga bibehölls. Ett EKG kartlades från hjärtytan på en råtta för att bestämma genomförbarheten av 4 x 4, ultratunna, töjbar, antitrombotisk och aktiv OECT-array. På grund av hög anpassningsförmåga hos nätstrukturen, artefaktbrus orsakat av dynamisk rörelse förekom inte i den inspelade datan. Dessutom, på grund av dess antitrombotiska egenskaper, enheten var kapabel till stabila mätningar över långa tidsperioder, även i en implantatmiljö med konsekvent blödning.
Den töjbara MEA som innehåller OECTS och rutnätssubstrat tillverkades på 1,2 µm parylensubstrat. De aktiva lagren i en tunn poly(3, 4-etylendioxitiofen)polystyrensulfonat (PEDOT:PSS)-systemet och ledningar åstadkoms på ett bikakenätsubstrat. Den bikakeformade gallerstrukturen möjliggjorde mekanisk stabilitet och strukturell sträckbarhet, tidigare undersökt experimentellt och via simulering. Det yttersta PMC3A-skiktet [poly(3-metoxipropylacetat)] möjliggjorde hög blodkompatibilitet för att bibehålla antitrombogenicitet. Enhetens sträckbarhet möjliggjorde dynamisk rörelse på biologiska substrat.
Innan man utförde biologiska experiment in vivo, författarna bedömde systematiskt enhetens elektriska och mekaniska karaktär. Den elektriska prestandan mättes i förhållande till arrayens transkonduktans, som indikerade tillräckligt stora kvantiteter för att mäta ECoG- eller EMG-signalerna från råttor. Tjockleken och vattenkontaktvinkeln på PMC3A-ytorna visade överensstämmande resultat jämfört med tidigare studier. Hemokompatibilitetsstudier på PMC3A utfördes med användning av trombocytvidhäftning genom att doppa prover i blodplättssuspensioner extraherade från humant blod. Svarstiden (τ) för OECTs före och efter PMC3A-beläggning mättes efter att en grindspänningspuls applicerats med en varaktighet på en millisekund, vilket indikerar att doppningsprocessen för PMC3A inte ändrade OECTs elektriska egenskaper. OECT-belagda PMC3As bekräftade också långsiktig elektrisk stabilitet.
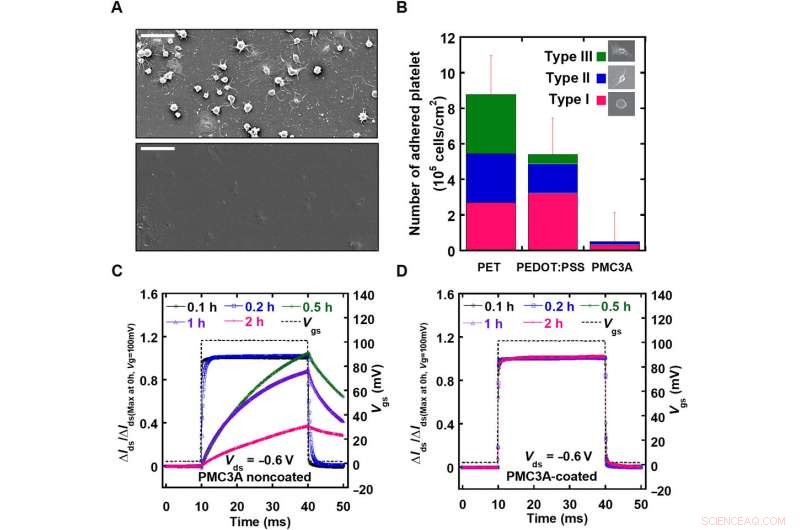
Utvärdering av blodkompatibiliteten för PMC3A-beläggning på OECTs. A) SEM-bilden av polyetylentereftalat (PET) och PMC3A-belagd film observerad efter 1 timmes vidhäftning av blodplättar. B) Det genomsnittliga antalet vidhäftade blodplättar på PET-film jämfört med PEDOT:PSS- och PMC3A-filmer efter 1 timmes trombocytvidhäftning. C) Efter trombocytvidhäftning med vidhäftningstider på 0,1-2 timmar, τ-värdena för OECTs med eller utan PMC3A-beläggning mättes genom att applicera en grindspänningspuls med en varaktighet på 50 ms. D) Utmärkt ytblodkompatibilitet möjliggjorde långvarig EKG-signalövervakning. Upphovsman:Science Advances, doi:10.1126/sciadv.aau2426
Forskarna genomförde sedan in vivo-studier i en råttmodell där genomförbarheten av de töjbara och hemokompatibla OECT-matriserna utfördes via EKG-mätningar på hjärtytor. De fysiologiska signalerna mättes med användning av 4 x 4 arrayen av sträckbara och hemokompatibla OECT:er genom att fästa dem på den exponerade ytan av hjärtat. Bikakehålen i det ultratunna substratet tillät konform kontakt mellan enhetens film och hjärtytan.
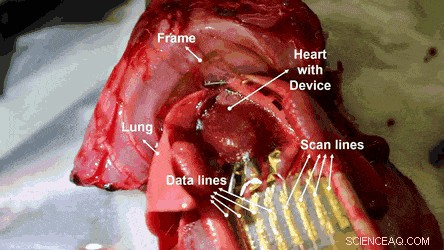
Elektroanatomisk kartläggning på en hjärtyta med aktiv MEA på det ultratunna bikakenätsubstratet. Upphovsman:Science Advances, doi:10.1126/sciadv.aau2426
Signal-brusförhållandet för den PMC3A-belagda OECT registrerad vid 51 dB 30 minuter efter fastsättning liknade värdet som registrerades direkt efter fastsättning. Den millisiemensordning av transkonduktans som observerades i studien berodde på vattenpermeabiliteten hos PEDOT:PSS. Som ett resultat, transkonduktansen för OECT var 100 gånger högre än den för Si-fälteffekttransistorerna (FET).
Forskarna demonstrerade också EKG-kartläggningssignaler med hjälp av OECT-arrayen när enheten placerades på en råtthjärtayta som täcker de vänstra och högra ventrikelområdena. Belastningsimpedansen utformades för att vara 0 ohm för att väsentligt undertrycka överhörningen i OECT-matrisen, som tidigare demonstrerats. Rumsliga spänningskartor för alla noder vid fyra sekventiella tidpunkter visualiserades. Baserat på sensorns plats, de anatomiska signalerna visade olika former. De töjbara och blodkompatibla OECT-matriserna registrerade framgångsrikt spatial-temporal distribution av EKG på råttas hjärtaytor med multiplexering.
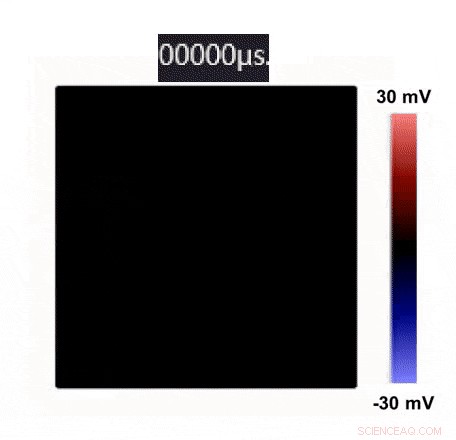
Den elektroanatomiska kartläggningen på en hjärtyta genom multiplexering. Upphovsman:Science Advances, doi:10.1126/sciadv.aau2426
I studien, ett högt SNR på 52 dB uppnåddes av två skäl; först, eftersom författarna lyckats använda OECT med hög transkonduktans i storleksordningen millisiemen. Högre med en faktor 10 jämfört med enkristall Si FET i närvaro av kirurgisk blödning, medan PMC3A-beläggningen samtidigt bibehöll hög jonledningsförmåga. Andra, rörelseartefaktbruset undertrycktes av den höga anpassningsförmågan hos mikronätsarkitekturen:enheten kan fästa vid det dynamiska målet under hjärtats rörelse. De töjbara och aktiva MEA med icke-trombogen PMC3A-beläggning kommer att möjliggöra mätningar av EKG, ECoG- eller EMG-signaler med högre noggrannhet i ytterligare prekliniska studier.
© 2018 Science X Network