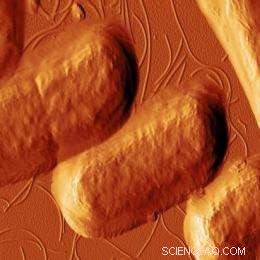
Denna bilden, taget med atomkraftsmikroskopi, visar E. coli-bakterier efter att de har exponerats för den antimikrobiella peptiden CM15. Peptiderna har börjat förstöra bakteriens cellväggar. Bild:Georg Fantner
I två decennier, forskare har strävat efter ett potentiellt nytt sätt att behandla bakterieinfektioner, använder naturligt förekommande proteiner som kallas antimikrobiella peptider (AMP). Nu, MIT-forskare har spelat in de första mikroskopiska bilderna som visar de dödliga effekterna av AMP, de flesta dödar genom att sticka hål i bakteriecellsmembran.
Forskare ledda av MIT-professor Angela Belcher modifierade en befintlig, extremt känslig teknik känd som höghastighets atomkraftsmikroskopi (AFM) för att låta dem avbilda bakterierna i realtid. Deras metod, beskrivs i den 14 mars onlineupplagan av Naturens nanoteknik , representerar det första sättet att studera levande celler med hjälp av högupplösta bilder inspelade i snabb följd.
Att använda denna typ av höghastighets-AFM kan tillåta forskare att studera hur celler svarar på andra droger och på virusinfektion, säger Belcher, Germeshausen professor i materialvetenskap och teknik och biologisk teknik och medlem av Koch Institute for Integrative Cancer Research vid MIT.
Det kan också vara användbart för att studera celldöd i däggdjursceller, såsom nervcellsdöd som inträffar hos Alzheimers patienter, säger Paul Hansma, en fysikprofessor vid University of California i Santa Barbara som har utvecklat AFM-teknik i 20 år. "Denna uppsats är ett mycket betydande framsteg inom den senaste avbildningen av cellulära processer, säger Hansma, som inte var involverad i forskningen.
Hög hastighet
Atomkraftsmikroskopi, uppfanns 1986, används ofta för att avbilda material i nanoskala. Dess upplösning (cirka 5 nanometer) är jämförbar med den för elektronmikroskopi, men till skillnad från elektronmikroskopi, den kräver inget vakuum och kan därför användas med levande prover. Dock, traditionell AFM kräver flera minuter för att producera en bild, så det kan inte registrera en sekvens av snabbt inträffande händelser.
På senare år har forskare har utvecklat höghastighets AFM-tekniker, men har inte optimerat dem för levande celler. Det var vad MIT-teamet ville göra, bygger på erfarenheten från huvudförfattaren Georg Fantner, en postdoktor i Belchers labb som hade arbetat med höghastighets AFM vid University of California i Santa Barbara.
Atomkraftsmikroskopi använder sig av en fribärare utrustad med en sondspets som "känner" ytan på ett prov. Krafter mellan spetsen och provet kan mätas när sonden rör sig över provet, avslöjar ytans form. MIT-teamet använde en cantilever ca 1, 000 gånger mindre än de som normalt används för AFM, vilket gjorde det möjligt för dem att öka bildhastigheten utan att skada bakterierna.
Mätningarna utförs i en flytande miljö, en annan kritisk faktor för att hålla bakterierna vid liv.
Med den nya inställningen, teamet kunde ta bilder var 13:e sekund under en period av flera minuter efter behandling med en AMP känd som CM15. De fann att AMP-inducerad celldöd verkar vara en process i två steg:en kort inkubationsperiod följt av en snabb "avrättning". De blev förvånade över att se att början av inkubationsperioden varierade från 13 till 80 sekunder.
"Inte alla celler började dö exakt samtidigt, även om de var genetiskt identiska och exponerades för peptiden samtidigt, säger Roberto Barbero, en doktorand i biologisk teknik och författare till tidningen.
De flesta AMPs verkar genom att punktera bakteriecellsmembran, som förstör den känsliga jämvikten mellan bakterien och dess omgivning. Andra verkar rikta in sig på maskiner inne i cellen. Det har funnits ett stort intresse för att utveckla AMP som läkemedel som kan komplettera eller ersätta traditionella antibiotika, men ingen har godkänts ännu.
Tills för några år sedan, man trodde att bakterier inte kunde bli resistenta mot AMPS, men nyare studier har visat att de kan. Det nya MIT-arbetet kan hjälpa forskare att förstå hur den resistensen utvecklas.