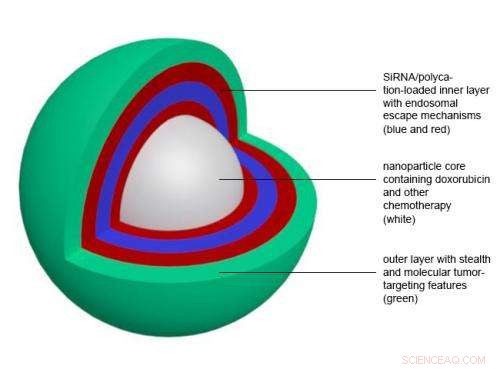
Schematisk ritning av en ny nanopartikel utvecklad vid MIT. Kredit:FORSKARNA
En aggressiv form av bröstcancer känd som "trippelnegativ" är mycket svår att behandla:Kemoterapi kan krympa sådana tumörer ett tag, men hos många patienter växer de ut igen och blir motståndskraftiga mot originalläkemedlen.
För att övervinna det motståndet, MIT kemiingenjörer har designat nanopartiklar som bär cancerläkemedlet doxorubicin, samt korta RNA-strängar som kan stänga av en av generna som cancerceller använder för att fly läkemedlet. Denna "ett-två slag" inaktiverar tumörernas försvar och gör dem mycket mer sårbara för kemoterapi.
"Det ger dig, övergripande, ett mycket effektivare system vid en lägre dos, eftersom du kan rikta in dig på dessa celler och se till att var och en av dem får rätt synergistisk dosering av de två komponenterna, säger Paula Hammond, David H. Koch professor i teknik, medlem av MIT:s Koch Institute for Integrative Cancer Research, och ledare för forskargruppen.
Genom att använda dessa partiklar, forskarna kunde krympa trippelnegativa brösttumörer hos möss, de rapporterar i den 21 oktober onlineupplagan av tidskriften ACS Nano . Partiklarna kan också anpassas för att behandla andra typer av cancer, säger forskarna.
Huvudförfattare till tidningen är Jason Deng, en postdoc i Hammonds labb. Andra författare är MIT doktorand Stephen Morton, junior Elana Ben-Akiva, och postdoktorerna Erik Dreaden och Kevin Shopsowitz.
Leverans enligt design
Trippelnegativa brösttumörer saknar de tre vanligaste bröstcancermarkörerna:östrogenreceptor, progesteronreceptor, och Her2. Forskare har utvecklat behandlingar som riktar sig mot var och en av dessa markörer, som har förbättrat överlevnaden för dessa cancerformer.
"Typiskt har dessa personliga terapier varit mycket mer effektiva än att bara skölja med ett kemoterapiläkemedel, eftersom de kommer åt hur tumörceller fungerar. Dock, vi har inte haft det för trippelnegativ bröstcancer, " säger Hammond.
Hon hoppas att de nya nanopartiklarna, som riktar sig mot ett protein som finns på ytan av trippelnegativa bröstcancerceller, kommer att hjälpa till att ändra på det. Nanopartiklarna har tre komponenter:en kärna fylld med doxorubicin, en beläggning av kort interfererande RNA (siRNA), och ett yttre skikt som skyddar partikeln från nedbrytning i blodomloppet.
Doxorubicin, ett läkemedel som dödar celler genom att skada deras DNA, används redan för att behandla bröstcancer och andra cancerformer, inklusive lungor, äggstockar, och sköldkörteln. Forskarna baserade sina nanopartiklar på en Food and Drug Administration-godkänd form av läkemedlet som kallas Doxil, som är förpackad i en liposom, eller fettmembran.
För att förbättra Doxils effektivitet, Hammonds team ville kombinera det med en annan typ av terapi som kallas RNA-interferens (RNAi), som använder mycket korta RNA-strängar för att blockera uttrycket av specifika gener inuti en levande cell.
Forskarna använde en teknik som kallas lager-för-lager för att belägga Doxil-partiklarna med ett lager siRNA blandat med en positivt laddad polymer som hjälper till att stabilisera RNA. Detta lager innehåller upp till 3, 500 siRNA-molekyler, var och en avsedd att blockera en gen som tillåter cancerceller att pumpa ut läkemedelsmolekylerna ur cellerna.
En av de stora utmaningarna som forskare har ställts inför när det gäller att utveckla RNAi som cancerbehandling är att få partiklarna att överleva i blodomloppet tillräckligt länge för att nå sina avsedda mål. För att övervinna detta, MIT-partiklarna inkluderar en yttre beläggning av hyaluronsyra. Dessa molekyler absorberar vatten, låter nanopartiklarna strömma genom blodkärlen ostört, säger Hammond.
"Detta smygskikt blir en vattenkudde som omger nanopartikeln, som låter den gå genom blodomloppet som om det vore vatten, " säger Hammond. "Det gör att den cirkulerar mycket mer effektivt."
Hyaluronsyra hjälper också till att rikta partiklarna till tumörerna genom att binda till ett protein som kallas CD44, som finns i stort överflöd på ytan av trippelnegativa bröstcancerceller.
De nya partiklarna är ett bra exempel på att bygga "smartare" läkemedel för att behandla cancer, säger Yuri Lvov, en professor i mikro- och nanosystem vid Louisiana Tech University som inte ingick i forskargruppen. "Det är inte en ny drog, men som ingenjörer har de byggt ett nytt fordon för leverans baserat på nanoteknikprinciper. Det här nya verktyget är väldigt bra."
Krympande tumörer
I en studie av möss, forskarna fann att nanopartiklarna överlevde i blodomloppet mycket längre än någon RNA-leveranspartikel de tidigare har testat, med en halveringstid på 28 timmar. Detta ger dem en mycket större chans att nå tumören.
Nanopartiklarna konstruerades för att frigöra siRNA-nyttolasten i en snabbare takt än doxorubicin när de når tumörställena. "Det ger oss en chans att först sänka försvaret av tumörcellerna genom att stänga av denna proteinpump, och sedan slår läkemedlet in för att döda tumörcellerna, " säger Deng.
För att studera nanopartiklarnas förmåga att bekämpa cancer, forskarna injicerade dem i möss med mänskliga trippelnegativa tumörceller implanterade under huden. Efter en injektion, de fann att målgenen redan tystades. Efter 15 dagar och tre injektioner, tumörer hade minskat betydligt.
Forskarna tror att detta system också kan användas för att rikta in sig på många andra typer av cancer genom att byta ut läkemedlet som finns i kärnan, siRNA-målet, och ytpartiklarna som riktar sig mot tumören. De testar nu partiklarna i en mer komplex musmodell av trippelnegativ bröstcancer, och de arbetar också med att anpassa partiklarna för att behandla äggstockscancer och lungcancer.
Den här historien återpubliceras med tillstånd av MIT News (web.mit.edu/newsoffice/), en populär webbplats som täcker nyheter om MIT-forskning, innovation och undervisning.