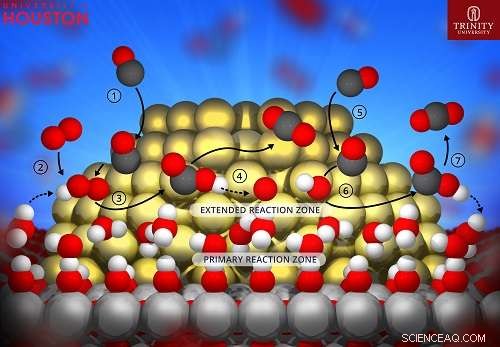
Schematisk bild av den lägsta energibanan för CO-oxidation på guld-titania-katalysatorer. Vattenskiktet på titania -stödet förlänger reaktionszonen på guld -nanoklusterna och tillhandahåller protoner som hjälper till i syredissocieringssteget. Upphovsman:Hieu Doan, University of Houston
Forskare från University of Houston och Trinity University har för första gången gett direkt bevis på en vattenmedierad reaktionsmekanism för katalytisk oxidation av kolmonoxid.
Arbetet använde guldnanopartiklar och titandioxid som katalysator för att påskynda processen och bestämde att vatten fungerar som en samkatalysator för reaktionen som omvandlar kolmonoxid till koldioxid. Medan forskare har arbetat med kolmonoxidoxidation med hjälp av guldkatalysatorer i åratal och insett att vatten kan förändra reaktionen, ingen har tidigare kunnat helt förklara varför det fungerade.
Arbetet beskrivs i tidningen 5 september Vetenskap .
"Vi kan med stor säkerhet säga att vi nu förstår rollen för var och en av komponenterna och vad de gör under denna katalytiska reaktion, sa Lars Grabow, biträdande professor i kemisk och biomolekylär teknik vid University of Houston. Han och Hieu Doan, en doktorsexamen student vid UH Cullen College of Engineering, utvecklat beräkningssimuleringar för att stödja experiment som körs av Trinity University -kemisterna Bert Chandler, Christopher Pursell och Johnny Saavedra.
Chandler, professor i kemi vid Trinity, sa att arbetet var ett sant samarbete.
"Det tog oss alla att få det att hända, "sa han." Det vi gjorde är att överbrygga klyftan mellan ytvetenskap och beräkningsmänniskor. Vi visste att vatten hjälpte reaktionen men förstod inte helt dess roll. Nu vet vi att vatten är en samkatalysator för denna reaktion. "
När det används i smycken, guld är uppskattat för sina icke -reaktiva egenskaper - det rostar inte eller smutsar när det utsätts för luft eller vatten. Och forskare har länge vetat att trots sitt rykte som en inert metall, guldnanopartiklar kan fungera som en katalysator för att påskynda kemisk reaktion.
Men ingen visste exakt varför det fungerade. Vatten visade sig vara nyckeln, även om det inte uttryckligen läggs till i processen, Sa Grabow.
Spårmängder vatten som sugs ut från luften drev reaktionerna på ytan av guldkatalysatorerna, han sa.
Under experimenten och beräkningsstudien, forskarna tittade på hur vatten, ythydroxyler och metallstödgränssnittet interagerade under kolmonoxidoxidation över en guld-titandioxidkatalysator.
"I samtliga fall, en väsentligen barriärfri protonöverföring sänkte systemets totala energi, generera H2O2 eller OOH. När OOH väl bildats, den vandrade längs Au -partikeln, tillåter atomer nära, men inte strikt, metallstödgränssnittet för att delta i reaktionen, "De skrev för att beskriva sina resultat, med hänvisning till alstring av väteperoxid eller hydroperoxyl och hydroperoxyls vandring längs guldpartiklarna.
Väsentligen, de fann att protoner från ett tunt lager av vatten som sträcker sig över katalysatorns yta lossnar från vattenmolekylerna och fäster vid syremolekyler, förflyttas kortvarigt på ytan av katalysatorn för att stimulera reaktionen innan den återgår till vattenskiktet.
Tidigare modeller fokuserade vanligtvis på enskilda komponenter i reaktionen, Grabow sa, vilket gör det här projektet till det första att dra ihop alla fasetter i en enda modell som fullt ut stöder treenighetskemisternas experimentella observationer. Chandler sa att arbetet kan ge ett sätt att producera rent väte från petroleum och naturgas.