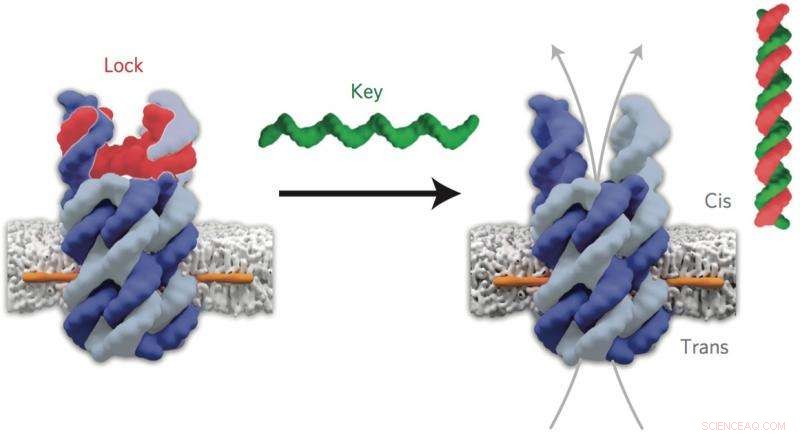
Det "låsta" DNA (rött) i den slutna nanoporen binder med "nyckel" -DNA (grönt) för att öppna kanalen. Upphovsman:Jonathan Burns et al. Naturnanoteknik, DOI 10.1038/nnano.2015.279
DNA har använts som en "molekylär byggsten" för att konstruera syntetiskt bioinspirerade porer som kommer att förbättra hur läkemedel levereras och hjälpa till att främja syntetisk biologi, enligt forskare från UCL och Nanion Technologies.
Studien, publicerad idag i Naturnanoteknik och finansieras av Biotechnology and Biological Sciences Research Council (BBSRC), Leverhulme Trust och UCL Chemistry, visar hur DNA kan användas för att bygga stabila och förutsägbara porer som har en definierad form och laddning för att kontrollera vilka molekyler som kan passera genom porerna och när.
Huvud författare, Dr Stefan Howorka (UCL Chemistry), sade:"Naturliga biologiska porer gjorda av proteiner är avgörande för att transportera gods in och ut ur biologiska celler men de är svåra att designa från grunden. DNA erbjuder en helt ny strategi för att konstruera högspecifika syntetiska porer som vi kan öppna och stänga vid behov. Vi har konstruerat våra porer för att fungera som dörrar - dörren låses bara upp när den är försedd med rätt nyckel. Genom att bygga dessa porer till droger, vi tror att det kommer att möjliggöra mycket mer exakt inriktning av terapier. "
Många läkemedel, inklusive cancerläkemedel, kan fraktas runt i kroppen i små bärare som kallas vesiklar som är riktade mot olika vävnader med hjälp av biologiska markörer. Tidigare, frisläppande av läkemedlen inuti blåsorna utlöstes med temperaturinducerade läckande blåsväggar eller med insatta peptidkanaler, som är mindre styva och förutsägbara än DNA.
Med hjälp av DNA -byggstenar, laget designade porer med förutbestämda strukturer och definierade egenskaper som var exakt förankrade i väggarna - eller membranen - hos vesiklar.
"Våra porer har formen av en öppen fat gjord av sex DNA-stavar. Vi konstruerade en molekylär grind för att stänga av en ingång men öppnar sedan kanalen igen när en specifik molekyl binds. Ankare med hög membranaffinitet fästes för att binda vattnet -lösliga porer i det oljiga membranet, "förklarade första författaren, Dr Jonathan Burns (UCL Chemistry).
Med hjälp av elektrofysiologiska tekniker, forskarna verifierade att poren vertikalt sträckte sig över membranets yta och var stabil med en invändig bredd på 2 nm, vilket är en lämplig storlek för små läkemedelsmolekyler att passa igenom.
Portens låsmekanism testades sedan med såväl elektrofysiologiska tekniker som med fluoroforer, som är lika stora som små molekyler. Eftersom DNA -poren hade en negativ negativ laddning, fluoroforer med en negativ negativ laddning rörde sig lättare än de med en positiv nettoladdning, visar selektivitet för vilken last kan komma ut. Att ta bort låset med en matchande nyckel ökade trafiken 140 gånger jämfört med en nyckel som inte matchade.
Medförfattare Astrid Seifert som arbetar med Dr Niels Fertig på Nanion Technologies, sa:"Vi kunde exakt analysera prestanda för var och en av porerna vi skapade. Vi satte först in porer i membran och testade sedan det biofysiska svaret för varje kanal med hjälp av avancerade mikrochips. Vi har inte bara utvecklat ett nytt sätt att designa mycket specifika porer men också en automatiserad metod för att testa deras egenskaper in situ, vilket kommer att vara viktigt för att testa porer som används för riktad läkemedelsleverans i framtiden. "
Forskarna planerar att testa de syntetiska porerna i en mängd olika scenarier, inklusive frisättning av cancerläkemedel till celler och utveckling av porer som frigör farmaceutiskt aktiva biomolekyler.
Dr Howorka la till, "Vår strategi är ett stort steg framåt när det gäller att bygga och använda syntetiska biologiska strukturer och lovar en ny era inom poredesign och syntetisk biologi. Vi har visat så exakt kontroll över beteendet hos porerna, både när det gäller selektivitet och när det gäller lyhördhet som vi tror att metoden banar väg för ett brett spektrum av applikationer från läkemedelsleverans till nanosensing. "