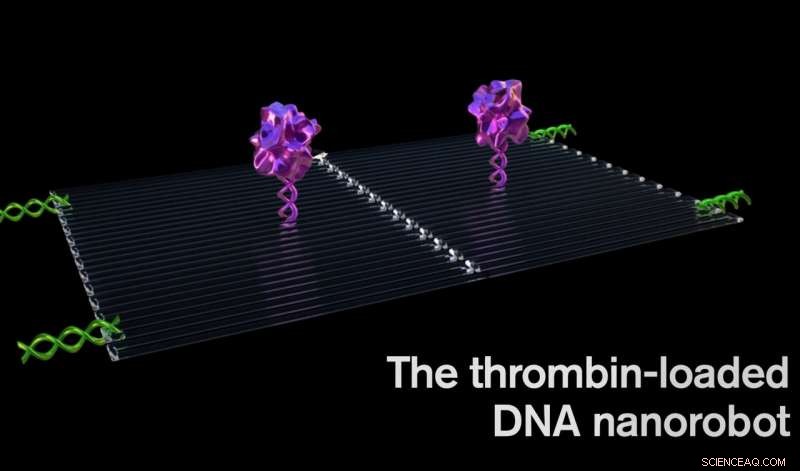
Trombin kan blockera tumörblodflödet genom att koagulera blodet i kärlen som matar tumörtillväxt, orsakar en sorts tumör-mini-hjärtattack, och leder till tumörvävnadsdöd. Kredit:Jason Drees, Arizona State University
I ett stort framsteg inom nanomedicin, Arizona State University (ASU) forskare, i samarbete med forskare från National Centre for Nanoscience and Technology (NCNST), av den kinesiska vetenskapsakademin, har framgångsrikt programmerat nanorobotar att krympa tumörer genom att stänga av deras blodtillförsel.
"Vi har utvecklat den första helt autonoma, DNA-robotsystem för en mycket exakt läkemedelsdesign och riktad cancerterapi, sa Hao Yan, chef för ASU Biodesign Institute's Center for Molecular Design and Biomimetics och Milton Glick-professorn vid School of Molecular Sciences.
"Dessutom, denna teknik är en strategi som kan användas för många typer av cancer, eftersom alla blodkärl som matar solida tumörer är i huvudsak desamma, sa Yan.
Den framgångsrika demonstrationen av tekniken, den första i sitt slag studie på däggdjur som använder bröstcancer, melanom, äggstocks- och lungcancermusmodeller, publicerades i tidskriften Naturens bioteknik .
Sök och förgör
Yan är expert inom området DNA-origami, som under de senaste två decennierna, har utvecklat tillverkning i atomär skala för att bygga fler och mer komplexa strukturer.
Tegelstenarna för att bygga deras strukturer kommer från DNA, som själv kan vikas till alla möjliga former och storlekar - allt i en skala som är tusen gånger mindre än bredden på ett människohår - i hopp om att en dag revolutionera datoranvändningen, elektronik och medicin.
Den ena dagen kan komma lite snabbare än väntat.
Nanomedicin är en ny gren av medicin som försöker kombinera löftet om nanoteknik för att öppna upp helt nya vägar för behandlingar, som att göra minimala, nanopartiklar i molekylstorlek för att diagnostisera och behandla svåra sjukdomar, speciellt cancer.
Tills nu, utmaningen att utveckla nanomedicin har varit svår eftersom forskare ville designa, bygga och noggrant kontrollera nanorobotar för att aktivt söka och förstöra cancertumörer – utan att skada några friska celler.
Det internationella teamet av forskare övervann detta problem genom att använda en till synes enkel strategi för att mycket selektivt söka och svälta ut en tumör.
Detta arbete inleddes för cirka 5 år sedan. NCNST-forskarna ville först specifikt stänga av tumörblodtillförseln genom att inducera blodkoagulering med hög terapeutisk effekt och säkerhetsprofiler i flera solida tumörer med hjälp av DNA-baserade nanobärare. Prof. Hao Yans expertis har uppgraderat nanomedicindesignen till ett helt programmerbart robotsystem, kunna utföra sitt uppdrag helt på egen hand.
"Dessa nanorobotar kan programmeras för att transportera molekylära nyttolaster och orsaka blockering av tumörblodtillförseln på plats, vilket kan leda till vävnadsdöd och krympa tumören, sa Baoquan Ding, en professor vid NCNST, ligger i Peking, Kina.
Nanorobotar till undsättning
För att utföra sina studier, forskarna utnyttjade en välkänd mustumörmodell, där mänskliga cancerceller injiceras i en mus för att inducera aggressiv tumörtillväxt.
När tumören väl växte, nanorobotarna sattes in för att komma till undsättning.
Varje nanorobot är gjord av en platt, rektangulärt DNA origami ark, 90 nanometer gånger 60 nanometer i storlek. Ett viktigt blodkoagulerande enzym, kallas trombin, är fäst på ytan.
Trombin kan blockera tumörblodflödet genom att koagulera blodet i kärlen som matar tumörtillväxt, orsakar en sorts tumör-mini-hjärtattack, och leder till tumörvävnadsdöd.
Först, ett genomsnitt av fyra trombinmolekyler fästes till en platt DNA-ställning. Nästa, det platta arket veks in på sig självt som ett pappersark till en cirkel för att göra ett ihåligt rör.
De injicerades med en IV i en mus, reste sedan genom hela blodomloppet, siktar in sig på tumörerna.
Nyckeln till att programmera en nanorobot som bara attackerar en cancercell var att inkludera en speciell nyttolast på dess yta, kallas en DNA-aptamer. DNA-aptameren kan specifikt rikta sig mot ett protein, kallas nukleolin, som görs i stora mängder endast på ytan av tumörendotelceller - och inte finns på ytan av friska celler.
När den väl är bunden till tumörens blodkärlsyta, nanoroboten programmerades, som den ökända trojanska hästen, att leverera sin intet ont anande droglast i själva hjärtat av tumören, exponerar ett enzym som kallas trombin som är nyckeln till blodkoagulering.
Nanorobotarna arbetade snabbt, samlas i stort antal för att snabbt omge tumören bara timmar efter injektionen.
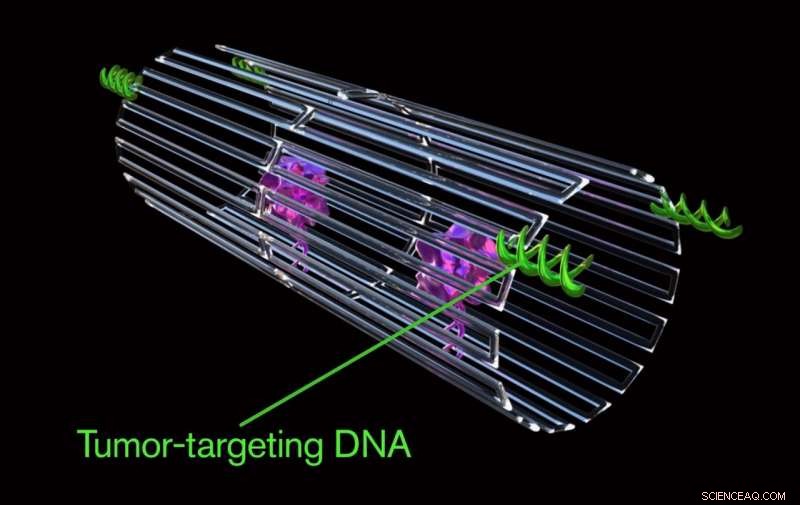
Nyckeln till att programmera en nanorobot som bara attackerar en cancercell var att inkludera en speciell nyttolast på dess yta, kallas en DNA-aptamer. DNA-aptameren kan specifikt rikta sig mot ett protein, kallas nukleolin, som görs i stora mängder endast på ytan av tumörendotelceller - och inte finns på ytan av friska celler. Kredit:Jason Drees, Arizona State University
Säker och ljuddesign
Först och främst, teamet visade att nanorobotarna var säkra och effektiva för att krympa tumörer.
"Nanoroboten visade sig vara säker och immunologiskt inert för användning i normala möss och, även i Bama miniatyrgrisar, visar inga påvisbara förändringar i normal blodkoagulation eller cellmorfologi, sa Yuliang Zhao, också professor vid NCNST och ledande forskare i det internationella samarbetsteamet.
Viktigast, det fanns inga bevis för att nanorobotarna spred sig in i hjärnan där de kunde orsaka oönskade biverkningar, såsom stroke.
"Nanorobotarna är definitivt säkra i normala vävnader hos möss och stora djur, " sa Guangjun Nie, ytterligare en professor vid NCNST och en nyckelmedlem i samarbetsgruppen.
Behandlingen blockerade tumörens blodtillförsel och genererade tumörvävnadsskada inom 24 timmar utan att ha någon effekt på friska vävnader. Efter att ha attackerat tumörer, de flesta av nanorobotarna rensades och degraderades från kroppen efter 24 timmar.
Efter två dagar, det fanns tecken på framskriden trombos, och 3 dagar, tromber i alla tumörkärl observerades.
Nyckeln är att utlösa trombin endast när det är inuti tumörens blodkärl. Också, i melanommusmodellen, 3 av 8 möss som fick nanorobotterapi visade fullständig regression av tumörerna. Medianöverlevnadstiden mer än fördubblades, sträcker sig från 20,5 till 45 dagar.
De provade också sitt system i ett test av en primär muslungcancermodell, som efterliknar det mänskliga kliniska förloppet hos lungcancerpatienter. De visade krympning av tumörvävnader efter en 2-veckors behandling.
Vetenskapen om det mycket små går stort
För Yan, den viktiga milstolpen i studien representerar slutet på början för nanomedicin.
"DNA-nanoroboten för trombinleverans utgör ett stort framsteg i tillämpningen av DNA-nanoteknologi för cancerterapi, " sa Yan. "I en melanommusmodell, nanoroboten påverkade inte bara primärtumören utan förhindrade också bildandet av metastaser, visar lovande terapeutisk potential."
Yan och hans medarbetare söker nu aktivt kliniska partners för att vidareutveckla denna teknik.
"Jag tror att vi är mycket närmare verkligheten, praktiska medicinska tillämpningar av tekniken, ", sade Yan. "Kombinationer av olika rationellt utformade nanorobotar som bär olika medel kan hjälpa till att uppnå cancerforskningens slutmål:utrotning av solida tumörer och vaskulariserade metastaser. Vidare, den nuvarande strategin kan utvecklas som en läkemedelsleveransplattform för behandling av andra sjukdomar genom modifiering av nanostrukturernas geometri, målgrupperna och de lastade lasterna."