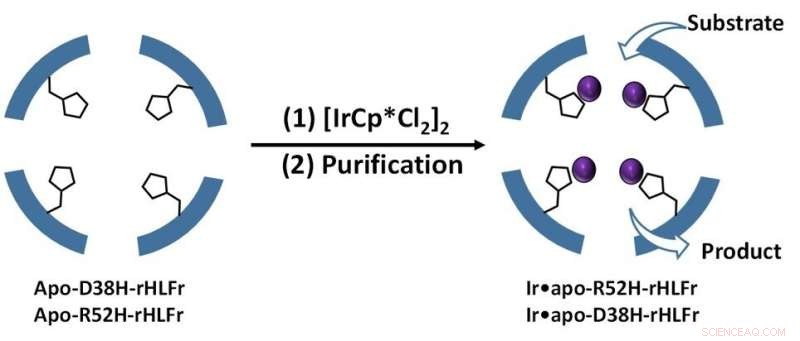
Figur 1. Buren konstruerades med aminosyraersättningar genom att introducera platsspecifika mutationer som möjliggjorde mer IrCp*-upptag. Kredit:Takafumi Ueno från Tokyo Institute of Technology
En ny hybrid ferritin-nanocage med histidinrester visar 1,5 gånger högre metalljonupptag och förbättrad katalytisk effektivitet för alkoholproduktion, enligt forskare från Tokyo Tech i en ny studie. Deras resultat tyder på att hybrid bio-nanocages effektivt kan katalysera reaktioner för att ge industriellt viktiga produkter.
Biologiska polymerer kan spontant självmontera till komplexa strukturer som liknar kärl eller burar, men är mycket mindre, och kallas "nano-burar". Dessa strukturer kan rymma ett brett utbud av molekyler inuti dem som beter sig som "gäster". Ett populärt exempel är "ferritin nanocage", som bildas av självmontering av 24 subenheter till proteinet ferritin och kan innesluta metalljoner som är viktiga katalysatorer. Med hjälp av dessa metalljoner omvandlar en katalytisk reaktion vilket substrat som helst till en produkt. Även om det är allmänt känt, har ferritinburens potentiella tillämpningar i industrin ännu inte utforskats fullt ut.
Hittills har de flesta ansträngningar att öka metalljonupptaget i ferritin resulterat i burar med låg stabilitet. För att få "gästen" att sitta bra i buren är effektiv design nyckeln. Med det i åtanke introducerade ett team av forskare under ledning av prof. Takafumi Ueno, från Tokyo Institute of Technology, Japan (Tokyo Tech), platsspecifika mutationer i kärnan av ferritin-nanocage och ökade dess upptag av iridiumkomplex (IrCp*) ). Deras resultat publiceras i Angewandte Chemie . Iridium är en viktig katalysator i alkoholproduktionsvägen och används kommersiellt inom läkemedels-, livsmedels- och kemisk industri.
Prof. Ueno förklarar, "Baserat på tidigare litteratur visste vi att närvaron av koordinationsaminosyror i buren förbättrar iridiumaktiviteten och att ersättning av dessa aminosyror med lämpliga rester kan lindra problemet. Eftersom iridiumkomplex beter sig som en katalysator, kan koordination rester skulle göra jobbet." Författarna använde aminosyran histidin för att ersätta två rester, arginin och asparaginsyra i de vanliga (vildtyp) ferritinburarna och skapa mutanterna R52H och D38H. Anmärkningsvärt nog påverkades inte monteringsstrukturen eller burstorleken av dessa förändringar.
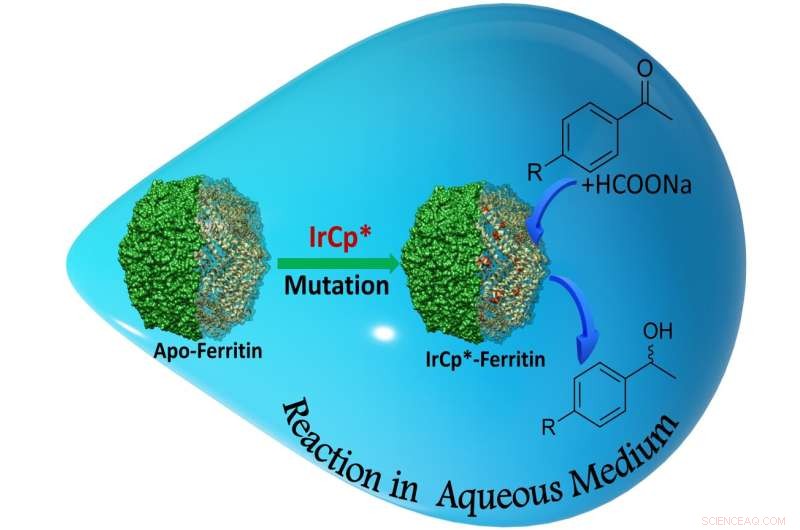
Figur 2. Nanocage fungerar som en hybrid biokatalysator under omvandlingen av substrat till alkoholer med hög specificitet. Kredit:Takafumi Ueno från Tokyo Institute of Technology
Därefter lade de till IrCp* till mutanterna och fann att R52H kunde bädda in 1,5 gånger fler iridiumatomer än vildtypsburen (Figur 1). Men det som slog dem var D38H-mutanten, som betedde sig exakt som vildtypen. Så varför hade inte båda mutationerna samma effekt? Enligt prof. Ueno, "Detta innebär att det inte bara är närvaron av histidinresten utan också dess position som är avgörande för att bestämma upptagningseffektiviteten i buren."
Med hjälp av de nya katalytiska burarna kunde forskarna uppnå alkoholproduktionshastigheter så höga som 88%. Uppenbarligen gynnade mutationerna en strukturell omarrangering av reaktionskomponenterna, vilket ökade omvandlingshastigheten (Figur 2).
För att förstå hur substratet betedde sig inuti buren använde forskarna simuleringar där substratmolekylerna kunde röra sig fritt inom nanocage. De observerade vissa interaktioner mellan substratet och histidin i R52H-mutanten, som inte fanns i vildtypsburen, dvs. substratet visade preferentiell bindning inom nanocage.
"Dessa hybrida bio-nanocages visade sig också vara mycket stabila, vilket tyder på att de skulle kunna användas som livskraftiga katalysatorer i industriella tillämpningar", avslutar prof. Ueno. Den nuvarande strukturbaserade designen av metalljonbindningsplatsforskningen skulle kunna utvecklas för att skapa nya ferritinmutanter med selektivt upptag av specifika gästmolekyler, för olika katalytiska tillämpningar inom den kemiska och farmaceutiska industrin. + Utforska vidare