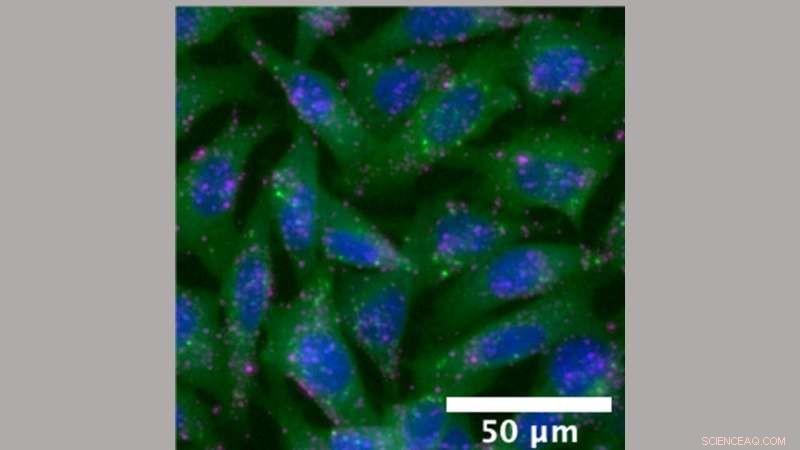
Mikroskopbild av cellerna som används för att testa nanopartiklar. Cellerna här är genetiskt modifierade för att fluorescera vid punkter där endosomer som bär nanopartiklar in i cellen öppnas. Kredit:Jordan Green; Johns Hopkins medicin
Johns Hopkins Medicine-forskare har utvecklat ett färgkodat test som snabbt signalerar om nyutvecklade nanopartiklar – ultrasmå fack utformade för att transportera mediciner, vacciner och andra terapier – levererar sin last till målcellerna. Historiskt sett har nanopartiklar en mycket låg leveranshastighet till cytosolen, insidan av cellerna, och frigör endast cirka 1%–2% av deras innehåll. Det nya testverktyget, konstruerat specifikt för att testa nanopartiklar, kan främja sökandet efter nästa generations biologiska läkemedel. Tekniken bygger på nanopartiklar som för närvarande används mot cancer och ögonsjukdomar, och i vacciner mot virus inklusive SARS-CoV-2, viruset som orsakar covid-19.
Forskarna rapporterar detaljer om verktyget, testat i musceller som odlats i laboratoriet och i levande möss, i numret 5 januari av Science Advances .
"Många av de nuvarande bedömningsverktygen för nanopartiklar testar bara om en nanopartikel når en cell, inte om terapin framgångsrikt kan fly den nedbrytande miljön i endosomen för att nå in i cellens cytosol, vilket är där läkemedlet måste placeras för prestanda", säger Jordan Green, Ph.D., professor i biomedicinsk teknik vid Johns Hopkins University School of Medicine. Det nya verktyget skapades för att spåra plats och frisättning av nanopartiklar, sa han.
Tidigare forskning har uppskattat att endast cirka 1%-2% av nanopartiklar "äts" av celler kan fly de cellulära avdelningarna som fångar dem för att undvika att smältas eller "spottas ut." Förutom egenskaperna hos dess last avgör en nanopartikels kemiska egenskaper om den accepteras av en cell och kan undvika dess cellulära försvar.
För att övervinna sådana hinder för slutleverans designade Green och hans team ett screeningsverktyg som bedömer hundratals nanopartikelformuleringar på deras förmåga att inte bara nå en cell, utan också hur effektivt nanopartikeln kan fly med sin last för att nå en cells inre.
Testet använder musceller som odlats i laboratoriet och som är genetiskt modifierade för att bära en fluorescerande markör som heter Gal8-mRuby, som lyser orangerött när ett cellulärt hölje som omsluter en nanopartikel öppnas och släpper ut sin last i cellen.
Bilder av processen analyseras sedan av ett datorprogram som snabbt spårar nanopartikelns plats med hjälp av rött fluorescerande ljus och kvantifierar hur effektiva nanopartiklarna är på att släppas ut i cellen genom att bedöma mängden orangerött fluorescerande ljus. Med denna teknik kan ett laboratorium screena hundratals unika nanopartiklar för leverans på några timmar, med detaljerad information om upptaget av nanopartiklarna och leveransen av deras last.
I experiment på möss administrerade Green och hans team biologiskt nedbrytbara nanopartiklar som bär på mRNA som kodade för en gen som kallas luciferas, vilket får cellerna att lysa. Forskarna spårade sedan om muscellerna accepterade genen och började uttrycka den – lysande upp målceller som en blixtbug.
Greens team fann att de bäst presterande nanopartiklarna i celltesterna hade en hög positiv korrelation till nanopartikelgenleveransprestanda i levande möss, vilket visar att nanopartikelanalysen är en bra prediktor för framgångsrik lastleverans.
I ytterligare musstudier upptäckte forskarna att olika kemiska gruppkombinationer i de polymerbaserade nanopartiklarna ledde till att nanopartiklarna riktade sig mot olika vävnadstyper. Genom att analysera hur partiklarna betedde sig i musens kropp fann forskarna att polymerens kemiska egenskaper kunde styra nanopartikelgenterapin till specifika målceller, såsom endotelceller i lungorna eller B-celler i mjälten.
"Genom att finjustera små kemiska förändringar kan vi styra en nanopartikel till specifika vävnader och till och med specifika celler", säger Green. "Detta skulle tillåta oss att utveckla mer exakt levererade terapier, vilket kan förbättra både effektivitet och säkerhet."
Nanopartikelleverans av biologiska läkemedel är ett växande område, särskilt för genterapier och vacciner.
Andra forskare som är involverade i studien inkluderar Yuan Rui, David R. Wilson, Stephany Y. Tzeng, Hannah M. Yamagata, Deepti Sudhakar, Cynthia A. Berlinicke och Donald J. Zack från Johns Hopkins University School of Medicine; Marranne Conge från Johns Hopkins University School of Medicine och Berea College; och Anthony Tuesca från AstraZeneca. + Utforska vidare