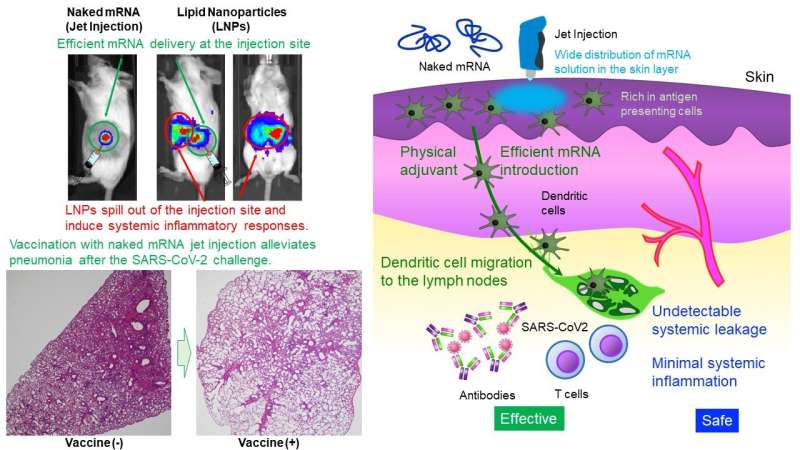
Uchida Laboratory of Innovation Center of NanoMedicine har visat att intradermal administrering av enbart mRNA (naket mRNA) utan skydd av nanopartiklar inducerade robust vaccination mot SARS CoV-2, ett virus som orsakar COVID-19, hos möss och primater. mRNA är mycket instabilt och anses allmänt kräva en liten kapsel, såsom lipidnanopartiklar (LNP), för administrering.
Metoden som rapporteras här är det första nakna mRNA-vaccinet som visar förebyggande mot SARS-CoV-2. Utan att använda LNP, som med stor sannolikhet orsakar systemiska biverkningar, kan detta vaccin tillåta upprepad dosering. Det är nu under utveckling för kliniska prövningar. Detaljerade forskningsresultat kommer att publiceras i Molecular Therapy .
Under covid-19-pandemin har mRNA-vacciner visat enastående effekt, med miljarder doser administrerade över hela världen. Utmaningar har dock uppstått mitt i deras snabba utveckling, i synnerhet när det gäller relativt starka biverkningar, inklusive allvarliga sådana, som fortfarande är viktiga problem.
Även om dessa biverkningar kan anses vara acceptabla för ett begränsat antal doser under en pandemi, är en säkrare plattform som tillåter flera doser under en livstid önskvärd för pågående covid-19-boosters och utvidgningen av mRNA-vaccintillämpningen till andra infektionssjukdomar. Nuvarande mRNA-vacciner har associerats med biverkningar, främst tillskrivna lipidnanopartiklar (LNP) som bär mRNA:t (mRNA inkapslat i en lipidbeläggning).
LNP har immunstimulerande egenskaper och kan spilla ut från injektionsstället, vilket leder till systemiska inflammatoriska svar. Icke desto mindre spelar LNP avgörande roller för vaccinets effektivitet, såsom att [Funktion I] förhindrar mRNA-nedbrytning och effektivt levererar mRNA till celler, [Funktion II] migrerar till lymfkörtlar för att leverera mRNA till immunceller och [Funktion III] stimulerar immunsystemet genom immunstimulerande lipider. Föreliggande studie syftar till att erhålla dessa funktioner utan att förlita sig på LNP.
Denna studie ger en enkel och säker design, administrering av naken mRNA. När det gäller [Funktion II] finns få immunceller i muskelvävnad, ett nuvarande administreringsställe för mRNA-vacciner. Därför var hudvävnaden, som är rikligare i immunceller, målinriktad.
Dessutom använde forskargruppen för [Funktion I] en Jet Injector som underlättar mRNA-leverans till hudcellerna med hjälp av fysisk stress inducerad av jetflöde. I en reporterstudie förbättrade Jet Injector mRNA-leveranseffektiviteten med mer än 100 gånger jämfört med en konventionell injektion med nål och spruta. Dessutom stannade mRNA på injektionsstället utan detekterbart systemiskt läckage.

Å andra sidan migrerade mRNA-laddade LNP:er (mRNA inkapslade i en lipidbeläggning) till levern, mjälten och andra systemiska organ efter intradermal administrering, vilket provocerade inflammationer där. Dessutom var inflammation på injektionsstället mycket liten i vår metod, medan mRNA inkapslat i en lipidbeläggning inducerade infiltration av inflammatoriska celler och vävnadsnekros.
Därefter visade forskargruppen först vaccinationsförmågan hos naket mRNA med hjälp av ett modellantigen. Jetinjektorn förbättrade drastiskt effektiviteten av antikroppsproduktion till en nivå som var jämförbar med den för mRNA inkapslat i en lipidbeläggning vid maximalt tolererbara doser.
Dessa antikroppar bekämpar virus i kroppen och förhindrar infektion, men de kan inte ta bort infekterade celler. Å andra sidan tar cellulär immunitet bort sådana sjuka celler, vilket spelar en avgörande roll för att förebygga allvarliga sjukdomar. Spännande nog ökar det nakna mRNA-vaccinet effektivt antalet immunocyter, såsom CD4-positiva T-celler och CD8-positiva T-celler.
Sedan genomförde forskargruppen virusutmaningsexperiment efter den nakna mRNA-vaccinationen riktad mot spikproteinet från SARS-CoV-2-viruset. Vaccinationen sänkte signifikant mängden virus i lungorna och lindrade lunginflammation jämfört med en ovaccinerad kontroll. Detta vaccin gav cynomolgusapor en vaccineffektivitet som var jämförbar med den för möss utan signifikanta biverkningar.
Den föreliggande studien omfattar även mekanistiska analyser. När det gäller [Funktion II] stannade det nakna mRNA-vaccinet på injektionsstället och migrerade inte till lymfkörtlarna. Å andra sidan migrerade antigenpresenterande celler som tog upp mRNA vid injektionsstället till lymfkörtlarna, vilket kan bidra till vaccinationseffektiviteten.
I själva verket inducerade vaccinet mognaden av lymfkörteln nära injektionsstället. För [Funktion III] orsakade Jet Injector övergående inflammation lokaliserad till injektionsstället och rekryterade lymfocyter. Nål- och sprutinjektion av naket mRNA inducerade inte ett sådant inflammatoriskt svar. Dessa resultat tyder på att immunstimuleringen av Jet Injector kan fungera som ett fysiskt adjuvans för att förbättra vaccinationseffektiviteten. Observerade lokala inflammatoriska reaktioner försvann inom några dagar.
Sammanfattningsvis minskar det nakna mRNA-vaccinet systemiska biverkningar, ett problem med mRNA inkapslat i en lipidbeläggning, och inducerar immunitet som är tillräcklig för att skydda mot infektionssjukdomar. Detta är en världsledande prestation för att förebygga infektionssjukdomar med enbart mRNA. Praktiskt taget kan detta vaccin bli en plattform som tillåter upprepad dosering med mindre biverkningar. För närvarande genomförs ytterligare studier, med målet att en klinisk prövning planeras till 2026.
Mer information: Saed Abbasi et al, Bärarfritt mRNA-vaccin inducerar robust immunitet mot SARS CoV-2 hos möss och icke-mänskliga primater utan systemisk reaktogenicitet, Molecular Therapy (2024). DOI:10.1016/j.ymthe.2024.03.022
Journalinformation: Molekylär terapi
Tillhandahålls av Innovation Center of NanoMedicine