Fluorescensstyrda interventionsstrategier kan förbättra standardterapier för att upptäcka och behandla mikroskopiska tumörer för att därigenom förhindra dödligt återfall. Cancerbiologer har gjort enorma framsteg inom fotoimmunoterapi och nanoteknik för att behandla metastaser, även om effekterna av sådana tekniker begränsas av heterogena effekter.
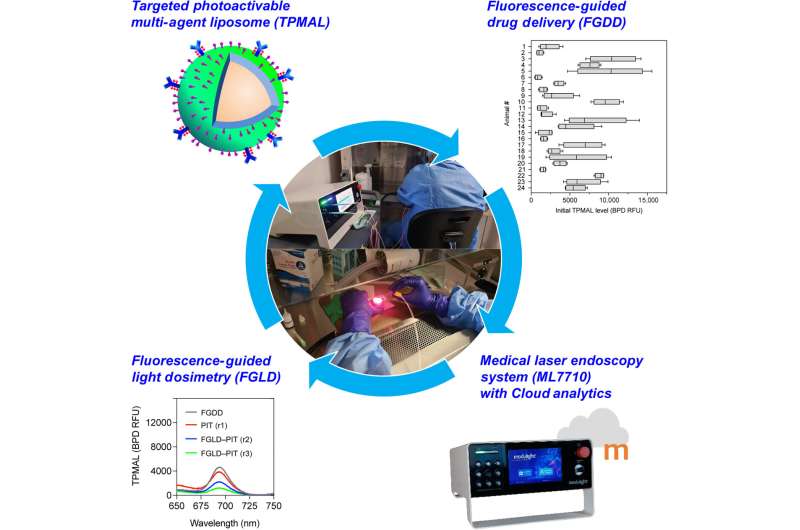
I en ny rapport publicerad i Science Advances , Barry J. Liang, och ett team av forskare inom bioteknik, cellbiologi och fotomedicin vid University of Maryland, Baltimore, Harvard Medical School U.S. och Modulight Corporation, Finland, integrerade tre tekniska framsteg för fluorescensstyrd intervention i riktade foto- aktiverbar multiagent liposomlaserendoskopi för förbättrad fotoimmunterapi.
Den fotoaktiverbara multiagensliposomen innehöll en nanoliposom märkt med fluoroforer för att spåra och fotosensibilisera immunkonjugat för fotoimmunterapi. Forskarna genomförde fluorescensstyrd läkemedelstillförsel under experimenten och fluorescensstyrd ljusdosimetri för att undersöka peritoneal karcinomatos i musmodeller.
Fluorescensstyrda läkemedelstillförselmetoder avslöjade att den riktade fotoaktiverbara multiagensliposomen förbättrade läkemedelsleveransen till metastaser ökade med 14 gånger. Teamet kombinerade interventionsmetoderna för att variera behandlingssvaret för tumörkontroll utan biverkningar.
Peritoneal metastasering eller ofullständig resektion och läkemedelsresistens kan göra avancerad äggstockscancer praktiskt taget obotlig med de befintliga metoderna inom kirurgi och kemoterapi. Även om tumörrecidiv är nästan universell, har femårsöverlevnaden på 30 % inte förändrats nämnvärt under de senaste tre decennierna.
Vid diagnos är upp till 70 % av dessa patienter i avancerade stadier. Den primära mekanismen för serös karcinommetastas involverar höggradig avsättning av många cancerknölar i hela bukhålan. Kvinnor med avancerad äggstockscancer som genomgår operation och kemoterapi har uppnått fullständig remission, även om patienterna återfaller på grund av kvarvarande sub-mm lesioner.
Även om sådana aggregat är svåra att upptäcka, kan de utveckla resistens mot standardbehandlingar, därför bör radikala tillvägagångssätt som kombinerar målinriktad terapi, avbildning och övervakning ta itu med läkemedelsresistenta mikrometastaser.
Även om intraoperativ fotodynamisk terapi för peritoneal karcinomatos med användning av icke-riktade fotosensibilisatorer och en fixerad ljusdoskombination är säker för klinisk användning, har teknologin ännu inte uppnått fullständiga svar eller långvarig tumörkontroll på grund av tumörheterogenitet och brist på specificitet under upptaget av fotosensibilisator.
I detta arbete använde Liang och kollegor riktade fotoaktiverbara multiagentliposomer (TPMAL) för fotokemoterapi konstruerade med molekylär inriktning och fluorescensspårningsfunktioner. Forskarna integrerade ett laserendoskopisystem för att främja ett tvådelat tillvägagångssätt för att säkerställa TPMAL-assisterad fotodynamisk terapi för säker och skräddarsydd läkemedelsleverans. Resultaten belyser effektiviteten och säkerheten hos fotoimmunterapi för att minska metastaserande börda in vivo.
Aktivera fotoimmunterapi i labbet
För att aktivera fotoimmunoterapi fäste forskarna kovalent fem fotosensibiliserande molekyler av bensoporfyrinderivat till varje monoklonal antikropp mot epidermal tillväxtfaktorreceptor genom karbodiimidkemi. Med hjälp av klickkemi kopplade de fotoimmunterapi kovalent till nanoliposomerna för att syntetisera riktade fotoaktiverbara flerskiktsliposomer.
De resulterande fotosensibilisatorerna immunkonjugat-nanoliposomer-karboxifluoresceinföreningar (förkortat PIC-Nal-CF) visade en genomsnittlig storlek i nanoskalaområdet med en lagringskapacitet på upp till 18 veckor. Genom att konjugera föreningen ändrade Liang och kollegor inte absorptionen av emissionsspektra av bensoporfyrinderivat och karboxifluorescein. De noterade en starkare fluorescerande signal vid 700 nm från konjugaten och noterade att materialets aktivitet var mer än fem gånger större än de fria elementen.
Liang och kollegor använde intralipid; ett ljusspridande medel på kliniken för intraperitoneal fotodynamisk terapi av peritoneal karcinomatos. De undersökte intralipidförändringar och fluorescensemissionsspektra för fotoimmunoterapikonjugaten (PIC-Nal-CF).
Med hjälp av 0,03 % bläck som ljusabsorberande medel studerade de den grumliga miljön av peritoneal karcinomatos, där tumörens serosanguinösa vätska reducerade fluorescenssignalen från karboxifluoresceinet till bensoporfyrin, medan intralipid hjälpte till med fluorescensövervakningen av föreningen.
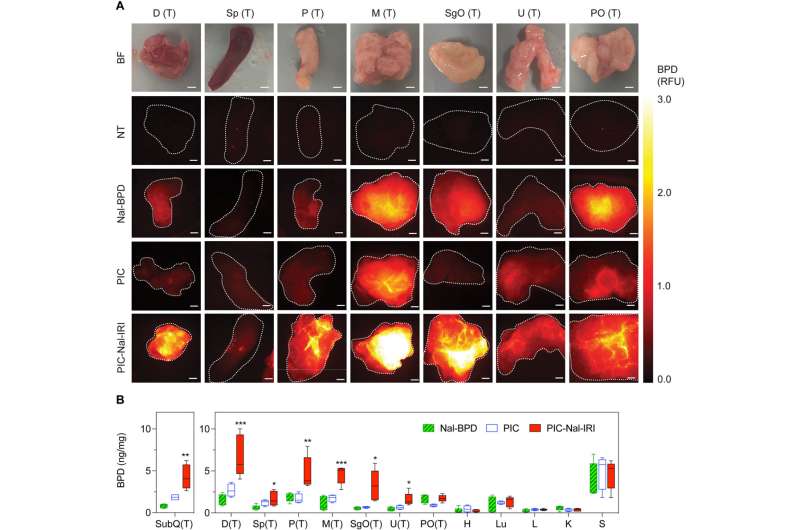
Teamet studerade biodistributionen av fotosensibiliserande immunkonjugat-nanoliposom-karboxifluoresceinföreningar i en musmodell av sjukdom och upptäckte föreningen i bukhålan hos möss för att framhäva förbättrad tumörselektivitet och retentionskapacitet.
Teamet bedömde biodistributionen av den theranostic föreningen genom att spåra fluorescenssignaler för att indikera deras förmåga att "låsa in" och "samleverera" genom att utforma läkemedelsförhållanden till målplatser. Jämfört med normala vävnader observerade de en ökad ackumulering av föreningen i metastaserande tumörer och noterade höga nivåer av bensoporfyrinackumulering i tumörvävnader efter injicering av föreningen av intresse.
Fotoimmunterapi begränsas vanligtvis av ett dåligt upptag av fotosensibilisator av tumörceller. Teamet studerade om fotosensibilisatorn och nanoliposomerna med irinotekan (PIC-Nal-IRI) kunde förbättra leveransen av enbart bensoporfyrinimmunkonjugat.
Efter 24 timmars intraperitoneal injektion uppvisade djuren som behandlats med konjugaten den högsta ackumuleringen av bensoporfyrinfluorescenssignal i tumörregionerna med låga signaler i alla friska vävnader. Läkemedelskonjugaten visade de högsta förhållandena mellan tumör och normal vävnad. Teamet studerade också intraoperativ fluorescensstyrd läkemedelstillförsel i olika djurmodeller.
På detta sätt undersökte Liang och kollegor användningen av fotodynamisk terapi som en lovande behandlingsstrategi för peritoneal karcinomatos. Ovariecancer är en dödlig gynekologisk malignitet i USA, med en femårig överlevnadsgrad av sjukdomen i stadium 1 på 92 %, men med en diagnos på 75 % av patienter i avancerade stadier och begränsade behandlingsalternativ för att påverka den totala överlevnaden.
Fotodynamisk terapi erbjuder en lovande behandlingsstrategi för peritoneal karcinomatos. Fotoimmunterapi är en riktad version av den process som introducerades 1983 för att förbättra tumörselektiviteten på komplexa ställen som bukhålan.
Metoden kan producera cytotoxiska reaktiva syrearter för att döda cancerceller och aktivera lokala och systemiska antitumörimmunsvar under lämpliga doser av ljus och fotosensibilisator.
De cancerriktade fotoaktiverade multiagensliposomer som utvecklats i detta arbete kan samlevereras med ljuskänsliga immunkonjugat och karboxifluoresceinfärgämnen eller irinotekankemoterapi för att utforska dynamiken i en ideal cancerbehandlingsstrategi för läkemedelstillförsel och behandling genom att ge insikter om de underliggande mekanismerna för antitumörimmun svar på fotoimmunoterapiföreningar.
Mer information: Barry J. Liang et al, Fluorescensstyrd fotoimmunterapi med riktad nanoteknologi och ML7710 för att hantera peritoneal karcinomatos, Science Advances (2023). DOI:10.1126/sciadv.adi3441
Willemien J. van Driel et al, Hyperthermic Intraperitoneal Chemotherapy in Ovarian Cancer, New England Journal of Medicine (2018). DOI:10.1056/NEJMoa1708618
Journalinformation: New England Journal of Medicine , Vetenskapens framsteg
© 2023 Science X Network