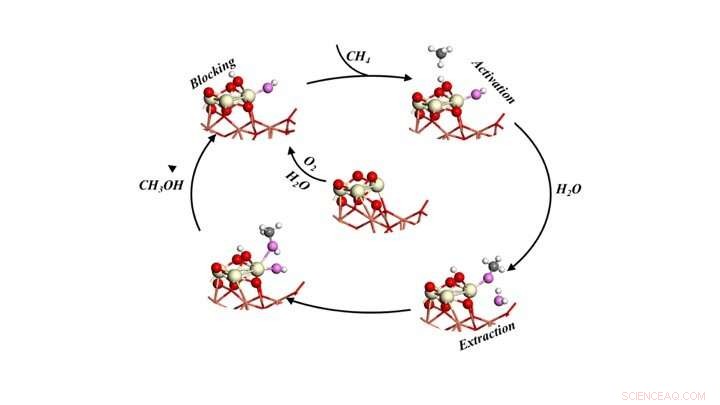
Katalytisk cykel för selektiv omvandling av metan till metanol genom att exponera metanen för syre och vatten. Kredit:Brookhaven National Laboratory
Forskare vid det amerikanska energidepartementets Brookhaven National Laboratory och medarbetare har avslöjat nya detaljer som förklarar hur en mycket selektiv katalysator omvandlar metan, huvudkomponenten i naturgas, till metanol, ett lätttransporterat flytande bränsle och råmaterial för tillverkning av plast, målar, och andra råvaror. Resultaten kan hjälpa till med utformningen av ännu mer effektiva/selektiva katalysatorer för att göra metanomvandling till ett ekonomiskt lönsamt och miljömässigt attraktivt alternativ till att ventilera eller fackla "avfallsgas".
Som beskrivs i en tidning som visas i Vetenskap , teamet använde teoribaserade modeller och simuleringar för att identifiera de omorganiseringar på atomnivå som äger rum under reaktionen, och genomförde sedan experiment för att verifiera dessa detaljer. Studierna avslöjade tre viktiga roller för vatten, arbetar i kombination med en ekonomisk ceriumoxid/kopparoxidkatalysator, att åstadkomma omvandling av metan till metanol med 70 procents selektivitet samtidigt som oönskade sidoreaktioner blockeras.
"Vi visste från tidigare arbete att vi hade utvecklat en mycket selektiv katalysator för direkt omvandling av metan till metanol i närvaro av vatten, " sa Brookhaven Lab-kemist Sanjaya Senanayake, som ledde projektet. "Men nu, använda avancerade teoretiska och experimentella tekniker, vi har lärt oss varför det fungerar så bra."
Fynden kan påskynda utvecklingen av katalysatorer som använder metan som läcker ut från gas- och oljekällor, där det vanligtvis ventileras direkt ut i atmosfären eller bränns av.
"Att transportera gas är extremt svårt och potentiellt farligt, ", sa Senanayake. "Men om du omvandlar den direkt till en vätska kan du flytta den och använda den istället för att slösa bort den. Även om kommersialiseringspotentialen för en sådan reaktion fortfarande kan ta flera år, vi hoppas att våra resultat och förståelsen för hur det hela fungerar kommer att hjälpa oss att nå dit snabbare."
Teori lägger grunden
Sökandet efter metan-till-metanol-katalysatorer har visat på några lovande utsikter. Men många arbetar i flera distinkta steg med höga energikrav. Och i många fall, konkurrerande reaktioner bryter ned metanet (och eventuell metanol som produceras) fullständigt till kolmonoxid (CO) och CO2. Så, när Brookhaven-teamet först observerade att deras katalysator direkt kunde omvandla metan till metanol med högt utbyte i en kontinuerlig reaktion, de ville veta mer om hur den utförde denna svåra uppgift.
De var särskilt intresserade av att ta reda på vattnets roll, som verkade underlätta nyckelsteg i processen och på något sätt blockera reaktionsvägarna som producerade CO och CO2.
Med hjälp av beräkningsverktyg i Brookhaven Labs Center for Functional Nanomaterials (CFN), Brookhavens Scientific Data and Computing Center, Stony Brook University (SBU), och National Energy Research Scientific Computing Center (NERSC) vid DOE:s Lawrence Berkeley National Laboratory (Berkeley Lab), Brookhaven-kemisten Ping Liu utvecklade det teoretiska tillvägagångssättet för att ta reda på vad som pågick.
Först, hon använde "density functional theory" (DFT) beräkningar för att identifiera hur reaktanterna (metan, syre, och vatten) förändrades när de interagerade med varandra och ceriumoxid/kopparoxid-katalysatorn i olika steg under reaktionen. Dessa beräkningar inkluderade också information om hur mycket energi det skulle ta att ta sig från ett atomarrangemang till nästa.
"DFT ger dig ett gäng "ögonblicksbilder" av stadierna som är involverade i reaktionen och de "stötar" eller barriärer du måste övervinna för att ta dig från ett stadium till nästa, " hon förklarade.
Sedan utförde hon "kinetiska Monte Carlo"-simuleringar - huvudsakligen med hjälp av datorer för att prova alla möjliga sätt som reaktionen kunde fortsätta från ögonblicksbild till ögonblicksbild. Simuleringarna tar hänsyn till alla möjliga vägar och energibehov för att gå från ett steg till nästa.
"Dessa simuleringar börjar med varje mellanstadium och tittar på alla möjligheter som kan gå till nästa steg - och ta reda på vad som är den mest troliga vägen, "Simuleringarna avgör det mest sannolika sättet att ögonblicksbilderna kan kopplas ihop i realtid."
Simuleringarna modellerar också hur olika reaktionsförhållanden, t.ex. förändringar i tryck och temperatur – kommer att påverka reaktionshastigheter och de troliga vägarna.
"Det fanns 45-50 möjliga komponenter i "reaktionsnätverket" som vi simulerade, sa Jose Rodriguez, en ledare för Brookhavens katalysgrupp som också har ett gemensamt uppdrag på SBU. "Av dem, Ping, Erwei Huang, och Wenjie Liao, två Ph.D. studenter vid SBU, kunde förutsäga vilka som skulle vara de mest gynnsamma förhållandena, den bästa vägen, för att gå från metan till metanol och inte till CO och CO2 - och allt inducerat av närvaron av vatten."
Modellerna förutspådde tre roller för vatten:1) aktivera metanet (CH4) genom att bryta en kol-vätebindning och tillhandahålla en -OH-grupp för att omvandla CH3-fragmentet till metanol, 2) blockera reaktiva platser som potentiellt skulle kunna omvandla metan och metanol till CO och CO2, och 3) underlättar undanträngningen av metanol som bildas på ytan till gasfasen som en produkt.
"All handling äger rum på en eller två aktiva platser i gränsytan mellan ceriumoxidnanopartiklarna och kopparoxidfilmen som utgör vår katalysator, sa Senanayake.
Men denna beskrivning var fortfarande bara en modell. Forskarna behövde bevis.

Brookhaven Lab och Stony Brook University (SBU) medlemmar av forskargruppen. Första raden, vänster till höger:Sanjaya Senanayake (Brookhaven), Mausumi Mahapatra (Brookhaven), Jose A Rodriguez (Brookhaven), Ping Liu (Brookhaven) och Wenjie Liao (SBU). Andra raden:Ivan Orozco (SBU), Ning Rui (Brookhaven), Zongyuan Liu (Brookhaven) och Erwei Huang (SBU). Kredit:Brookhaven National Laboratory
Experiment ger bevis
För att samla bevis, forskarna från Brookhaven och SBU genomförde ytterligare experiment i Brookhavens Chemistry Divisions laboratorier och tog flera resor till Advanced Light Source (ALS) vid Berkeley Lab. I detta team ingick SBU Ph.D. studenten Ivan Orozco och postdoktorala Zongyuan Liu, Robert M. Palomino, Ning Rui, och Mausumi Mahapatra.
På ALS, gruppen arbetade med Berkeley Labs Slavomir Nemsak och medarbetare Thomas Duchon (Peter-Grünberg-Institut i Tyskland) och David Grinter (Diamond Light Source i Storbritannien) för att utföra experiment med användning av omgivande tryck (AP) röntgenfotoelektronspektroskopi (XPS) , vilket gjorde det möjligt för dem att spåra reaktionen när den skedde i realtid för att identifiera nyckelsteg och intermediärer.
"Röntgenstrålningen exciterar elektroner, och elektronernas energi talar om för dig vilka kemiska arter du har på ytan och artens kemiska tillstånd. Det gör ett "kemiskt fingeravtryck." sa Rodriguez. "Med den här tekniken, du kan följa ytkemin och reaktionsmekanismen i realtid."
Att köra reaktionen med och utan vatten under en rad betingelser bekräftade att vatten spelade de tre förutsagda rollerna. Mätningarna visade hur reaktionsförhållandena förde processen framåt och maximerade produktionen av metanol genom att förhindra sidoreaktioner.
"Vi hittade direkta bevis för bildning av CH3O - en mellanliggande prekursor för metanol - i närvaro av vatten, " sa Rodriguez. "Och eftersom du har vattnet, du modifierar all ytkemi för att blockera sidoreaktionerna, och släpper även enkelt metanolen från katalysatorytan så att den inte sönderdelas."
"Nu när vi har identifierat designprinciperna för katalysatorn, " Senanayake sa, "Närnäst måste vi bygga ett riktigt system för att använda en sådan katalysator och testa det - och se om vi kan göra det bättre."