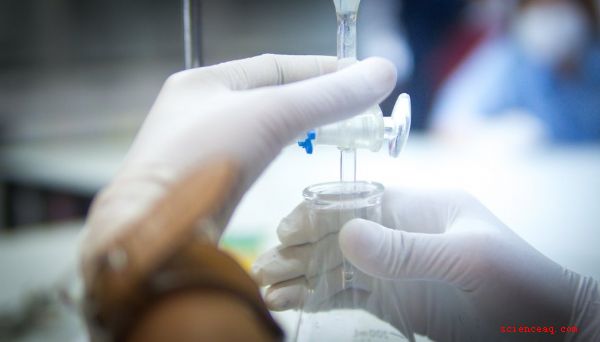
I kemi är titrering en process genom vilken en kemist kan hitta koncentrationen av en lösning med god noggrannhet, om hon vet vilken substans som finns i den. Detta kan vara mycket praktiskt för att bestämma koncentrationerna av syror och baser, såsom saltsyra och natriumhydroxid. Vanligtvis lägger kemisten till en andra lösning, droppe för droppe, tills blandningen plötsligt ändrar färg, vilket signalerar slutet på titreringen.
Grundläggande process
Lösningen med okänd koncentration kallas "titer." "titranten." Vid syrabas-titrering läggs tillräckligt med titrant till titern för att neutralisera den. Så om titer är en bas, lägger en kemist till en syra som titer.
En labbtekniker lägger till en färgindikator till titer innan den indikerar neutraliseringspunkten. Detta är viktigt eftersom om han lägger till titranten för snabbt kan teknikern gå rätt vid neutraliseringspunkten och inte veta exakt hur mycket titrant som behövdes för att nå den.
Indikatorer
Vid syrabas-titrering, neutraliseringspunkten sker vid ett pH av 7,0. Litmus är en bra indikator för en syrabas-titrering, eftersom den ändrar färg vid ett pH på cirka 6,5 - tillräckligt nära, vilket kommer att förklaras nedan. Eftersom indikatorer reagerar med den uppmätta lösningen, bör de användas i moderation - endast några droppar om möjligt.
Equivalence Point |
Den punkt där titranten neutraliserar hela titern och lämnar neutralt vatten, kallas ”ekvivalenspunkten.” Detta är när titranten har ”använt” hela titern. Syran och basen har helt annullerat varandra. Ett exempel på denna typ av ömsesidig annullering illustreras i denna kemiska formel:
HCl + NaOH -> NaCL + H 2O Vid jämvikt är lösningens pH 7,0. Om du använder en pH-mätare kan du registrera pH regelbundet när titranten läggs till. Ett diagram över pH-värdet (som den vertikala axeln) mot titreringsvolymen skulle ge en sluttande kurva som är särskilt brant runt ekvivalenspunkten. PH är ett mått på H3O + -koncentrationen i en lösning. Att lägga till en eller två droppar till en neutral lösning förändrar kraftigt H3O + -koncentrationen, med en faktor 10 eller mer. Fördubbling av det tillagda beloppet förändrar inte koncentrationen nästan lika mycket. Det är detta som gör titreringskurvan så brant i den ena regionen, och därför gör ekvivalenspunkten så lätt att identifiera i diagrammet. Mängden titrering som behövs för att neutralisera titern är därför lätt att kvantifiera. En titreringskurva kan också kurva konduktivitet (som den vertikala axeln) mot titranten. Syror och baser leder elektricitet. Därför kan du mäta konduktivitet genom att sätta in elektroder i titer. Elektroderna skulle vara anslutna till ett batteri och ammeter (eller voltmeter). Titreringskurvan kommer att förändras utfällbart vid ekvivalenspunkten. I detta fall kommer konduktiviteten att ha ett märkbart minimum vid ekvivalenspunkten. Denna metod har fördelen av att det inte behövs en indikator som kan störa eller delta i neutraliseringsreaktionen och påverka dess resultat.
Titration Curve
Potentiometrisk titrering