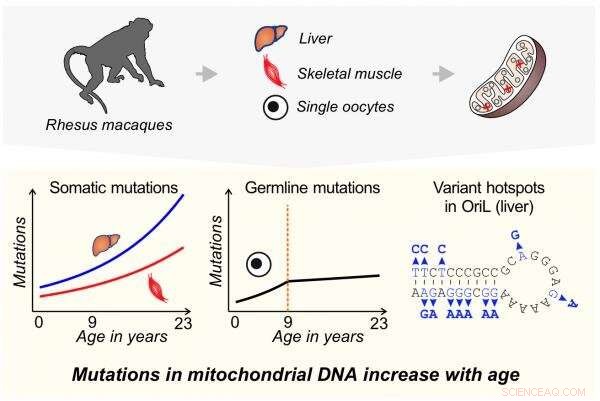
En ny studie visar att mutationsfrekvenser i mitokondrie-DNA är lägre, och ökar mindre med åldern, i prekursorerna till äggceller än i cellerna i andra vävnader hos en primat. Mitokondrie-DNA sekvenserades i prover av lever, skelettmuskler och enstaka oocyter från 1- till 23-åriga rhesusmakaker. Nya mutationer ökade med åldern snabbast i lever och långsammast i oocyter. Mutationsfrekvensen i oocyter ökade endast fram till 9 års ålder. Ljussträngsreplikationsursprunget (OriL), regionen som är ansvarig för att kopiera mitokondriella genomen, visade sig vara en hotspot för mutationsackumulering med åldrande i levern. Kredit:Barbara Arbeithuber
Nya mutationer inträffar i ökande takt i mitokondriella genomen hos utvecklande äggceller hos åldrande rhesusapor, men ökningarna verkar platåga vid en viss ålder och är inte lika stora som de som ses i icke-reproduktiva celler, som muskler och lever. En ny studie som använder otroligt noggrann DNA-sekvenseringsmetoder tyder på att det kan finnas en skyddsmekanism som håller mutationshastigheten i reproduktionsceller relativt lägre jämfört med andra vävnader hos primater, ett faktum som kan relateras till primatens – och därmed människans – benägenhet att föröka sig vid senare åldrar.
"På grund av de sjukdomar hos människor som orsakas av mutationer i mitokondriernas genom och trenden i moderna mänskliga samhällen att skaffa barn i högre åldrar, är det viktigt att förstå hur mutationer ackumuleras med åldern", säger Kateryna Makova, Verne M. Willamans ordförande för Life. Sciences at Penn State och ledare för forskargruppen.
"Mitt labb har varit intresserad av att studera mutationer – inklusive mutationer i mitokondriellt DNA – under lång tid. Vi är också intresserade av evolution, så vi ville se hur mutationer i mitokondriellt DNA ackumuleras i fortplantningsceller eftersom dessa mutationer kan överföras till nästa generation." En artikel som beskriver studien, ledd av forskare vid Penn State, dyker upp online veckan den 4 april 2022 i The Proceedings of the National Academy of Sciences .
Mitokondrier är cellulära organeller – ofta kallade cellens kraftpaket på grund av sin roll i energiproduktionen – som har ett eget genom skilt från cellens "kärngenom", som finns i kärnan och är vad vi ofta tänker på som "genomet". Mutationer i mitokondrie-DNA bidrar till flera mänskliga sjukdomar, men att studera nya mutationer är utmanande eftersom verkliga mutationer är svåra att skilja från sekvenseringsfel, som inträffar i en högre takt jämfört med mutationshastigheten för de flesta sekvenseringstekniker.
"För att övervinna denna svårighet använde vi en metod som kallas "duplexsekvensering", säger Barbara Arbeithuber, en postdoktor vid Penn State vid tidpunkten för forskningen som nu är forskargruppledare vid Johannes Kepler University Linz i Österrike. "DNA består av två komplementära strängar, men de flesta sekvenseringstekniker tittar bara på sekvenserna från en av strängarna åt gången. Vid duplexsekvensering bygger vi konsensussekvenser för varje sträng individuellt och jämför sedan de två. Fel är extremt osannolikt att händer på samma plats på båda strängarna, så när vi ser förändring på båda strängarna kan vi vara säkra på att det representerar en sann mutation."
Teamet sekvenserade mitokondriella genomet från muskelceller, leverceller och oocyter - prekursorceller i äggstocken som kan bli äggceller - i rhesusmakaker som varierade i ålder från 1 till 23 år. Detta åldersintervall täcker nästan hela apornas reproduktiva livslängd. Vävnader för studien samlades in opportunistiskt under loppet av flera år från primatforskningscentra när djur dog av naturliga orsaker eller offrades på grund av sjukdomar som inte var relaterade till reproduktion. Oocyter, och inte spermier, användes eftersom mitokondrier ärvs uteslutande genom moderlinjen.
Sammantaget såg forskarna en ökning av mutationsfrekvensen i alla testade vävnader när makakerna åldrades. Leverceller upplevde den mest dramatiska förändringen med en 3,5-faldig ökning av mutationsfrekvensen under cirka 20 år. Mutationsfrekvensen i muskler ökade 2,8 gånger under samma tidsperiod. The mutation frequency in oocytes increased by 2.5-fold up to age nine, at which point it remained steady.
"From a reproductive biology perspective, oocytes are really interesting and special cells," said Francisco Diaz, associate professor of reproductive biology at Penn State. "They are generated prior to birth and sit in the ovary for years and years and years, and then a few of them are activated each reproductive cycle. So, you would expect them to accumulate a lot of mutations over that time, but instead we see that they accumulate mutations for a while and then they do not. This seems to indicate that the germ line—reproductive cells like egg and sperm—may be more resilient than we thought."
In addition to changes in the rate of mutations over time, the research team also identified variation in mutation frequency across the mitochondrial genome, including several hotspots where mutations occurred much more frequently than you would expect by chance that varied by tissue. One of the hotspots was located in the region responsible for copying of mitochondrial genomes.
"Although it is very challenging to perform a study like this in humans, using a primate model species gives us a close approximation," said Makova. "Our results suggest that primate oocytes might have a mechanism to protect or repair their mitochondrial DNA, an adaptation that helps to allow later reproduction. The precise mechanism leading to the plateau in mutation frequency in oocytes remains enigmatic, but it might act at the level of elimination of defective mitochondria or oocytes."