Kredit:HIMS
Kemister vid University of Amsterdams Van 't Hoff Institute for Molecular Sciences har upptäckt en ny klass molekyler. Den här veckan rapporterar de in Naturkommunikation på deras syntesmetod som leder till "kvasi [1] catenanes":kringelliknande molekyler bestående av två molekylära ringar "motsatt" kopplade till en central kolatom. Upptäckten är ett viktigt steg mot syntes av lassopeptider; nya molekyler med potentiell användning som läkemedel.
Nature Communication-artikeln är kronan för en femårig forskningsinsats vid professor Jan van Maarseveens forskargrupp Synthetic Organic Chemistry, med doktoranden Luuk Stemers i spetsen. Han har utvecklat en metod som banar väg för syntes av så kallade lassopeptider.
Lassopeptider är små proteiner som, som deras namn indikerar, består av en molekylär 'loop' runt ett molekylärt 'rep'. De isolerades först från bakterier i början av det nuvarande seklet. Nyligen, DNA -analys har avslöjat att lassopeptider är ganska vanliga inom bakterier. Deras biologiska funktion är att fungera som ett antibiotikum mot andra mikroorganismer, vilket gör dem till en potentiell ny klass av antibiotika.
Det faktum att syntetiska kemister 15 år efter upptäckten av lasso-peptider ännu inte har kunnat utveckla en strategi som leder till deras unika molekylarkitektur understödjer komplexiteten hos dessa molekyler.
Flaskhalsen här är att repet vanligtvis är tätt bunden i öglan. Detta skiljer lassopeptider från rotaxaner för vilka skotska kemisten Sir Fraser Stoddart delade Nobelpriset för kemi förra året. Under rotaxansyntes "dras" repet genom öglan.
Eftersom detta är omöjligt för lassopeptidsyntes, Amsterdamkemisterna använde ett annat tillvägagångssätt, tvingar öglan att stänga på rätt plats runt repet. Detta visade sig vara ett ganska uppdrag. Så småningom lyckades Luuk Stemers skapa en molekylär byggnadsställning som hjälpte syntesen på ett sådant sätt att slingan bildas korrekt runt repet.
Den nya syntesmetoden är ett stort steg framåt på den syntetiska vägen mot funktionella lassopeptider. För att demonstrera kraften i metoden använde Stemers sitt ställning för att även tvinga repets båda ändar att bilda en andra slinga.
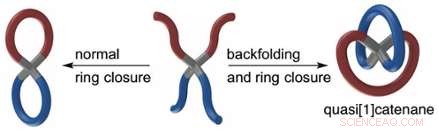
Detta resulterade i syntesen av en helt ny klass av kringelliknande molekyler som Amsterdamforskarna myntade quasi [1] catenanes. ("Riktiga" catenaner består av två löst sammanflätade molekylära ringliknande strukturer. Den franska kemisten Jean-Pierre Sauvage utvecklade catenaner och delade Nobelpriset med Stoddard, och den nederländska kemisten Ben Feringa.)
Nästa steg i Amsterdam -forskarnas forskningsinsats mot lassopeptidsyntes blir att införa lätt brytbara bindningar i kvasi [1] catenane, så att ringarna kan låsas upp.