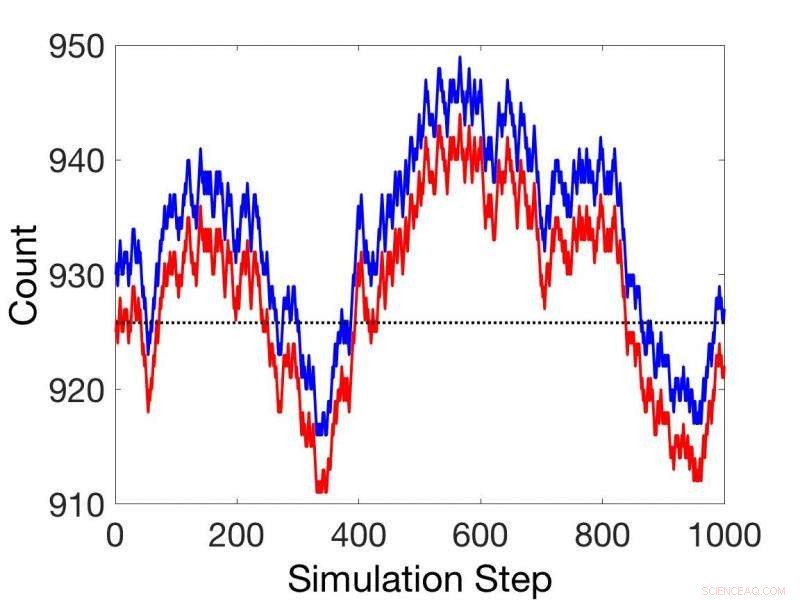
Jämförelser mellan stokastiska kinetiska simuleringar i icke-steady state (röd) och simuleringar med hjälp av kopplad reaktionssats (blå). Kredit:Pacific Northwest National Laboratory
Massaktionslagen beskrevs första gången för 150 år sedan. I dag, det är fortfarande ett basbegrepp i varje förstaårs kemitext. Lagen säger att hastigheten för en kemisk reaktion är proportionell mot koncentrationen av reaktanterna. För lösningar i dynamisk jämvikt, lagen förutsäger hur dessa lösningar kommer att bete sig.
Men det är en utmaning att tillämpa lagen om massaktion på komplexa system, såsom biologisk metabolism. För en, de flesta hastighetskonstanter är inte tillgängliga, och att mäta de saknade är mycket arbetskrävande.
Inom biologisk forskning, att mäta hastighetskonstanter kräver isolering och rening av enskilda enzymer, sedan bestämma hastighetskonstanterna med spektrofotometri - det vill säga, hur mycket ljus en kemikalie absorberar. Detta saktar ner genomströmningshastigheten, gör det svårt att karakterisera varje nytt genom. Trots allt, för att göra detta krävs tusentals hastighetsparametrar.
På grund av dessa problem, ett stort antal enzymhastighetsparametrar har bestämts för bara ett fåtal väl beskrivna system, såsom Escherichia coli. För de flesta biologiska system, forskare har ännu inte erhållit hastighetskonstanter.
Under tiden, den valda metoden för att modellera storskaliga biologiska processer (såsom metabolism) involverar begränsningsbaserade flödesmodeller. Men dessa modeller lider av brist på fysik när det gäller lagen om massaktion, begränsar förmågan hos begränsningsbaserade tillvägagångssätt även när de utvidgas till att omfatta termodynamik och andra faktorer.
Som svar, vissa forskare har föreslagit att studera elementära reaktioner med hjälp av massreaktionens lag genom reaktionsaffiniteter istället för hastighetskonstanter.
Ett nytt papper i journalen Fysisk biologi av William R. Cannon och Scott E. Baker vid Pacific Northwest National Laboratory granskar sambandet mellan reaktionsaffinitet och fri energi för isolerade reaktioner genom att använda begrepp från statistisk termodynamisk integration. Cannon och Baker bestämde sig för att explicit visa sambandet mellan kinetiska formuleringar av hastigheter som använder hastighetskonstanter och en statistisk termodynamisk formulering som använder kemiska potentialer.
Därefter presenterar de ett teorem för kopplade reaktioner baserat på kemiska potentialer, som kan ge relativa hastigheter för alla sekventiellt kopplade reaktioner under alla förhållanden, steady state eller inte. Detta undanröjer behovet av hastighetskonstanter i många tillämpningar.
Att använda kemiska potentialer istället för hastighetskonstanter representerar ett metodologiskt språng som författarna säger skulle kunna signalera ett stort framsteg för prediktiv modellering inom systembiologi.
Den nya metoden kommer att möjliggöra komplexa, storskaliga biologiska system som metabolism som ska modelleras med kinetik och termodynamik. Detta kommer att resultera i mer exakta förutsägelser för designen av mikroorganismer för att bete sig på önskade sätt, sådana som skulle kunna utnyttjas för att producera biobränslen.
Dessutom, författarna säger, den nya metoden kommer att ge grundläggande insikt i den termodynamiska kopplingen mellan levande organismer och deras miljö.