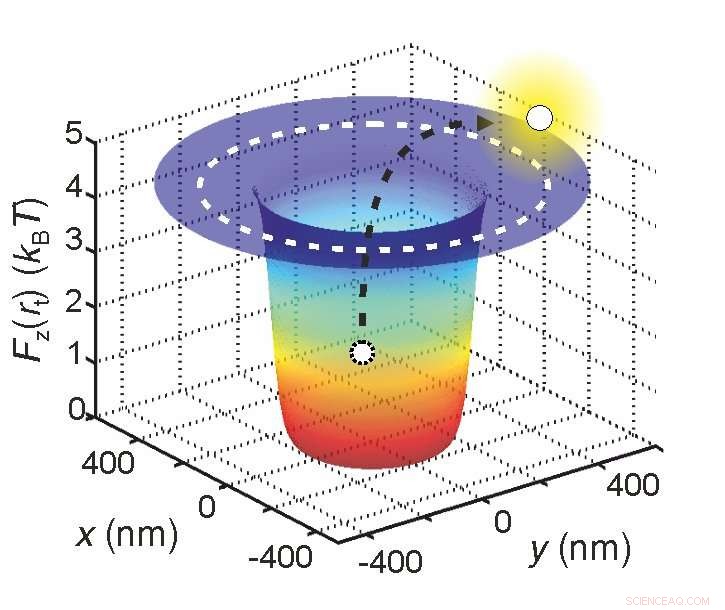
Forskare kan bestämma den effektiva elektriska laddningen av en molekyl genom att fånga den i en potentiell brunn genom att mäta hur länge den stannar inne. Upphovsman:Madhavi Krishnan / Zürichs universitet
För första gången, forskare har exakt mätt den effektiva elektriska laddningen av en enda molekyl i lösning. Denna grundläggande insikt från en SNSF -professor kan också bana väg för framtida medicinsk diagnostik.
Elektrisk laddning är en av nyckelegenskaperna som gör att molekyler kan interagera. Livet i sig beror på detta fenomen:många biologiska processer involverar interaktioner mellan molekyler som proteiner, där deras avgift spelar en väsentlig roll. Än, laddningen av ett protein i en vattenhaltig miljö - dess naturliga sammanhang i en levande organism - är svårt att avgöra exakt med hjälp av traditionella metoder.
Madhavi Krishnan, som innehar en SNSF -professur vid universitetet i Zürich, har utvecklat en metod för att exakt mäta laddningen av en enda molekyl i lösning. Hennes framsteg beskrevs i en serie artiklar i Naturnanoteknik , Fysisk granskning E och den Journal of Chemical Physics . Denna upptäckt kan bana väg för nya diagnostiska verktyg eftersom, på kemisk nivå, många sjukdomar är kopplade till en förändring av ett proteins elektriska laddning, vilket hindrar molekylen från att agera som den ska.
En molekyls elektriska laddning kan vara ganska annorlunda i gasfasen och i lösning. Anledningen till denna skillnad ligger i komplexa interaktioner mellan objektet och den omgivande vätskan. Därav, standard gasfasmätningar ger inte direkt information om molekylens beteende i dess biologiska sammanhang.
"Som barn sparkar en boll"
Molekyler i lösning är i konstant rörelse, slumpmässigt sparkar varandra. Krishnan och Ph.D. studenten Francesca Ruggeri utnyttjade detta välkända fenomen, kallade Brownian motion, för att mäta den effektiva laddningen av en molekyl direkt i lösning.
Först, de fångade molekylen i en "potentiell brunn". I stället för en verklig brunn, detta är en situation där molekylens potentiella energi är som lägst. I en sådan situation, studsande vattenmolekyler försöker kontinuerligt utvisa molekylen från brunnen.
"Det är som barn som leker med en boll i botten av en grop, "förklarar Krishnan." Bollen är molekylen vi är intresserade av, och barnen är vattenmolekylerna. Bollen måste få en ganska hård spark för att flyga ur gropen. "
Ju högre molekylens effektiva laddning, desto större djup av den potentiella brunnen och, följaktligen, desto lägre är sannolikheten för att molekylen matas ut från brunnen. I praktiken, detta innebär att den tid som krävs för att molekylen ska sparkas ut ur brunnen är direkt relaterad till dess effektiva laddning.
"I slutändan handlar det om en statistisk princip, "förklarar Krishnan." Om vi vet hur länge en molekyl förblir instängd i brunnen, vi vet exakt hur djup brunnen är. Och eftersom detta djup beror direkt på molekylens effektiva laddning, Vi kan också härleda detta värde mycket exakt. "
Två glasplattor
För att skapa en potentiell brunn, forskare komprimerade en lösning som innehåller proteinerna mellan två glasplattor, en av dem är täckt med mikroskopiska hål. Molekyler fångade i potentiella brunnar märktes med fluorescerande medel, vilket gjorde att de kunde spåras med ett optiskt mikroskop.
Även om upptäckten har viktiga grundläggande konsekvenser, det kan också bana väg mot nya diagnostiska verktyg för många sjukdomar orsakade av felformade proteiner, som Alzheimers och cancer. "Vi vet att 3D-konformationen av ett protein påverkar dess effektiva laddning, och vårt arbete kan presentera en ny väg för att upptäcka defekta proteiner. "