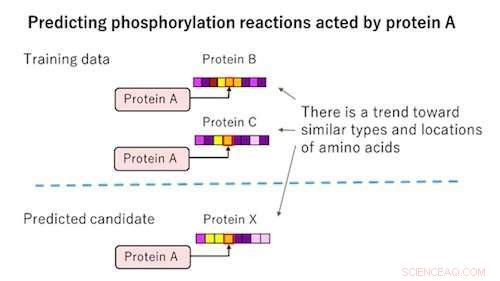
Figur 1:Konventionell AI -teknik. Upphovsman:Fujitsu
Fujitsu Laboratories Ltd., Insight Center for Data Analytics, en forskningsinstitution för dataanalys baserad i Irland, och Fujitsu (Ireland) Limited meddelade idag utvecklingen av en teknik som gör det möjligt att förutsäga stora mängder okända kemiska reaktioner, ungefär dubbelt så många som det konventionella förfarandet. Vid allvarliga sjukdomar, inklusive cancer, det är vanligt att det finns abnormiteter i fosforyleringsreaktioner, som är kemiska reaktioner som uppstår mellan proteiner. Följaktligen, det finns höga förväntningar på att förtydligande av fosforyleringsreaktioner leder till effektiva behandlingar. För närvarande, dock, eftersom endast ett fåtal fosforyleringsreaktioner har identifierats, det har varit ett problem att förutsäga stora mängder fosforyleringsreaktioner orsakade av kombinationer av okända proteiner. Nu, genom att bygga ett kunskapsdiagram som kan omfatta en översikt över sambandet mellan proteiner, det är möjligt att kontrollera sambandet mellan nya proteiner där fosforyleringsreaktioner kan förutsägas. På det här sättet, denna teknik kommer att bidra till medicinsk utveckling, eftersom det kan förväntas vara användbart i frontlinjerna för forskning kring läkemedelsupptäckt, och har anpassade applikationer inom precisionsmedicin.
Utvecklingsbakgrund
Biologiska system i kroppen upprätthålls genom utbyte av information genom de kemiska reaktionerna av olika proteiner i cellerna. Under de senaste åren har vetenskapen har förstått att många allvarliga sjukdomar, som cancer, orsakas delvis av abnormiteter i fosforyleringsreaktioner, som är representativa för de kemiska reaktionerna mellan proteiner. Om läkemedel som reparerade onormala fosforyleringsreaktioner kunde utvecklas, som skulle möjliggöra effektivare behandlingar. För närvarande, dock, endast ett fåtal fosforyleringsreaktioner är väl förstådda, så det finns ett behov av upptäckten av okända fosforyleringsreaktioner, och för att berika data om fosforyleringsreaktioner.
Frågor
Fosforyleringsreaktioner är kemiska reaktioner där ett protein fäster en fosforylgrupp till aminosyrorna som utgör ett annat protein. För att upptäcka dem, det är nödvändigt att kontrollera kombinationer av proteiner som orsakar fosforyleringsreaktioner genom biologiska experiment. Ändå, eftersom det finns mer än cirka 800, 000 möjliga kombinationer bara med proteiner, och eftersom betydande kostnader och tid krävs för biologiska experiment, det är nödvändigt att redan från början förutsäga kombinationer med hög sannolikhet. Det är känt att huruvida en fosforyleringsreaktion kommer att inträffa beror på strukturen hos aminosyrasekvensen som utgör proteinet. AI -teknik används därför redan för att förutsäga nya fosforyleringsreaktioner genom att träna AI i strukturen av aminosyrasekvenser som redan är kända för att orsaka fosforyleringsreaktioner. Även om denna teknik kan förutsäga reaktioner där strukturen för aminosyrasekvensen liknar de som är kända för att orsaka fosforyleringsreaktioner, den har inte kunnat förutsäga sådana i vilka strukturen för aminosyrasekvensen skiljer sig väsentligt från de redan kända fosforyleringsreaktionerna.
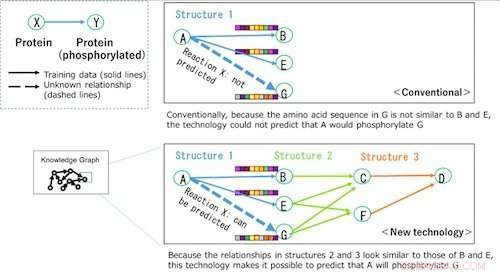
Figur 2:Exempel på att förutsäga fosforyleringsreaktioner med hjälp av kunskapsdiagram. Upphovsman:Fujitsu
Enligt färsk medicinsk forskning, det finns ett fenomen där proteiner som har genomgått reaktioner kan fosforylera andra proteiner i en kedjereaktion (kedjad information), och detta kan vara nyckeln till att förutsäga nytt, okända fosforyleringsreaktioner relaterade till det fenomenet. Baserat på sådan forskning, Fujitsu Laboratories, Insight Center, och Fujitsu Irland har nu inkluderat inte bara strukturell information om aminosyrasekvenser i kunskapsdiagrammet, men också kedjad information. Organisationerna har utvecklat en teknik (patentsökt) för att representera de komplexa mönstren för kemiska reaktioner som optimerade attribut, som är kopplade till raderna i kunskapsdiagrammet. Eftersom dessa attribut anpassades till den sofistikerade konstruktionen av kunskapsdiagrammet, de kan leda till mycket exakta förutsägelseresultat. Konventionellt, förhållandet mellan proteiner kunde endast kontrolleras genom en enda länk i kedjan. Men genom att fullständigt visa sambandet mellan proteiner som kopplingar av fosforyleringsreaktioner (kedjad information), det blir möjligt att klargöra placeringen av de olika proteinerna ur ett holistiskt perspektiv, och att förutsäga okända relationer.
Effekter
När denna teknik testades med hjälp av utvärderingsdata, modellen utbildades i fosforyleringsreaktioner (9, 802 reaktioner), och förutspådde 11, 581, 940 nya fosforyleringsreaktioner. Detta visade sin förmåga att förutsäga ungefär dubbelt så många fosforyleringsreaktioner jämfört med konventionell teknik som utbildade AI i strukturen för aminosyrasekvenser, utan väsentlig förändring av förutsägelsens noggrannhet. Dessutom, för att testa om fosforyleringsreaktioner som förutspås med denna teknik faktiskt kan uppstå inom ett levande väsen, tester utfördes av System Biology Ireland, en irländsk biologisk forskningsinstitution och en gemensam forskningspartner, med hjälp av masspektrometriutrustning och antikroppar. I detta test, experter på biologi valde ut och testade några fosforyleringsreaktionsprognosresultat för proteiner relaterade till cancer, och kunde bekräfta nio fosforyleringsreaktioner, varav åtta var reaktioner som inte hade kunnat förutses med konventionell teknik. Systembiologi Irland (SBI) chef Walter Kolch, en världsledande myndighet inom systembiologisk forskning, sade om dessa resultat "Kombinera Fujitsus kunskapsgrafologi med SBI:s förståelse av biologiska nätverk, Vi har utvecklat en ny beräkningsmetod som kan förutsäga vilka kinas som fosforylerar vilka substrat. Metoden är korrekt och kan upptäcka tidigare okända fosforyleringsplatser, ett stort steg framåt för utveckling av nya läkemedel och mer fokuserad precisionsmedicin. "
Genom att kombinera data om nya fosforyleringsreaktioner som förutses av denna teknik med andra biomedicinska data, det förväntas koppla de kemiska reaktionerna från orsakerna till en sjukdom (avvikelser i fosforyleringsreaktioner) till sjukdomens symptom, som sedan kan tillhandahållas till forskarna i frontlinjen som användbar information vid upptäckt av läkemedel. Effektiviteten av behandlingar för sjukdomar som cancer kan variera mycket mellan patienter. Denna teknik, dock, förväntas klargöra den individuella variationen i effekterna av behandlingar, bidra till marknadsföring av medicin som är skräddarsydd för enskilda patienter. Fujitsu Laboratories, Insight Center, och Fujitsu Irland kommer att fortsätta att förbättra noggrannheten hos denna teknik för att behandla biomedicinsk data med kunskapsgrafer, att utvidga tekniken till biomedicinska projekt vid Fujitsu Limited under budgetåret 2018. Dessutom har genom att införliva denna teknik i Fujitsus AI -teknik, inklusive Fujitsu Human Centric AI Zinrai, organisationerna planerar att påskynda den biomedicinska verksamheten.