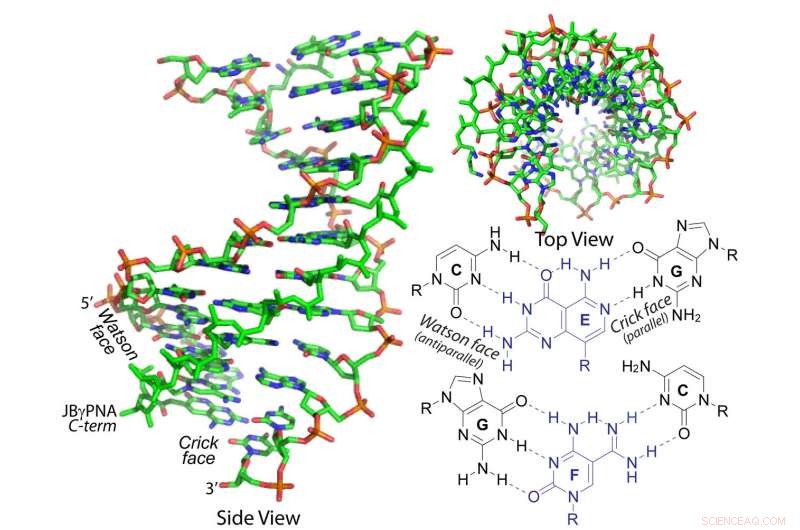
Utvecklad av forskare vid Carnegie Mellon University, denna janus gamma-peptidnukleinsyra (PNA) kan invadera dubbelhelixen av DNA och RNA. Kredit:Carnegie Mellon University
Forskare från Carnegie Mellon University har utvecklat en syntetisk molekyl som kan känna igen och binda till dubbelsträngat DNA eller RNA under normala fysiologiska förhållanden. Molekylen kan ge en ny plattform för att utveckla metoder för diagnos och behandling av genetiska tillstånd. Deras resultat publiceras i Kommunikationskemi .
Arbetet utfördes av ett internationellt team av experter, inklusive Carnegie Mellon professor i kemi Danith Ly, en expert på peptidnukleinsyradesign, kemi postdoc Shivaji Thadke och kemi doktorand Dinithi Perera, Kemiprofessor och kärna magnetisk resonans expert Roberto Gil, och Arnab Mukherjee, en datavetare vid Indian Institute of Science Education and Research i Pune.
"Eftersom den dubbelspiralformade strukturen av DNA först klargjordes av Watson och Crick, forskare har försökt designa molekyler som kan binda till DNA och låta en kontrollera flödet av genetisk information, " sa Ly. "Detta är den första bifaciala molekylen som kan invadera dubbelsträngat DNA eller RNA under biologiskt relevanta förhållanden."
DNA, som innehåller all genetisk information från en organism, består av två strängar av nukleotider. Nukleotiderna ansluter till varandra med hjälp av vätebindningar, bildar en spiralformad kedja av Watson-Crick baspar. Även om dessa baspar ger en relativt enkel kod till vår genetiska information, att komma in i dubbelhelixen för att ändra koden är svårt på grund av de starka bindningarna mellan basparen.
Ly och hans kollegor vid Carnegie Mellon University Institute for Biomolecular Design and Discovery (IBD) och Center for Nucleic Acids Science and Technology (CNAST) är ledande inom design och utveckling av gammapeptidnukleinsyror (gamma PNA). Syntetiska analoger till DNA och RNA, gamma -PNA kan programmeras att binda till det genetiska materialet (DNA eller RNA) som orsakar sjukdom, tillåta dem att söka efter skadliga sekvenser och binda till dem för att förhindra att en gen inte fungerar.
Gruppen har skapat dubbelsidiga gamma-PNA som kallas Janus gamma-PNA. Uppkallad efter den romerska guden med två ansikten, Janus PNAs kan känna igen och binda med båda strängarna av en DNA- eller RNA-molekyl.
Begreppet bifacial igenkänning, som är grunden för Janus gamma PNA, skapades först för mer än två decennier sedan av Jean-Marie Lehn, en nobelpristagare känd för sitt arbete inom supramolekylär kemi, och förklaras av andra forskare inom området.
Framgången för denna forskning har hållits tillbaka av två hinder. Först, forskare hade bara kunnat göra ett litet antal Janus -baser, och dessa baser varierade avsevärt i form och storlek. Dessa begränsningar innebar att de olika Janus-baserna bara kunde känna igen upprepningar av samma uppsättning baspar och inte kunde användas tillsammans som byggstenar för att känna igen mer komplexa sekvenser i DNA eller RNA.
För det andra, det var svårt att syntetisera Janus -baser för kanoniska baspar. Den komplementära naturen hos de två sidorna av Janus-baserna gjorde att molekylerna hybridiserade och binder till varandra, hindrar dem från att införlivas i DNA och RNA.
I den aktuella studien, Ly och kollegor övervinner dessa hinder. De skapade en helt ny uppsättning bifaciala nukleinsyraigenkänningselement, 16 totalt, som stod för varje möjlig kombination av nukleobaser som kunde finnas i den genetiska koden. Janus gamma PNA kan användas för att känna igen vilken kombination av baspar som helst och blandas och matchas för att detektera och binda till komplexa genetiska sekvenser.
Thadke löste det kemiska syntesproblemet genom att ta fram en ny lösnings- och fastfassyntesmetod för att utveckla Janus gamma PNA. Han använde också ett knep inneboende i den spiralformade förorganisationen i ryggraden i gamma-PNA för att förhindra självkomplementära Janus-baser från att hybridisera till varandra.
Dessa nya Janus gamma PNA har en utomordentligt hög bindningsenergi och är de första som kan invadera en kanonisk basparad DNA eller RNA dubbelhelix vid en fysiologiskt relevant jonstyrka och temperatur.
De gör detta genom att dra nytta av när dubbelsträngade DNA- och RNA-molekyler "andas" och bindningarna mellan basparna öppnas för bråkdelar av en sekund. När detta händer, Janus PNA sätter in sig själv mellan de separerade strängarna. Om basparen inte matchar, Janus PNA stöts ut från DNA-molekylen. Men om de matchar, Janus PNA binder till båda strängarna i molekylen.
Janus gamma PNA har ett brett utbud av biologiska och biomedicinska användningsområden. De kan utformas för att rikta in sig på genomiskt DNA för genredigering och transkriptionsreglering. De kan också utformas för att binda sekvensspecifikt och selektivt till de sekundära och tertiära strukturerna av RNA, något som traditionella antisensemedel och småmolekylära ligander inte kan göra. Till exempel, Janus gamma PNA kan programmeras att binda till RNA-upprepade expansioner, vilket kan leda till nya behandlingar för ett antal neuromuskulära och neurodegenerativa störningar, inklusive myotonisk dystrofi typ 1 och Huntingtons sjukdom, eller till icke-kodande RNA, inklusive patogens ribosomala och telomeras-RNA, för att bekämpa genetiska och infektionssjukdomar.
Tekniken utforskas av startups såväl som av läkemedelsföretag för terapeutisk utveckling.