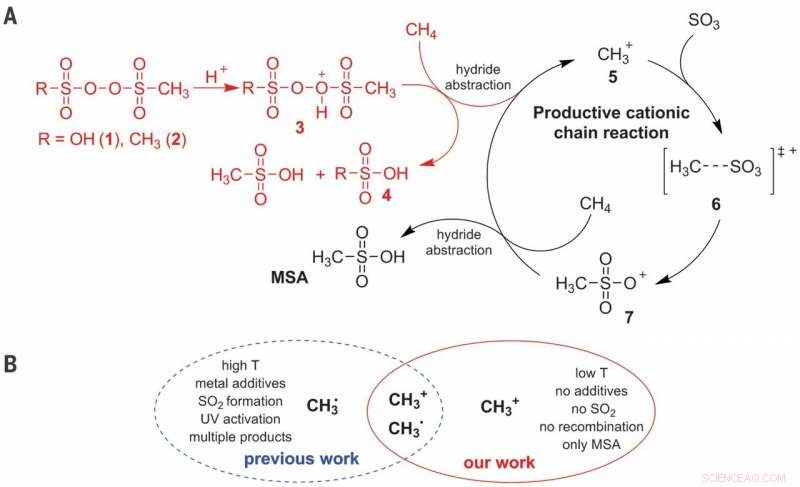
(A) Föreslagen jonisk reaktionsmekanism för C -H -aktivering av CH4 vid selektiv produktion av MSA (metansulfonsyra). (B) Fördelar med den katjoniska vägen framför den radikala vägen. T, temperatur. Kredit:Vetenskap, doi:10.1126/science.aav0177
Metan är en viktig komponent i naturgas och en av de svåraste molekylerna för kontrollerad aktivering, eftersom det mesta av produkten resulterar i koldioxid. Den industriella omvandlingen av metan till alkoholderivat är vanligtvis baserad på en kretsloppsväg som börjar med överoxidation till kolmonoxid. Även om mer direkta tillvägagångssätt har visat lovande i mycket sura medier i liten skala, de är inte riktigt kostnadseffektiva. I en färsk studie som nu publicerats i Vetenskap , Christian Díaz-Urrutia och Timo Ott vid Grillo-Werke AG Companys FoU-avdelning beskriver en reaktion i pilotanläggningsskala som direkt kombinerade metan (CH 4 ) och svaveltrioxid (SO 3 ) i svavelsyra (H 2 SÅ 4 ) för att bilda metansulfon (CH 4 O 3 S) syra utan biprodukter. Reaktionen verkade fortskrida via en katjonisk kedjemekanism initierad genom att tillsätta en låg koncentration av sulfonylperoxid, förökas med metenium (CH 3 + ) molekyler.
Direkt funktionalisering av metan för att bilda förädlade produkter är en utmaning på grund av potentiell överoxidation i många reaktionsmiljöer och sulfonering är ett attraktivt tillvägagångssätt för att uppnå selektiviteten av intresse. I den praktiska processen, Díaz-Urrutia och Ott producerade metansulfonsyra (MSA) med endast två huvudreaktanter; metan och svaveltrioxid. De uppnådde 99 procent selektivitet och utbyte av MSA i arbetet. Forskarna baserade den elektrofila initiatorn på ett sulfonylperoxidderivat, som de protonerade under supersura förhållanden för att producera en mycket elektrofil syreatom som kan aktivera en C-H-bindning av metan. De föreslog mekanistiska studier för att stödja bildandet av en katjonmeten (CH 3 + ) som en nyckelmellanprodukt under reaktionen. Den föreslagna metoden är skalbar med reaktorer kopplade i serie för att prospektivt producera upp till 20 ton MSA per år.
Medan storskalig frackingteknik och biogasproduktion har gett tillgång till stora mängder inaktiv metan, den största kemiska omvandlingen av metan är fortfarande begränsad till de mycket energikrävande Fischer-Tropsch-processerna. För närvarande, metan omvandlas industriellt till Syngas, en blandning av kolmonoxid och väte, för att bilda användbara produkter inklusive metanol och Fischer-Tropsch kolväten, som syntetiseras i efterföljande steg. Produktionen av syngas är kraftigt kostnadsbegränsande, dock; "MegaMethanol"-fabriker eller Fischer-Tropsch-pärlkomplexet i Qatar överstiger 10 miljoner ton (MT) av den totala årliga kolväteproduktionen. Som ett resultat, den direkta omvandlingen av metan till värdefulla produkter med en ekonomiskt lönsam teknik är av extremt intresse.
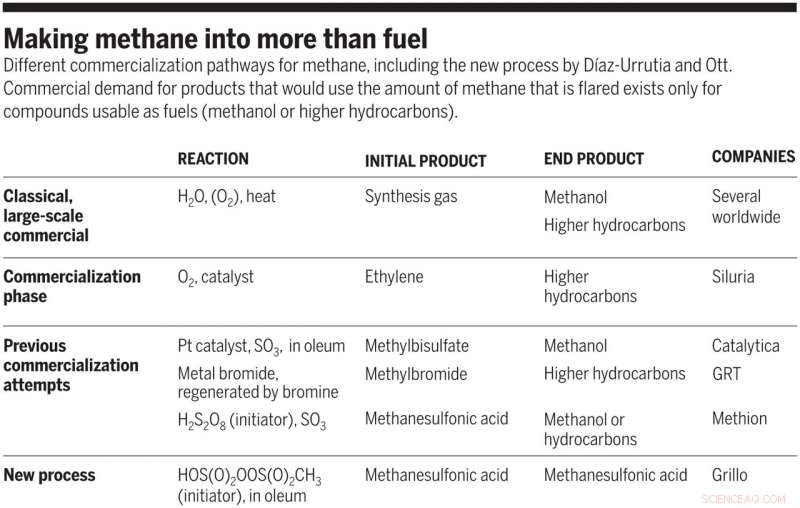
Att göra metan till mer än bränsle. Olika kommersialiseringsvägar för metan, inklusive den nya processen av Díaz-Urrutia och Ott. Kommersiell efterfrågan på produkter som skulle använda mängden metan som blossar upp finns bara för föreningar som kan användas som bränslen (metanol eller högre kolväten). Kredit:Vetenskap, doi:10.1126/science.aav0177
I detta sammanhang, potentialen att sulfonera metan (CH 4 ) till metansulfonsyra (CH 4 O 3 S, MSA) har uppnått betydande uppmärksamhet på grund av överflöd av både råvaror och förmågan till dess snabba integration i befintliga industriella kemiska processer. MSA är biologiskt nedbrytbart och icke-oxiderande med potentiella tillämpningar inom metallåtervinning, energilagring och produktion av biodiesel. Tidigare arbete med metansulfonering led av låga utbyten och omvandlingar, på grund av friradikal rekombination, resulterar i oönskade biprodukter som etan, gör metoderna olämpliga för storskalig produktion. Tekniskt, balansen mellan reaktivitet och selektivitet som krävs av en industriell process kan tillhandahållas genom supersyrakemi. Díaz-Urrutia och Ott rapporterade om behandling av oleum (20 till 60 procent svaveltrioxid) med CH 4 vid cirka 50 0 C med mindre än 1 molprocent av den elektrofila initiatorn för att bilda MSA med 99 procent utbyte och 99 procent selektivitet.
CH 4(g) + SÅ 3(l) → CH 3 SÅ 3 H (l)
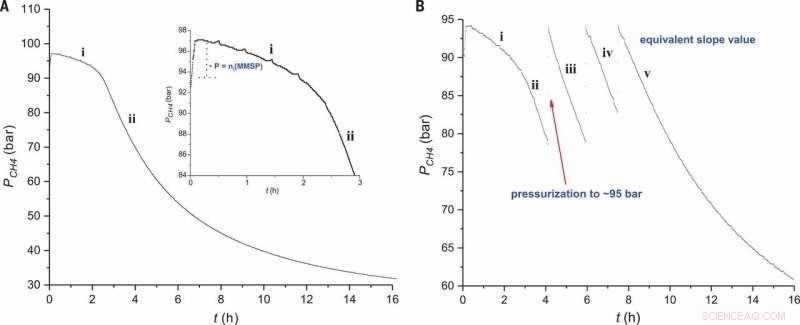
Reaktionsprofil för metansulfonering. Trycket av CH4 plottas mot tiden under (A) standardförhållanden med användning av 0,9 mol% elektrofil initiator (Figur 2, post 2) och (B) successiva tillsatser av CH4 (Fig. 2, post 3). Insättningen i (A) visar en inzoomad vy av region i. Kredit:Vetenskap, doi:10.1126/science.aav0177.
Forskarna studerade först reaktionen i ett batchsystem för att optimera experimentella förhållanden och få ytterligare insikt i reaktionsmekanismen. För den elektrofila initiatorn, de använde monometylsulfonylperoxidsvavelsyra (MMSP) för att förbättra den tekniska genomförbarheten. För ökad produktivitet, de använde en fyra-liters reaktor istället för en 400 ml reaktor, på grund av större mängder CH 4 bildas i huvudutrymmet i den större reaktorn. Forskarna kunde således upprätthålla konstanta mängder metan under hela reaktionen för högre utbyten av MSA. De använde en optimal temperatur på 50 0 C för att uppnå mer än 99 procent selektivitet mot MSA, medan tidigare radikala vägar hade liknande resultat vid högre temperaturer (85 0 C) på grund av termisk sönderdelning av den elektrofila sulfonylperoxidinitiatorn. Lågtemperaturexperiment kan också erbjuda hög omvandling och MSA-selektivitet, men krävde längre reaktionstider. Díaz-Urrutia och Ott gav jämförelsevis insikter för att stödja en icke-radikal mekanism i det nuvarande arbetet.
När forskarna undersökte reaktionsprofilen för experimentet, de observerade en induktionsperiod omedelbart efter tillsats av den elektrofila reaktorn, där mängden MSA (produkt) var proportionell mot den initiala mängden MMSP (initiator). I steg två av reaktionsprofilen, de observerade lösligheten av CH 4 minska med ökande tryck i reaktorn. Aktiveringsenergin för processen bestämdes till 111±1 kJ/mol, liknande de som tidigare rapporterats. Den beskrivna katjoniska vägen inträffade under mycket specifika förhållanden. Forskarna uppnådde hög selektivitet genom elektroniska förändringar i elektrofila substitutioner, i motsats till de tidigare rapporterade friradikalbaserade atomabstraktionsreaktionerna.

Sulfonering av metan till MSA. (A) Schematisk över Díaz-Urrutia- och Ott-processen. Reaktionen fortskrider som en kaskad genom reaktorer kopplade i serie. Pilotanläggningen kunde producera upp till 20 ton MSA per år. Överskottet SO3 släcks i reaktor Q, CH4-överskottsströmmen och MSA/H2SO4-sumpströmmen recirkuleras tillbaka till reaktor 1, och den MSA-berikade blandningen destilleras i kolumn D för erhållande av ren MSA. (B) Koncentrationen av MSA ökar när den passerar genom reaktorerna. (C) Avlång kvartsfönsterreaktor med gashjul, för förbättrad CH4-blandning. Kredit:Vetenskap, doi:10.1126/science.aav0177.
Eftersom de första resultaten var mycket lovande, forskarna byggde en pilotanläggning och testade den ekonomiska och tekniska genomförbarheten av MSA-produktion i industriell skala. Díaz-Urrutia och Ott konstruerade anläggningen med en beräknad kapacitet på 20 ton/år MSA-produktion, baserat på deras batchreaktioner i laboratorieskala, och stod för metanlöslighet och återvinning, samt för koncentrationen av svaveltrioxid och metan. Denna konfiguration gjorde det möjligt för forskarna att konstant öka koncentrationen av MSA när reaktionsblandningen passerade genom reaktorerna. När de använde gaskromatografi med flamjoniseringsdetektion (GC-FID) för att övervaka proverna, de upptäckte inte närvaron av högre alkaner i den återvunna strömmen av metan eller några andra radikalrekombinationsprodukter, möjliggör dess direkta användning som återkopplingslager för kaskadreaktionen.
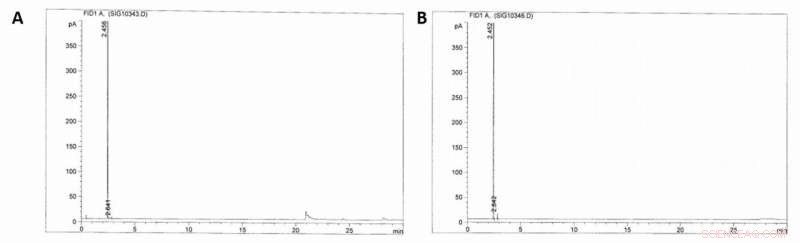
GC-FID-kromatogram. A) GC-FID-kromatogram av reaktorns gasfas (100 bar) innan sulfonering av metan har skett. B) GC-FID-kromatogram av gasfasen efter (~40 bar) sulfoneringen av metan har inträffat (16 timmar, rykande svavelsyra 36 %, 50°C). Kredit:Vetenskap, doi:10.1126/science.aav0177.
För att ha råd med ren MSA, Díaz-Urrutia och Ott avslutade processen genom ett sista destillationssteg. De återvände sedan den återstående blandningen av svavelsyra och MSA till den första reaktorn för fortsatt regenerering av svaveltrioxid och svavelsyra (SO 3 och H 2 SÅ 4 ). Med hjälp av de fyra reaktionskamrarna i installationen, forskarna kunde producera 200 kg ren MSA per vecka, uppgår till två till tre ton på 80 dagar. På det här sättet, den påvisade kombinationen av hög selektivitet, omvandling och atomekonomi gjorde processen idealisk för storskalig valorisering av de lättillgängliga metan- och svaveltrioxidreagensen.
Om denna nya process av metansulfonsyra blir framgångsrik på marknaden, billigare reagens kommer att kunna ersätta de mineralsyror som för närvarande används. Dock, även om produktionen av MSA skulle öka dramatiskt, Mängden metan som förbrukas i processen skulle fortfarande försämras av de mängder som flammade upp. Ändå, Díaz-Urrutias och Otts arbete förutspår en ny syntetisk kemisk process för att syntetisera en intressant kemikalie, vilket gör det möjligt för forskarna att föreställa sig en rad förädlade produkter som ska härledas från metan eller högre alkaner genom att använda denna väg av supersyrakemi i framtiden.
© 2019 Science X Network