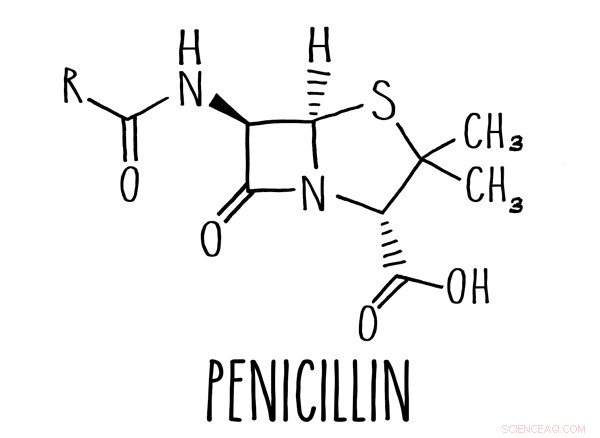
En beta-laktamring är kärnan i många antibiotika, inklusive penicillin. Kredit:Caltech
I den pågående kapprustningen med människor och deras antibiotika på ena sidan, och bakterier med deras förmåga att utveckla försvar mot antibiotika å andra sidan, människor har värvat en ny allierad – andra bakterier.
Många vanliga antibiotika, inklusive det mest kända antibiotikumet, penicillin, är baserade kring en molekylstruktur som kallas en beta-laktamring. Dessa droger, det passande namnet betalaktamantibiotika, störa en bakteries förmåga att bygga sin cellvägg.
När bakterier utvecklar resistens mot befintliga antibiotika, forskare och läkemedelsföretag arbetar för att skapa nya. Det betyder att mycket arbete görs med att skapa nya typer av betalaktamer, och det är där Frances Arnolds labb kommer in i bilden.
Beta-laktamer görs genom att ta en kedjeliknande molekyl och slinga den, ungefär som att ta ena änden av ett snöre och knyta den i en knut till mitten av snöret.
Den största utmaningen är att kontrollera exakt var längs molekylen reaktionen äger rum. Med traditionell syntetisk kemi, kemister måste fästa extra bitar på molekyler som de vill förvandla till betalaktamer. Utan de där extra bitarna, knutarna kommer att hamna på inkonsekventa ställen, vilket resulterar i några slingor som är stora och några som är små. Det är inte önskvärt för någon som försöker tillverka en konsekvent sats antibiotika. Men tillägget av de extra bitarna gör syntesen mer komplicerad eftersom ytterligare steg krävs för att lägga till dem och ännu fler steg för att ta bort dem efter att loopningen är klar.

En laktamring skapas genom att en molekyl loopas på sig själv, ungefär som att knyta en ögla i ett snöre. Kredit:Caltech
Doktorand Inha Cho och postdoktor Zhi-Jun Jia, båda från Arnolds labb, har utvecklat något enklare genom att använda riktad evolution, en teknik utvecklad av Arnold, Linus Pauling professor i kemiteknik, Bioteknik och biokemi, och chef för Donna och Benjamin M. Rosen Bioengineering Center. I riktad evolution, som Arnold utvecklade på 1990-talet och som hon fick 2018 års Nobelpris i kemi, enzymer utvecklas i ett labb tills de beter sig på ett önskat sätt. Den genetiska koden för ett användbart enzym överförs till bakterier som Escherichia coli. När bakterierna växer, dela upp, och gå om sina liv, de tar bort enzymet.
I detta fall, Cho och Jia tog ett enzym som kallas cytokrom P450, som har varit en mångsidig arbetshäst i Arnold-labbet, och utvecklade det för att producera betalaktamer. Två andra versioner av enzymer skapades också för att konstruera andra ringstorlekar av laktamer. En version skapar en gamma-laktam, en slinga med fyra kolatomer och en kväveatom. Och den andra versionen skapar en delta-laktam, en slinga med fem kolatomer och en kväveatom.
"Vi utvecklar nya enzymer med aktivitet som inte kan hittas i naturen, " säger Cho. "Laktamer kan finnas i många olika droger, men speciellt i antibiotika, och vi behöver alltid nya."
Jia påpekar att enzymerna de har skapat också är otroligt effektiva, med varje molekyl av enzym som kan producera upp till en miljon betalaktammolekyler. "De representerar de mest effektiva enzymerna som skapas i vårt labb, och är redo för industriella tillämpningar, säger Jia.
Pappret, med titeln "Site-selektiv enzymatisk CH-amidering för syntes av olika laktamer" och medförfattare av Arnold, visas i 10 maj-numret av Vetenskap .