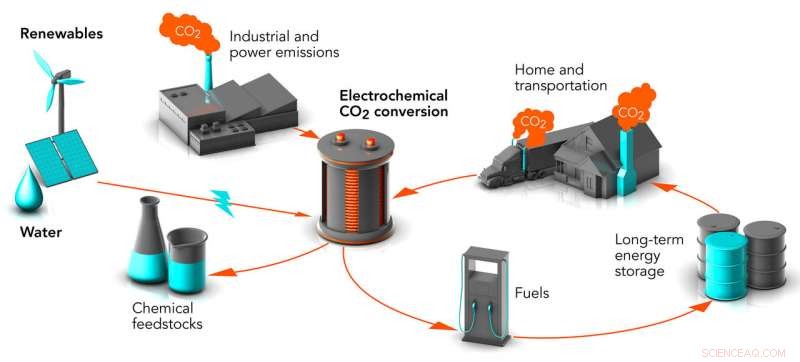
Forskare vid Stanford och SLAC arbetar med sätt att omvandla avfall koldioxid (CO2) till kemiska råvaror och bränslen, förvandla en potent växthusgas till värdefulla produkter. Processen kallas elektrokemisk omvandling. När den drivs av förnybara energikällor, det skulle kunna minska halterna av koldioxid i luften och lagra energi från dessa intermittenta källor i en form som kan användas när som helst. Upphovsman:Greg Stewart/SLAC National Accelerator Laboratory
Ett sätt att minska koldioxidhalten i atmosfären, som nu är på sin högsta punkt i 800, 000 år, skulle vara att fånga upp den potenta växthusgasen från rökstackar från fabriker och kraftverk och använda förnybar energi för att förvandla den till saker vi behöver, säger Thomas Jaramillo.
Som chef för SUNCAT Center for Interface Science and Catalysis, ett gemensamt institut för Stanford University och Department of Energys SLAC National Accelerator Laboratory, han är i stånd att hjälpa till att få det att hända.
Ett stort fokus för SUNCAT -forskning är att hitta sätt att omvandla CO 2 till kemikalier, bränslen, och andra produkter, från metanol till plast, rengöringsmedel och syntetisk naturgas. Produktionen av dessa kemikalier och material från ingredienser från fossila bränslen står nu för 10 % av de globala koldioxidutsläppen; produktion av bensin, diesel, och flygbränsle står för mycket, mycket mer.
"Vi har redan släppt ut för mycket koldioxid 2 , och vi är på väg att fortsätta släppa ut det i flera år, eftersom 80% av den energi som förbrukas världen över idag kommer från fossila bränslen, " säger Stephanie Nitopi, vars SUNCAT -forskning ligger till grund för hennes nyförvärvade Stanford Ph.D.
"Du kan fånga CO 2 från rökstackar och förvara det under jorden, "säger hon." Det är en teknik som just nu spelas. Ett alternativ är att använda det som råvara för att tillverka bränslen, plast, och specialkemikalier, vilket förskjuter det finansiella paradigmet. Avfall CO 2 utsläpp nu blir något du kan återvinna till värdefulla produkter, ger ett nytt incitament att minska mängden koldioxid 2 släpps ut i atmosfären. Det är en win-win."
Vi frågade Nitopi, Jaramillo, SUNCAT -personalforskaren Christopher Hahn och postdoktoralforskaren Lei Wang berättar vad de arbetar med och varför det är viktigt.
F. Först grunderna:Hur omvandlar du CO 2 i dessa andra produkter?
Tom:Det är i huvudsak en form av artificiell fotosyntes, det är därför DOE:s gemensamma centrum för artificiell fotosyntes finansierar vårt arbete. Växter använder solenergi för att omvandla CO 2 från luften till kol i deras vävnader. Liknande, vi vill utveckla teknik som använder förnybar energi, som sol eller vind, att konvertera CO 2 från industriella utsläpp till kolbaserade produkter.
Chris:Ett sätt att göra detta kallas elektrokemisk CO 2 minskning, där du bubblar CO 2 gas upp genom vatten och det reagerar med vattnet på ytan av en kopparbaserad elektrod. Kopparen fungerar som en katalysator, sammanföra de kemiska ingredienserna på ett sätt som uppmuntrar dem att reagera. Enkelt uttryckt, den initiala reaktionen tar bort en syreatom från CO 2 för att bilda kolmonoxid, eller CO, som är en viktig industrikemikalie i sig. Sedan förvandlar andra elektrokemiska reaktioner CO till viktiga molekyler som alkoholer, bränslen och annat.
Idag kräver denna process en kopparbaserad katalysator. Det är den enda kända som gör jobbet. Men dessa reaktioner kan producera många produkter, och att skilja ut den du vill ha är kostsamt, så vi måste identifiera nya katalysatorer som kan styra reaktionen mot att endast göra den önskade produkten.
Hur så?
Lei:När det gäller att förbättra en katalysators prestanda, en av de viktigaste sakerna vi tittar på är hur man gör dem mer selektiva, så de genererar bara en produkt och inget annat. Cirka 90 procent av bränsle- och kemikalietillverkningen beror på katalysatorer, och att bli av med oönskade biprodukter är en stor del av kostnaden.
Vi tittar också på hur man kan effektivisera katalysatorer genom att öka deras yta, så det finns mycket fler platser i en given volym material där reaktioner kan inträffa samtidigt. Detta ökar produktionstakten.
Nyligen upptäckte vi något överraskande:När vi ökade ytan på en kopparbaserad katalysator genom att forma den till en flagnande "nanoflower"-form, det gjorde reaktionen både mer effektiv och mer selektiv. Faktiskt, it produced virtually no byproduct hydrogen gas that we could measure. So this could offer a way to tune reactions to make them more selective and cost-competitive.
Stephanie:This was so surprising that we decided to revisit all the research we could find on catalyzing electrochemical CO 2 conversion with copper, and the many ways people have tried to understand and fine-tune the process, using both theory and experiments, going back four decades. There's been an explosion of research on this—about 60 papers had been published as of 2006, versus more than 430 out there today—and analyzing all the studies with our collaborators at the Technical University of Denmark took two years.
We were trying to figure out what makes copper special, why it's the only catalyst that can make some of these interesting products, and how we can make it even more efficient and selective—what techniques have actually pushed the needle forward? We also offered our perspectives on promising research directions.
One of our conclusions confirms the results of the earlier study:The copper catalyst's surface area can be used to improve both the selectivity and overall efficiency of reactions. So this is well worth considering as a chemical production strategy.
Does this approach have other benefits?
Tom:Absolutely. If we use clean, renewable energy, like wind or solar, to power the controlled conversion of waste CO 2 to a wide range of other products, this could actually draw down levels of CO 2 in the atmosphere, which we will need to do to stave off the worst effects of global climate change.
Chris:And when we use renewable energy to convert CO 2 to fuels, we're storing the variable energy from those renewables in a form that can be used any time. Dessutom, with the right catalyst, these reactions could take place at close to room temperature, instead of the high temperatures and pressures often needed today, making them much more energy efficient.
How close are we to making it happen?
Tom:Chris and I explored this question in a recent Perspective article in Vetenskap , written with researchers from the University of Toronto and TOTAL American Services, which is an oil and gas exploration and production services firm.
We concluded that renewable energy prices would have to fall below 4 cents per kilowatt hour, and systems would need to convert incoming electricity to chemical products with at least 60% efficiency, to make the approach economically competitive with today's methods.
Chris:This switch couldn't happen all at once; the chemical industry is too big and complex for that. So one approach would be to start with making high-value, high-volume products like ethylene, which is used to make alcohols, polyester, antifreeze, plastics and synthetic rubber. It's a $230 billion global market today. Switching from fossil fuels to CO 2 as a starting ingredient for ethylene in a process powered by renewables could potentially save the equivalent of about 860 million metric tons of CO 2 emissions per year.
The same step-by-step approach applies to sources of CO 2 . Industry could initially use relatively pure CO 2 emissions from cement plants, breweries or distilleries, till exempel, and this would have the side benefit of decentralizing manufacturing. Every country could provide for itself, develop the technology it needs, and give its people a better quality of life.
Tom:Once you enter certain markets and start scaling up the technology, you can attack other products that are tougher to make competitively today. What this paper concludes is that these new processes have a chance to change the world.