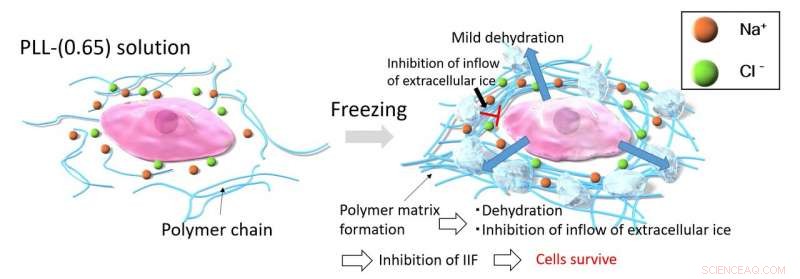
När celler fryses med PLL-(0,65), frysningsprocessen koncentrerar PLL-(0,65)-molekylerna, vilket i sin tur får dem att aggregera på grund av starka intermolekylära attraktionskrafter. Denna aggregering av PLL-(0,65) fångar joner och vatten i matrisen för att förhindra någon dramatisk osmotisk förändring. Den tjocka polymermatrisen hämmar inflödet av extracellulär is in i cellerna, vilket undviker problemet med intracellulär isbildning (IIF). Bild med tillstånd:Kazuaki Matsumura från JAIST.
Kryokonservering innebär att biologiskt material bevaras, såsom celler, vävnader, och organ, vid ultralåga temperaturer så att de kan återupplivas och användas vid ett senare tillfälle. För att uppnå kryokonservering så att de konserverade materialen inte skadas, forskare använder olika kemikalier som kallas kryoskyddsmedel, som underlättar frysningsprocessen. Tyvärr, många av de befintliga kryoskyddande medlen har stora begränsningar. Till exempel, dimetylsulfoxid är användbar för att kryokonservera röda blodkroppar, men det är också giftigt för cellerna.
För att övervinna dessa begränsningar, forskare vid Japan Advanced Institute of Science and Technology (JAIST) och japanska RIKEN har experimenterat med en klass av kemikalier som kallas polyamfolyter, identifiera en polyamfolyt som heter karboxylerat ε-poly-ʟ-lysin (COOH-PLL) som ett lovande kryoskyddsmedel som inte har toxiska effekter på celler.
Dock, mekanismen genom vilken COOH-PLL fungerar som ett kryoskyddsmedel förblev dåligt förstådd, och detta hindrade ansträngningar att utveckla bättre polyamfolyt kryoskyddsmedel. För att komma till rätta med denna kunskapslucka, detta team av forskare, som leddes av professor Kazuaki Matsumura från JAIST — och som även inkluderade Asst. Prof. Robin Rajan från JAIST och Dr. Fumiaki Hayashi och Dr. Toshio Nagashima från RIKEN – genomförde en annan studie där de använde en metod som kallas solid-state nuclear magnetic resonance (NMR) spektroskopi för att karakterisera vad som händer med vattenmolekyler, natrium- och kloridjoner, och en form av COOH-PLL som kallas PLL-(0,65) när de blandas och fryses till temperaturer som används vid kryokonservering. Deras resultat visas i ett färskt nummer av den peer-reviewed tidskriften Communications Materials.
Som förväntat, NMR-signalerna som registrerades från dessa frusna lösningar indikerade minskad molekylär rörlighet och ökad lösningsviskositet (dvs. ökat motstånd mot flöde) vid ultralåga temperaturer. Viktigt, PLL-(0,65)-molekylerna fångade vattenmolekylerna och jonerna på sätt som förhindrade bildandet av intracellulära iskristaller och motverkade effekterna av osmotisk chock (en form av fysiologisk dysfunktion där en plötslig förändring av jonkoncentrationerna runt en cell kan leda till snabbt in- eller utflöde av vätska in i eller från cellen, skadar den). Intracellulära iskristaller och osmotisk chock är viktiga orsaker till cell- eller vävnadsskador under frysning, så förmågan hos PLL-(0,65) att förhindra båda hjälper till att förklara dess effektivitet som kryoskyddsmedel.
När man beskriver det vetenskapliga värdet av dessa fynd, Prof. Matsumura noterar att användningen av NMR "möjliggjorde karakteriseringen av de kryoskyddande egenskaperna hos polymerer som fungerar genom mekanismer som skiljer sig från de för nuvarande kryoskyddsmedel." Han förutspår att denna karakterisering "kommer att underlätta den molekylära designen av nya kryoskyddsmedel, " som kommer att "främja den kliniska användningen av polymera kryoskyddande medel som kan fungera som effektiva alternativ till medel med små molekyler som dimetylsulfoxid och glycerol."
Kryoskyddsmedel för små molekyler är endast användbara för att bevara celler och små vävnader, men polymera kryoskyddsmedel kan göra det möjligt för forskare att uppnå kryokonservering av större vävnadsvolymer eller till och med hela organ. Detta skulle vara ett viktigt framsteg för framväxande områden som regenerativ medicin, som syftar till att återställa normala fysiologiska funktioner genom att ersätta eller regenerera celler, vävnader, och organ.
Teamets resultat kan också ha viktiga konsekvenser för grundläggande biologi. På senare år har forskare har lärt sig att proteiner som är inre störda, som saknar en fast tredimensionell form, tjäna en viktig roll för att skydda celler från skador relaterade till uttorkning och osmotisk chock vid låga temperaturer. Eftersom proteiner i sig är en klass av polyamfolyter, dessa nyligen publicerade rön om COOH-PLL:s beteende vid ultralåga temperaturer kan hjälpa till att förklara mekanismerna genom vilka proteiner som är naturligt störda skyddar celler. Ytterligare forskning om mekanismerna för sådana proteiner kan i sin tur leda till utvecklingen av avancerade material med användning inom regenerativ medicin.
Sammanfattningsvis, dessa fynd kan vara av stort värde för biologi och medicin. "Baserat på vår nu förbättrade förståelse av mekanismerna för polymera kryoskyddande medel, " noterar prof. Matsumura, "vi förväntar oss att utveckla ny kryokonserveringsteknik för stora vävnadsvolymer och organ, som kommer att tillåta implementering av regenerativ medicin i industriell skala via etablering av banker av konstruerade vävnader." Dessa steg mot regenerativ medicin kommer att göra mycket för att förbättra livet för människor som lever med medicinska sjukdomar som för närvarande är obotliga.