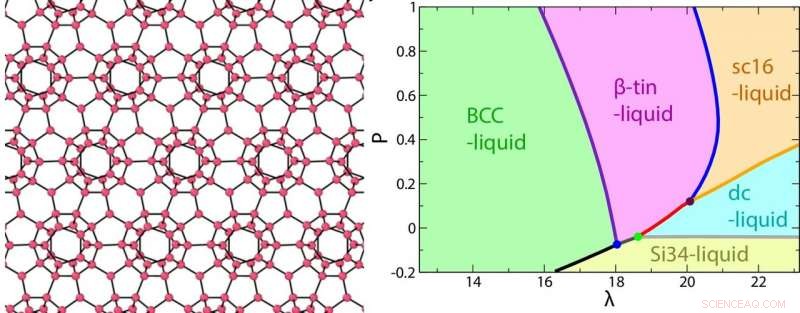
En bild av klathratstrukturen (Si34) av vätska av vattentyp som bildas vid ett undertryck (vänster) och fasdiagrammet som en funktion av tetrahedralitetens styrka λ och tryck P.Kreditt:2018 Hajime Tanaka, Institute of Industrial Science, University of Tokyo
En japanbaserad forskargrupp har studerat det anomala beteendet hos tetraedriska vätskor som vatten. Via datorsimulering, de beräknade fasdiagrammen för en rad modellvätskor. Varierar en parameter som kallas lambda (λ), som styr mängden tetraedrisk struktur i vätskan, de fann att vätskor med större λ visade fler avvikelser, såsom expansion vid låg temperatur. Vattens värde av λ maximerar effekten av tetrahedralitet, därav dess särskilt ovanliga egenskaper.
Vatten har en speciell plats bland vätskor för sina ovanliga egenskaper, och förblir dåligt förstådd. Till exempel, det expanderar precis vid frysning till is, och blir mindre viskös under komprimering, runt atmosfärstryck. Att rationalisera dessa konstigheter är en stor utmaning för fysik och kemi. Ny forskning som leds av University of Tokyos Institute of Industrial Science (IIS) tyder på att de beror på graden av strukturell ordning i vätskan.
Vatten tillhör en vätskeklass vars partiklar bildar lokala tetraedriska strukturer. Tetrahedraliteten i vatten är en följd av vätebindningar mellan molekyler, som är begränsade till fasta riktningar. I en studie i Förfaranden från National Academy of Sciences ( PNAS ), forskarna undersökte varför de fysiska egenskaperna hos vatten uttryckt i dess fasdiagram är så anmärkningsvärda, även jämfört med andra tetraedriska vätskor, såsom kisel och kol.
Tetraedriska vätskor simuleras ofta av en energipotential som kallas SW -modellen. Vätskan antas innehålla två faser i termodynamisk jämvikt - ett stört tillstånd som har hög rotationssymmetri, och ett tetraedriskt ordnat tillstånd som inte gör det. Trots sin enkelhet, modellen förutsäger exakt avvikande vätskebeteenden. Tvålägeegenskapen styrs av parametern lambda (λ), som beskriver den relativa styrkan hos parvisa och trekroppsintermolekylära interaktioner. Den högre λ är, graden av tetraedral ordning ökar.
"Vi insåg att λ, som är ganska stor för vatten, var nyckeln till dessa vätskor unika, "författare John Russo för medstudien." Effektivt λ styr graden av tetrahedralitet:när λ ökar, tetraedriska skal som bildas runt varje molekyl blir energiskt mer stabila. Därav, dessa skal övervinner den ogynnsamma förlusten av entropi som följer med skapandet av ordning. "De lokala tetraederna liknar solid-state strukturer, varför kristalliserar vätskor med hög λ lättare.
Genom att kontinuerligt justera λ, de simulerade en uppsättning fasdiagram för att modellera vad som händer när en "enkel" vätska blir gradvis mer vattenliknande. Med ökande λ, de olika termodynamiska och dynamiska anomalierna hos tetraedriska vätskor- såsom expansion vid låg temperatur och brytning av standard Arrhenius-lag för diffusion- blev mer uttalade.
Dock, det var inte så enkelt som "mer tetraeder lika med konstigare beteende". Tetrahedralitetens inflytande maximerades för vatten, som har λ =23,15. Ovan här, beteendet hos densitet som en funktion av temperaturen närmade sig normalt igen, eftersom skillnaden i volym mellan ordnade och oordningstater började sjunka. Således, vatten har ett utsökt finjusterat eller "Goldilocks" -värde på λ som låter det enkelt växla mellan ordning och slumpmässighet. Detta ger den hög strukturell flexibilitet som svar på förändrade temperaturer eller tryck, som är ursprunget till dess unika beteende.
"Länka observerbara egenskaper, såsom viskositet mot mikroskopiska strukturer, är vad fysisk kemi handlar om, "medförfattare Hajime Tanaka säger." Vatten, det mest förekommande och ändå mest ovanliga ämnet på jorden, har länge varit den sista gränsen i detta avseende. Vi var glada över att en enkel, välkänd modell kan helt förklara vattnets konstigheter, som härrör från den känsliga balansen mellan ordning och oordning i vätskan. "