Mikronstora droppar smält i sarkom, ett stört protein kopplat till ALS, visualiseras genom ett konfokalt fluorescensmikroskop. Upphovsman:Priya Banerjee Lab vid UB
University of Buffalo -fysiker använder innovativa verktyg för att studera egenskaperna hos en bisarr klass av molekyler som kan spela en roll vid sjukdom:proteiner som samlas för att bilda sfäriska droppar inuti mänskliga celler.
Forskarnas senaste forskning belyser de förhållanden som driver sådana droppar att byta från en vätska, flytande tillstånd till en hårdare, geliknande tillstånd.
Publicerad den 19 februari i tidskriften Biomolekyler som en utvald artikel, studien finner att vissa proteindroppar härdar, bli gelatinös i trånga miljöer (t.ex. provrör där många andra molekyler finns, efterliknar de överbelastade förhållandena inuti levande celler).
"Dessa droppbildande proteiner är ett relativt nytt studieområde, så vi vet väldigt lite om deras grundläggande egenskaper, säger huvudutredaren Priya R. Banerjee, Ph.D., biträdande professor i fysik vid UB College of Arts and Sciences. "Som fysiker, vi vill kvantifiera dynamiken i dessa droppar och lära oss vilka faktorer som påverkar dem. Detta är viktigt eftersom dynamiken i proteindroppar är en nyckel till deras cellulära funktion och dysfunktion.
"Tidigare forskning har fokuserat på strukturen hos proteinerna själva, men vårt arbete visar att miljöfaktorer är lika viktiga. Vi ser att yttre förhållanden kan förändra dropparnas inre tillstånd, som kan påverka deras funktion i mänskliga celler. "
Forskningen är viktig eftersom kondenserande proteiner kan vara inblandade i hälsa och sjukdomar. Nya studier pekar på potentiella roller för dessa droppar i så olika funktioner som genuttryck, stressrespons och immunsystemets funktion.
Det nya dokumentet undersöker ett droppbildande protein som kallas smält i sarkom (FUS). Flytande FUS -droppar finns i normala hjärnceller, men hos vissa patienter med den neurodegenerativa sjukdomen amyotrofisk lateral skleros (ALS), proteinet bildar aggregat av fast material, Säger Banerjee. Det är oklart varför.
Använda lasrar för att tvätta och peta proteindroppar
Forskningen använde två innovativa tekniker för att visa hur miljöförhållanden kan påverka droppar tillverkade av FUS eller andra relaterade proteiner.
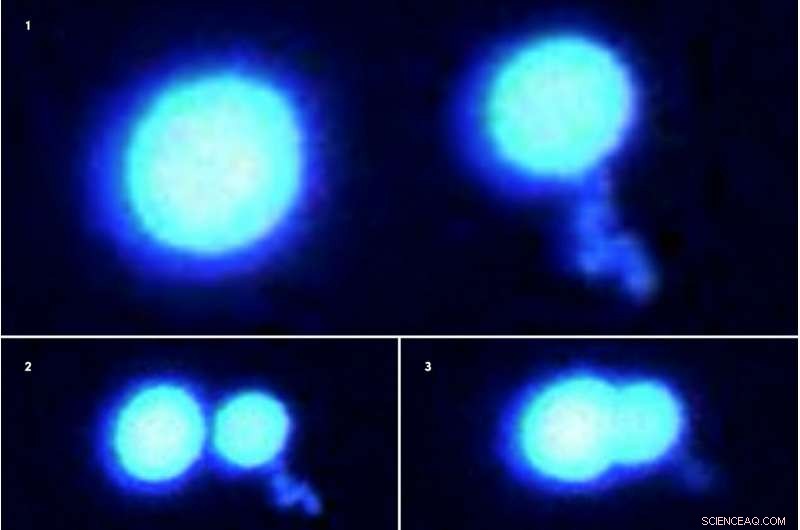
Två proteindroppar vägrar att gå ihop när de skjuts ihop (fluorescensmikroskopbilder 1-3, visas i följd). Dropparna, tillverkad av smält i sarkomproteiner, har det svårt, gelliknande tillstånd när de sitter i en lösning fylld med andra molekyler. Forskare använde state-of-the-art optisk pincetteknik för att ta tag i och manipulera dessa proteinmikrodroppar. Upphovsman:Priya Banerjee Lab vid UB
I en uppsättning experiment, forskare använde mycket fokuserade laserstrålar - kallade optiska pincetter - för att fånga och skjuta ihop två proteindroppar som flyter i en flytande buffertlösning.
Proteindropparna smälte enkelt samman för att bilda en enda större droppe när bufferten var tunt befolkad med andra inerta vulstmolekyler, såsom polyetylenglykol (PEG). Men när koncentrationen av PEG eller andra kemikalier i bufferten ökade, proteindropparna blev mer gelatinartade och kunde inte kombineras helt.
I en andra uppsättning tester, teamet använde lasrar på ett annat sätt - ”laserpoking” - för att studera hur FUS och relaterade proteindroppar reagerar på trånga miljöer.
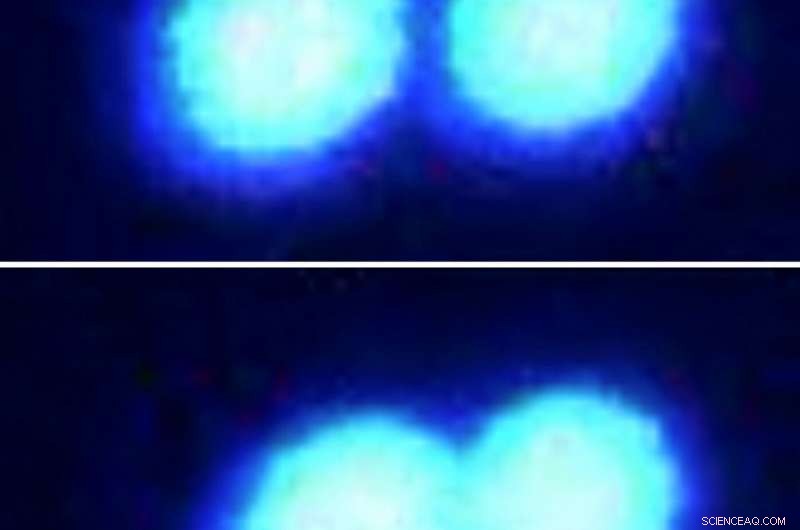
Två proteindroppar smälter lätt ihop när de skjuts ihop (visas sekventiellt i fluorescensmikroskopbilder, uppifrån och ner.) Dropparna, tillverkad av smält i sarkomproteiner, har en flytande konsistens när de sitter i en lösning som är tätt befolkad av andra molekyler. Forskare använde state-of-the-art optisk pincetteknik för att ta tag i och manipulera dessa proteinmikrodroppar. Upphovsman:Priya Banerjee Lab vid UB
I dessa experiment, Banerjee och kollegor fäste fluorescerande taggar till många proteinmolekyler i en enda droppe, får proteinerna att lysa. Forskarna "petade" sedan mitten av droppen med en laser med hög intensitet, ett förfarande som fick alla fluorescerande molekyler som träffades av lasern att bli permanent mörka.
Nästa, forskare mätte hur lång tid det tog för nya glödande proteiner att flytta in i det mörka området. Detta hände snabbt i proteindroppar som flyter i glesbefolkade buffertlösningar. Men återhämtningstiden var dramatiskt långsammare för droppar suspenderade i buffertlösningar tjocka med PEG eller andra föreningar - en indikation, ännu en gång, att proteindroppar blir gelatinösa i trånga miljöer. Fynden gällde både FUS och andra relaterade proteindroppar med olika primära strukturer.
"Våra experiment gjordes i provrör, men våra resultat tyder på att inuti levande celler, trängselstatus kan påverka dynamiken hos proteindroppar, "Säger Banerjee.
En viktig fråga som återstår är om och hur flytande FUS -droppar påverkar proteinets förmåga att forma till fasta klumpar, som sett hos vissa ALS -patienter. Banerjee hoppas kunna ta itu med detta problem genom framtida forskning.