Onlineomslag - ett beräknat miniatyrmesoskop (CM2). Bildkredit:Xue et al., Vetenskapliga framsteg, doi:10.1126/sciadv.abb7508
Online -omslagsfotografiet på Vetenskapliga framsteg denna vecka visar fluorescensavbildning med ett beräknat miniatyrmesoskop (CM 2 ). Tekniken för fluorescensavbildning är ett viktigt verktyg för biologer och neurovetenskapare; dock, konventionella mikroskop och miniatyriserade mikroskop (miniskop) begränsas av produkt med begränsad rymdbandbredd-en mätning av informationskapaciteten för ett optiskt system, grunt skärpedjup och oförmåga att lösa tredimensionella (3-D) distribuerade sändare. För att övervinna befintliga gränser, Yujia Xue och ett team av forskare inom el- och datateknik, biologi, neurofotonik och biomedicinsk teknik vid Boston University, USA, utvecklat ett lätt och kompakt mesoskop som kallas det beräknade miniatyrmesoskopet (CM 2 ).
Den nya plattformen integrerade en mikrolins för avbildning och en LED -array för excitation inom samma inställning. Enheten utförde enkelbilds 3D-avbildning och underlättade en 10-faldig synfältförstärkning och en 100-faldig skärpedjup, jämfört med befintliga miniskop. Xue et al. testade enheten med fluorescerande pärlor och fibrer tillsammans med fantomförsök för att mäta effekterna av bulkspridning och bakgrundsfluorescens. Teamet diskuterar det praktiska med detta mesoskop för breda tillämpningar inom biomedicin och 3D-neural inspelning.
Framstegsfluorescensmikroskopi
Fluorescensmikroskopi är en nyckelteknik inom grundläggande biologi och systemneurovetenskap. Den senaste tekniska utvecklingen syftar till att övervinna skalbarriärer för att undersöka enskilda neuroner med bara några mikron i storlek. Till exempel, makroskop, mesolensmikroskop och tvåfotonmikroskop har börjat överbrygga denna skala; dock, utvecklingen av sådana avbildningssystem begränsas av skalberoende geometriska aberrationer av optiska element. Det uppnåbara synfältet (FOV) begränsas också av systemets grunda skärpedjup i många bioimaging -applikationer. Forskare är också inriktade på att miniatyrisera tekniken för att möjliggöra in vivo -avbildning i fritt uppförande djur. Till exempel, miniatyriserade mikroskop som kallas "miniskop" har fått oöverträffad tillgång till neurala signaler, även om systemen förblir begränsade av sin optik, ungefär som deras fluorescensmikroskopi -motsvarigheter. Xue et al. introducerade och demonstrerade därför ett beräknat miniatyrmikroskop (CM 2 ) med storskalig, 3D-fluorescensmätningar på en kompakt, lätt plattform.
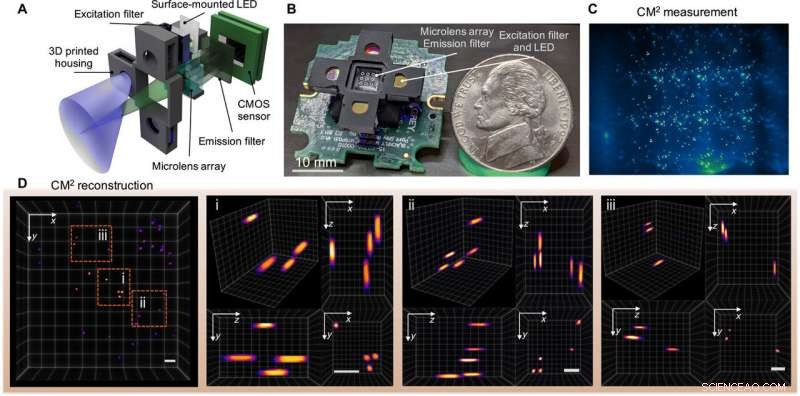
Single-shot 3D fluorescens CM2. (A) CM2 kombinerar en MLA-optik och ljusemitterande diod (LED) array-excitation i en kompakt och lätt plattform. (B) Bild på CM2 -prototypen (de elektriska ledningarna och sensordrivrutinen utelämnas). Foto:Yujia Xue, Boston University. (C) CM2-mätning på 100 μm fluorescerande partiklar suspenderade i klart harts. (D) Projicerad vy av den rekonstruerade CM2-volymen (7,0 mm vid 7,3 mm med 2,5 mm) och tre inzoomningsområden med ortogonala vyer. Skalstänger, 500 μm. CMOS, komplementär metalloxid halvledare. Upphovsman:Science Advances, doi:10.1126/sciadv.abb7508 
Teamet använde enkel optik i installationen för att åstadkomma förbättringar av produktutrymme-bandbredd (SBP) och 3D-avbildning utan att behöva mekanisk skanning. Tekniken kringgick de fysiska gränserna för den integrerade optiken genom att gemensamt designa hårdvaran och algoritmen. CM 2 bildmetod kombinerade flera olika funktioner i mikroskopisk bildbehandling, såsom integrerad avbildning, ljusfältmikroskopi och kodad bländaravbildning. I sin verkningsmekanism, Mikroskopet samlade in en enda 2-D-mätning med hjälp av en mikrolensmatris (MLA) för efterföljande beräkningsmässig rekonstruktion av 3D-fluorescensfördelningen.
CM 2 använde mikrolinsmatrisen som det enda avbildningselementet och tillät installationen att övervinna de synfältgränser (FOV) -gränser som tillämpas av objektivlinsen för konventionella mikroskop. CM 2 algoritm löste 2-D-till-3-D-avvecklingsproblemet för att tillhandahålla djuplösta rekonstruktioner. Xue et al. förklarade principen för CM 2 enkelbilds 3D-avbildningskapacitet genom att dra en analogi till frekvensdelningsmultiplexering (FDM). Teamet kvantifierade sedan uppnådd upplösning av CM 2 genom att beräkna systemets 3D-moduleringsöverföringsfunktion (MTF) och analysera lateral upplösning.
Karakterisering av CM2:s avbildningsprincip, skiftvarians, och upplösning. (A) CM2 producerar axiellt varierande array -PSF:er för att uppnå optisk snittning. Den axiella skjuvningen i sidofokusen kännetecknas väl av den geometriska modellen som presenteras i studien. PCC för de axiellt skannade PSF:erna kvantifierar den förväntade axiella upplösningen. EM, utsläpp. (B) 3D MTF (visas i loggskala) visar att CM2 fångar ut utökad axiell frekvensinformation och förstorar systemets SBP. Stödet från den experimentella MTF matchar med teorin (i streckad kurva). Vinkeln för varje lutat ”band” i MTF bestäms av vinkelplaceringen för motsvarande mikrolins αMLA (i streckad linje). (C) Den laterala skiftvarianten kännetecknas av PCC för de sidoskannade PSF:erna. PSF i den centrala FOV (markerad med orange gränslinjer) innehåller 3 × 3 foci; PSF i den yttre FOV (markerad med blå gränslinjer) innehåller 2 × 3 eller 3 × 2 foci; PSF i hörnet FOV (markerat med gula gränslinjer) innehåller 2 × 2 foci. (D) Upplösningen vid olika regioner av FOV kännetecknas av att rekonstruera ett 5 µm pinhålsobjekt med hjälp av CM2:s skift-invarianta modell. Hela sidobredden vid halv max (FWHM) är genomgående under 7 μm. Den axiella FWHM är ~ 139 μm i centrala FOV och nedbryts till ~ 172 och ~ 189 μm i yttre och hörn FOV, respektive. (E) Geometri för avbildning av ett lutat fluorescerande mål. (F) Rå CM2 -mätning. (G) MIP för rekonstruerad volym (8,1 mm x 5,5 mm x 1,8 mm). Funktionerna på 7 μm (grupp 6, element 2) kan lösas som visas i zoom-in xy-projektionen. Den axiella snittförmågan kännetecknas av xz -projektionen, validera den funktionsstorleksberoende axiella upplösningen. Upphovsman:Science Advances, doi:10.1126/sciadv.abb7508 
Xue et al. approximerade bildbildningen av CM 2 installation med hjälp av en skivvis skift-invariant modell. De kännetecknade upplösningen och lateral skiftvarians för installationen före experimentell avbildning och avbildade ett fluorescerande upplösningsmål för att validera den laterala upplösningen för CM 2 . De validerade observationerna med hjälp av Zemax-simulerade mätningar för att hitta en bra överensstämmelse mellan simuleringarna och experimenten. Den nya plattformen gjorde det möjligt för forskarna att lokalisera fluorescerande emitter fördelade över en stor volym. De testade prestanda för CM 2 på prover med en funktionsstorlek som liknar en enda neuron. Under dessa experiment, CM 2 algoritmen var tolerant mot signalnedbrytningar såsom minskade signal-brusförhållanden för att möjliggöra högkvalitativ, rekonstruktion av hela synfältet. Teamet jämförde CM 2 rekonstruktion och en axiell stapel som förvärvats av en objektivlins för att demonstrera noggrannheten i enkelskottslokalisering av enskilda partiklar.
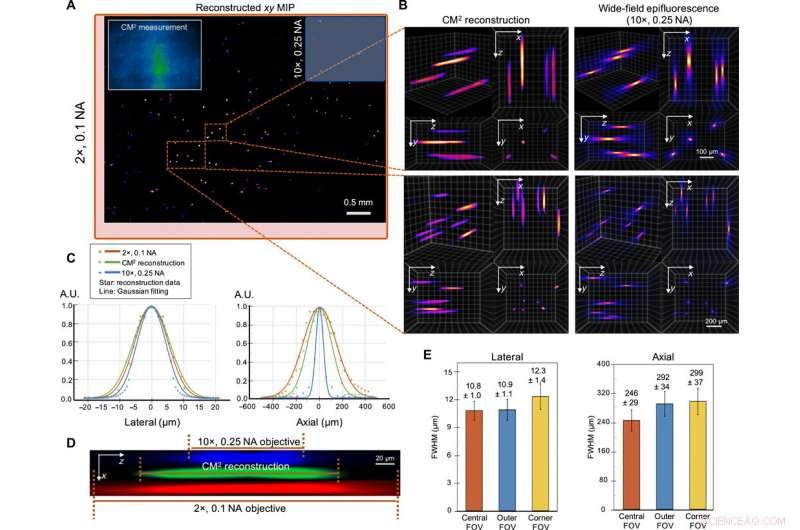
Single-shot 3D-avbildning av 10 μm fluorescerande partiklar i en klar volym. (A) xy MIP för den rekonstruerade volymen som spänner över 5,7 mm med 6,0 mm med 1,0 mm. Övre vänster insats:Rått CM2 -mått. FOV för CM2 är jämförbar med en 2 × objektiv (röd avgränsningsruta) och är ~ 25 × bredare än 10 × objektivet (blå gränslåda). (B) Zooma in CM2 3D-rekonstruktion riktmärkt av den axiella stacken med en 10 ×, 0.25 NA objektiv. (C) Laterala och axiella tvärsnitt av den återvunna 10 µm partikeln. Genom att jämföra med mätningarna från den vanliga bredfältsfluorescensmikroskopin, CM2 återfår troget partikelns sidoprofil och uppnår enstaka djupsnitt. A.U., godtyckliga enheter. (D) xz tvärsnittsvy av en rekonstruerad fluorescerande partikel, jämfört med den axiella stacken som erhållits från 2 × och 10 × objektiv. (E) För att karakterisera rekonstruktionens rumsliga variationer, statistiken över de laterala och axiella FWHM -värdena för de rekonstruerade partiklarna ritas för den centrala, yttre, och hörn FOV. Sidobredden ändras endast något (~ 0,9%) i det yttre FOV men ökar i hörnet FOV (~ 13,9%). Den axiella förlängningen försämras från ~ 246 μm i den centrala FOV till ~ 292 och ~ 299 μm i de yttre och hörn FOV -regionerna, respektive. Upphovsman:Science Advances, doi:10.1126/sciadv.abb7508
Experiment på fluorescerande fibrer på en krökt yta och på kontrollerade spridningsfantomer.
Forskarna testade sedan förmågan att avbilda komplexa volymetriska fluorescerande prover på fluorescerande fibrer spridda på en 3D-tryckt krökt yta, efterlikna ytprofilen för en musbark, spänner över ett brett synfält och ett utökat djup. Algoritmen återställde i fokus fokusstrukturerna och löstes för 3D-objektet, samtidigt som de flesta enskilda fibrerna löses. Teamet genomförde vidare experiment på åtta avbildningsfantomer för att testa prestanda för CM 2 under bulkspridning och stark bakgrundsfluorescens. Under försöken, de utsäde alla fantomer med samma koncentration av målfluorescerande partiklar och krediterade skillnaderna i rekonstruktion till bulkspridning och bakgrundsfluorescens. Teamet inkluderade sedan 1,1 µm bakgrundsfluorescerande partiklar för att efterlikna olösliga fluorescerande källor som vanligen ses på biologiska prover; såsom neutropiler i hjärnan. De kvantifierade spridningsnivån för varje fantom, utförde 3-D rekonstruktion för varje spridande fantom och utförde alla deconvolutions med samma beräkningsinställning. Det uppskattade rekonstruktionsdjupsområdet varierade med ytvariationer i varje fantom.

Rekonstruktion av fluorescerande fibrer. Filmfilen visualiserar den volymetriska rekonstruktionen av fluorescerande fibrer på en böjd yta. För jämförelse, djupkartan uppskattad från brännstapeln från ett vidfält epi-fluorescensmikroskop med ett 2 ×, 0.1 NA -objektiv visas. Upphovsman:Science Advances, doi:10.1126/sciadv.abb7508
På det här sättet, Yujia Xue och kollegor utvecklade ett nytt miniatyriserat fluorescensavbildningssystem för att möjliggöra enstaka mesoskopisk 3D-avbildning. Beräkningsminiatyrmesoskopet (CM 2 ) metodintegrerad fluorescensavbildning och excitationsmodulerna på samma kompakta plattform. Teamet presenterade simuleringarna och experimenten för att fastställa verkningsmekanismen och 3D-avbildningskapaciteten hos CM 2 . De simulerade hjärnövergripande avbildning av kärlnätverk och de primära resultaten var lovande. CM 2 prototyp är ännu inte jämförbar med huvudmonterade in vivo-applikationer (på djurmodeller) i neurovetenskapliga laboratorier, även om teamet tänker sig att optimera enheten för full-kortikal in vivo-avbildning i fritt rörliga möss. Bildenheten kan förbättras ytterligare med ytterligare utveckling av hårdvara och algoritmer för att öppna nya och spännande möjligheter inom in vivo neural inspelning och biomedicinska applikationer.
© 2020 Science X Network