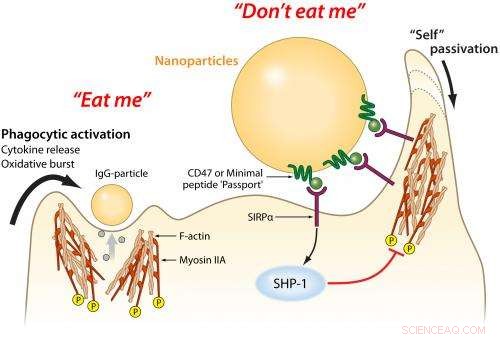
Makrofager är immuncells "gränsvakter" som har utvecklats för att äta alla möjliga främmande mikrober, men de äter också många partiklar som är avsedda för terapi och bildbehandling. En "Minimal peptid" Pass "som är fäst till partiklarna ger igenkänningssignaler så att partiklarna inte äts upp, vilket förbättrar leveransen till sjuka celler i kroppen. Upphovsman:Mary Leonard, Biomedicinsk konst och design, University of Pennsylvania
Kroppens immunsystem finns för att identifiera och förstöra främmande föremål, om de är bakterier, virus, smuts eller fläckar. Tyvärr, nanopartiklar avsedda att leverera läkemedel, och implanterade enheter som pacemaker eller konstgjorda leder, är lika främmande och utsatta för samma svar.
Nu, forskare vid University of Pennsylvania School of Engineering and Applied Science och Penn's Institute for Translational Medicine and Therapeutics har hittat ett sätt att tillhandahålla ett "pass" för sådana terapeutiska apparater, så att de kan ta sig förbi kroppens säkerhetssystem.
Forskningen genomfördes av professor Dennis Discher, doktorander Pia Rodriguez, Takamasa Harada, David Christian och Richard K. Tsai och postdoktor Diego Pantano från Molecular and Cell Biophysics Lab in Chemical and Biomolecular Engineering på Penn.
Det publicerades i tidningen Vetenskap .
"Ur din kropps perspektiv, "Rodriguez sa, "en pilspets för tusen år sedan och en pacemaker idag behandlas likadant - som en utländsk inkräktare.
"Vi skulle verkligen vilja saker som pacemaker, suturer och läkemedelsleveransfordon för att inte orsaka ett inflammatoriskt svar från det medfödda immunsystemet. "
Det medfödda immunsystemet angriper främmande kroppar på ett generellt sätt. Till skillnad från det anpassade immunsystemets inlärda svar, som inkluderar de riktade antikropparna som bildas efter en vaccination, det medfödda immunsystemet försöker förstöra allt det inte känner igen som en del av kroppen.
Detta svar har många cellulära komponenter, inklusive makrofager - bokstavligen "stora ätare" - som hittar, uppsluka och förstöra inkräktare. Proteiner i blodserum fungerar tillsammans med makrofager; de fäster vid föremål i blodströmmen och uppmärksammar makrofager. Om makrofagen bestämmer att dessa proteiner sitter fast vid en främmande inkräktare, de kommer att äta den eller signalera andra makrofager att bilda en barriär runt den.
Läkemedelsleveransnanopartiklar utlöser naturligtvis detta svar, så forskarnas tidigare försök att kringgå det innebar att belägga partiklarna med polymer "borstar". Dessa borstar sticker ut från nanopartikeln och försöker fysiskt blockera olika blodserumproteiner från att fastna på dess yta.
Dock, dessa borstar saktar bara ner makrofag-signalproteinerna, så Discher och kollegor försökte ett annat tillvägagångssätt:Övertyga makrofagerna om att nanopartiklarna var en del av kroppen och inte borde rensas.
2008, Dischers grupp visade att det humana proteinet CD47, finns på nästan alla däggdjurscellmembran, binder till en makrofagreceptor som kallas SIRPa hos människor. Som en patrullerande gränsbevakare som inspekterar ett pass, om en makrofags SIRPa binder till en cell CD47, den berättar för makrofagen att cellen inte är en inkräktare och ska få fortsätta.
"Det kan finnas andra molekyler som hjälper till att dämpa makrofagsvaret, "Discher sa." Men mänsklig CD47 är helt klart en som säger, "Ät inte mig". "
Sedan publiceringen av studien har andra forskare bestämde den kombinerade strukturen för CD47 och SIRPa tillsammans. Med hjälp av denna information, Dischers grupp kunde beräkningsutforma den minsta sekvens av aminosyror som skulle fungera som CD47. Denna "minimala peptid" måste vikas och passa tillräckligt bra in i SIRPa -receptorn för att fungera som ett giltigt pass.
Efter kemiskt syntetisering av denna minimala peptid, Dischers team kopplade den till konventionella nanopartiklar som kan användas i en mängd olika experiment.
"Nu, vem som helst kan göra peptiden och lägga den på vad de vill, "Sa Rodriguez
Forskargruppens experiment använde en musmodell för att demonstrera bättre avbildning av tumörer och såväl som förbättrad effektivitet av en partikel mot läkemedelstillförsel mot cancer.
Eftersom denna minimala peptid en dag kan fästas vid ett brett utbud av läkemedelsleveransfordon, forskarna bifogade också antikroppar av den typ som kan användas för att rikta cancerceller eller andra typer av sjuk vävnad. Utöver ett bevis på koncept för terapi, dessa antikroppar tjänade också makrofagernas uppmärksamhet och säkerställde att den minimala peptidens pass kontrollerades och godkändes.
"Vi visar att peptiden faktiskt hämmar makrofagens svar, "Discher sa." Vi tvingar fram interaktionen och överväldiger den sedan. "
Testet av denna minimala peptids effekt var hos möss som var genetiskt modifierade så att deras makofager hade SIRPa -receptorer som liknade människor. Forskarna injicerade två sorters nanopartiklar - de som bär peptidpasset och de utan - och mätte sedan hur snabbt mössens immunsystem rensade dem.
"Vi använde olika fluorescerande färgämnen på de två typerna av nanopartiklar, så vi kunde ta blodprov var 10:e minut och mäta hur många partiklar av varje slag som var kvar med hjälp av flödescytometri, "Rodriguez sa." Vi injicerade de två partiklarna i ett 1-till-1-förhållande och 20-30 minuter senare, det fanns upp till fyra gånger så många partiklar med peptiden kvar. "
Även att ge terapeutiska nanopartiklar ytterligare en halvtimme innan de äts av makrofager kan vara en stor välsignelse för behandlingar. Sådana nanopartiklar kan behöva göra några resor genom den makrofag-tunga mjälten och levern för att hitta sina mål, men de ska inte stanna i kroppen på obestämd tid. Andra kombinationer av externa proteiner kan vara lämpliga för mer permanenta enheter, såsom pacemakerledningar, gör att de kan gömma sig från immunsystemet under längre perioder.
Även om mer forskning är nödvändig innan sådana tillämpningar blir verklighet, att reducera peptiden till en sekvens av endast några få aminosyror var ett kritiskt steg. Den relativa enkelheten hos denna passmolekyl som är lättare att syntetisera gör den till en mer attraktiv komponent för framtida läkemedel.
"Det kan göras rent i en maskin, "Discher sa, "och enkelt modifieras under syntesen för att fästa på alla typer av implanterade och injicerade saker, med målet att lura kroppen att acceptera dessa saker som "jag". "