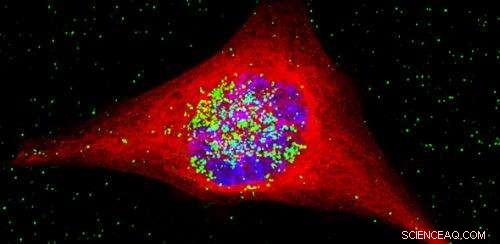
En cancercell som innehåller nanopartiklarna. Nanopartiklarna är gröna, och har kommit in i kärnan, vilket är området i blått. Kredit:M. Welland
En "trojansk häst" behandling för en aggressiv form av hjärncancer, som innebär att man använder små nanopartiklar av guld för att döda tumörceller, har framgångsrikt testats av forskare.
Den banbrytande tekniken kan så småningom användas för att behandla glioblastoma multiforme, som är den vanligaste och mest aggressiva hjärntumören hos vuxna, och notoriskt svåra att behandla. Många drabbade dör inom några månader efter diagnosen, och bara sex av 100 patienter med tillståndet lever efter fem år.
Forskningen involverade ingenjörsmässiga nanostrukturer innehållande både guld och cisplatin, ett konventionellt kemoterapiläkemedel. Dessa släpptes in i tumörceller som hade tagits från glioblastompatienter och odlats i labbet.
Väl inne, dessa "nanosfärer" utsattes för strålbehandling. Detta fick guldet att frigöra elektroner som skadade cancercellens DNA och dess övergripande struktur, vilket förstärker effekten av kemoterapiläkemedlet.
Processen var så effektiv att 20 dagar senare, cellkulturen visade inga tecken på någon återupplivning, vilket tyder på att tumörcellerna hade förstörts.
Även om ytterligare arbete måste göras innan samma teknik kan användas för att behandla personer med glioblastom, resultaten utgör en mycket lovande grund för framtida terapier. Viktigt, forskningen utfördes på cellinjer som härrörde direkt från glioblastompatienter, gör det möjligt för teamet att testa strategin för utveckling, läkemedelsresistenta tumörer.
Studien leddes av Mark Welland, Professor i nanoteknik och stipendiat vid St John's College, Universitetet i Cambridge, och Dr Colin Watts, en kliniker vetenskapsman och hederskonsult neurokirurg vid institutionen för klinisk neurovetenskap. Deras arbete rapporteras i tidskriften Royal Society of Chemistry, Nanoskala .
"Den kombinerade terapin som vi har utarbetat verkar vara otroligt effektiv i levande cellkultur, " sa professor Welland. "Detta är inget botemedel, men det visar vad nanoteknologi kan åstadkomma för att bekämpa dessa aggressiva cancerformer. Genom att kombinera denna strategi med material som riktar sig mot cancerceller, vi borde kunna utveckla en terapi för glioblastom och andra utmanande cancerformer i framtiden."
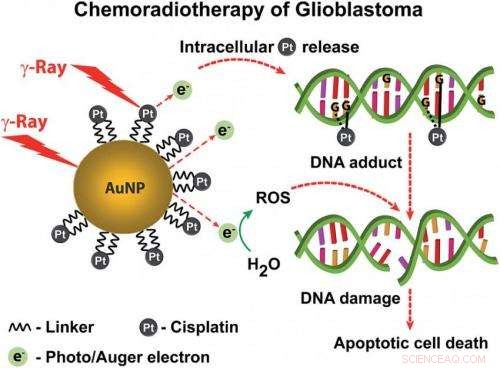
Ett diagram som visar nanosfärens sammansättning. Kredit:M. Welland
Hittills, glioblastoma multiforme (GBM) har visat sig vara mycket resistent mot behandlingar. En anledning till detta är att tumörcellerna invaderar omgivande, frisk hjärnvävnad, vilket gör kirurgiskt avlägsnande av tumören praktiskt taget omöjligt.
Används på egen hand, kemoterapiläkemedel kan orsaka en nedgång i hastigheten med vilken tumören sprider sig. I många fall, dock, Det här är temporärt, när cellpopulationen sedan återhämtar sig.
"Vi måste kunna träffa cancercellerna direkt med mer än en behandling samtidigt", sa Dr Watts. "Detta är viktigt eftersom vissa cancerceller är mer motståndskraftiga mot en typ av behandling än en annan. Nanoteknik ger möjligheten att ge cancercellerna denna "dubbla smäll" och öppna upp för nya behandlingsalternativ i framtiden."
I ett försök att slå tumörer mer heltäckande, forskare har under en tid undersökt hur guldnanopartiklar kan användas i behandlingar. Guld är ett godartat material som i sig inte utgör något hot mot patienten, och storleken och formen på partiklarna kan kontrolleras mycket noggrant.
När de utsätts för strålbehandling, partiklarna avger en typ av lågenergielektron, kända som Auger-elektroner, kan skada den sjuka cellens DNA och andra intracellulära molekyler. Detta låga energiutsläpp innebär att de bara påverkar på kort håll, så de orsakar ingen allvarlig skada på friska celler som finns i närheten.
I den nya studien, forskarna lindade först guldnanopartiklar inuti en positivt laddad polymer, polyetylenimin. Detta interagerade med proteiner på cellytan som kallas proteoglykaner vilket ledde till att nanopartiklarna fick i sig av cellen.
Väl där, det var möjligt att excitera det med standardstrålbehandling, som många GBM-patienter genomgår som en självklarhet. Detta frigjorde elektronerna för att attackera cellens DNA.
Medan guld nanosfärer, utan medföljande droger, visade sig orsaka betydande cellskador, Behandlingsresistenta cellpopulationer återhämtade sig så småningom flera dagar efter strålbehandlingen. Som ett resultat, forskarna konstruerade sedan en andra nanostruktur som var fylld med cisplatin.
Den kemoterapeutiska effekten av cisplatin kombinerat med den radiosensibiliserande effekten av guldnanopartiklar resulterade i förbättrad synergi som möjliggör en mer effektiv cellulär skada. Efterföljande tester visade att behandlingen hade minskat den synliga cellpopulationen med en faktor på 100 tusen, jämfört med en obehandlad cellkultur, inom loppet av bara 20 dagar. Ingen befolkningsförnyelse upptäcktes.
Forskarna tror att liknande modeller så småningom kan användas för att behandla andra typer av utmanande cancerformer. Först, dock, själva metoden måste omvandlas till en användbar behandling för GBM-patienter. Denna process, som kommer att stå i fokus för mycket av gruppens kommande forskning, kommer med nödvändighet att innebära omfattande försök. Ytterligare arbete måste göras, för, för att bestämma hur behandlingen bäst ska levereras och inom andra områden, som att modifiera storleken och ytkemin hos nanomedicinen så att kroppen kan ta emot den på ett säkert sätt.
Sonali Setua, en doktorand som arbetade med projektet, sa:"Det var oerhört tillfredsställande att jaga ett så utmanande mål och att kunna rikta in sig på och förstöra dessa aggressiva cancerceller. Detta fynd har enorm potential att testas i en klinisk prövning inom en snar framtid och utvecklas till en ny behandling att övervinna terapeutisk resistens av glioblastom."
Welland tillade att betydelsen av gruppens resultat hittills delvis berodde på det direkta samarbetet mellan nanoforskare och kliniker. "Det gjorde en enorm skillnad, eftersom vi genom att arbeta med kirurger kunde säkerställa att nanovetenskapen var kliniskt relevant, " sa han. "Det optimerar våra chanser att ta det här bortom labbstadiet, och faktiskt ha en klinisk effekt."