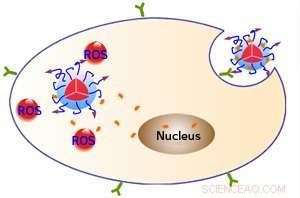
Ytpeptider (lila pilar) tillåter fluorescerande nanopartiklar att binda till ett protein (grönt) på målcellerna och tas upp i cellerna. Ljusexponering får nanopartiklarna att generera reaktiva syrearter (ROS), dödar cellerna, och frigör även läkemedlet doxorubicin (apelsin), som sedan kan komma in i cellkärnan. Kredit:WILEY-VCH Verlag GmbH &Co. KGaA, Weinheim
Nanosystem som är "teranostiska" - de kombinerar både terapeutiska och diagnostiska funktioner - utgör en spännande ny möjlighet för att leverera läkemedel till specifika celler och identifiera platser för sjukdomar. Bin Liu från A*STAR Institute of Materials Research and Engineering, och kollegor vid National University of Singapore, har skapat nanopartiklar med två distinkta anticancerfunktioner och en avbildningsfunktion, allt stimuleras på begäran av en enda ljuskälla. Nanopartiklarna inkluderar också cellinriktningsegenskapen som är nödvändig för behandling och avbildning på rätt platser.
Systemet är byggt kring en polyetylenglykol-baserad polymer som bär en liten peptidkomponent som gör att den kan binda preferentiellt till specifika celltyper. Polymeren i sig fungerar som en fotosensibilisator som kan stimuleras av ljus för att frigöra reaktiva syrearter (ROS). Det bär också kemoterapiläkemedlet doxorubicin i en prodrug-form.
Polymerens naturliga fluorescens hjälper till med diagnos och övervakning av terapin eftersom den visar var nanopartiklar har samlats. ROS som genereras av ljusstimulering har en direkt "fotodynamisk" terapeutisk aktivitet, som förstör målcellerna. ROS bryter dessutom kopplingen mellan polymeren och doxorubicinet. Således, cancerceller kan utsättas för en tvådelad attack från ROS-terapin och kemoterapiläkemedlet som frigörs inom dem (se bild).
"Detta är den första nanoplattformen som kan erbjuda on-demand och bildstyrd fotodynamisk terapi och kemoterapi med utlöst läkemedelsfrisättning genom en ljusströmbrytare, " förklarar Liu, betonar systemets betydelse.
Forskarna visade kraften i deras plattform genom att applicera den på en blandning av odlade cancerceller, varav några överuttryckte ett ytprotein som kunde binda till målpeptiden på nanopartiklarna. Fluorescensavbildning indikerade att nanopartiklarna togs upp av målcellerna och att ROS och doxorubicin frisattes i dessa celler - allt i betydligt högre nivåer än i celler som användes som kontroller. Doxorubicinet som frisattes i cellcytoplasman kom lätt in i kärnan - dess aktivitetsställe. Avgörande, den kombinerade behandlingen hade en större cytotoxisk effekt än någon terapi ensam.
"Det vita ljuset som används i detta arbete penetrerar inte vävnaden tillräckligt för in vivo-applikationer, Liu förklarar, "men vi försöker nu använda nära-infrarött laserljus för att förbättra vävnadspenetrationen och gå mot on-demand cancerterapi." Hon föreslår också att med några ändringar, systemet kan vara lämpligt för diagnos och behandling av andra patologiska processer inklusive inflammation och HIV-infektion.