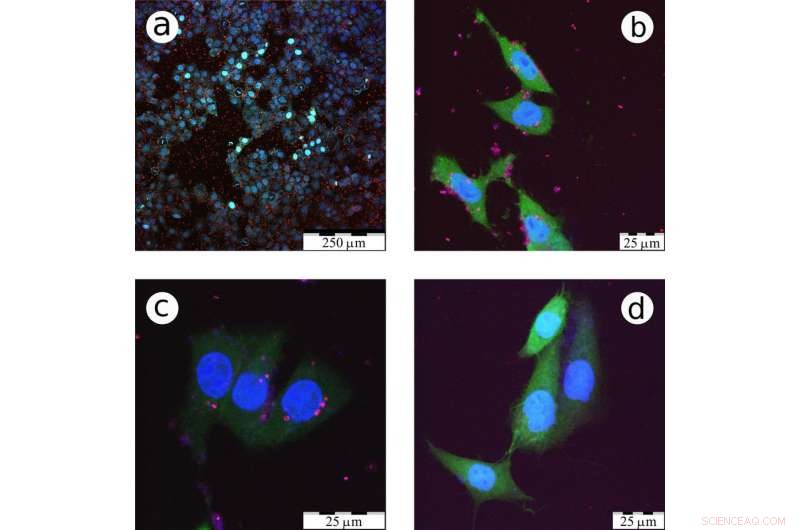
Dessa är konfokala fluorescensmikroskopbilder av CF2Th-cancerceller inkuberade med LA-Si NP. Kredit:Victor Timosjenko/ Vetenskapliga rapporter
En grupp ryska och franska forskare, med deltagande av forskare från Lomonosov Moscow State University, har syntetiserat nanopartiklar av ultrarent kisel som uppvisar effektiv fotoluminescens, sekundär ljusemission efter fotoexcitation. Dessa partiklar penetrerade lätt in i cancerceller för användning som självlysande markörer vid tidig diagnos och behandling av cancer. Studien publicerades i tidskriften Vetenskapliga rapporter .
Enligt medförfattaren Victor Timosjenko, tidigare försök i andra laboratorier var misslyckade, främst för att nanopartiklarna syntetiserades genom kemiska reaktioner i sura lösningar. "De erhållna partiklarna var inte tillräckligt rena, " säger han. "Biprodukter av de kemiska reaktionerna gjorde dem giftiga. Vidare, dessa nanopartiklar hade en form, som var långt ifrån en sfär, och det bidrar inte till utseendet på fotoluminescensen. Dessa två nackdelar begränsade kraftigt deras tillämpningar."
För att komma till rätta med dessa brister, forskarna använde en annan metod, så kallad laserablation, som skjuter ut atomer från målet med en laserstråle, så att de trasiga atomerna bildar en nanokristall. Problemet var att de sönderrivna atomerna i det här fallet ofta inte kombinerade med partiklar, men med några godtyckliga lager, och även om nanopartiklarna erhölls, de var inte fotoluminescerande. Antingen var nanopartiklarna för stora, eller så svalnade de för snabbt och hade inte tid att bilda nanokristaller av hög kvalitet. Således, det var nödvändigt att värma dem under en kort tid för att uppmuntra kristallisation.
"I det syftet, vi bestämde oss för att använda kort, högintensiva laserpulser, " säger professor Timosjenko. "De kastade inte bara ut kiselatomerna från målet, men dessutom joniserade dem. De emitterade elektronerna ledde till jonisering av heliumatomer som utgör atmosfären i vilken det förekom. Inom nanosekunder, laserplasma bildade de förhållanden som gjorde att atomerna kunde sintra till sfäriska nanokristaller. Dessa pärlor som faller på ytan samlas som ett fluffigt lager, som sedan kan dispergeras i vatten."
Dessa sfäriska nanopartiklar hade precis rätt storlek, två till fyra nanometer i diameter, vilket gav effektiv fotoluminescens där varje fallande foton balanserades med en utskjuten. I motsats till nanopartiklar erhållna genom kemisk etsning, de krävde inga giftiga tillsatser. Och viktigast av allt, som demonstrerats av biologiska experiment, de kunde lätt tränga in i cellerna. Dessutom, nanosfärerna penetrerade cancerceller mycket lättare än friska. Detta beror på att cancerceller alltid är redo att dela sig, och därmed absorbera allt för att producera dotterceller. Enligt Victor Timosjenko, beroende på typen av celler, cancerceller absorberar vanligtvis nanopartiklar 20 till 30 procent mer effektivt än friska, som ligger till grund för diagnostik av cancer i tidigt stadium.
"Vår främsta prestation var att producera nanopartiklarna och fastställa att de lätt tränger in i cancerceller, " Victor Timosjenko sa. "Problemet med diagnosen är en separat uppgift, som löstes samtidigt av biologer, med vårt deltagande. Du kan, till exempel, ersätta analysen av biopsi, ett ganska långt och opålitligt "ja-nej"-test, istället för att upptäcka om en nanopartikel penetrerade ett vävnadsprov eller inte. Det finns också icke-invasiva diagnostiska metoder. Det fotoluminescerande ljuset som emitteras från nanopartiklarna är i detta fall svårt att använda, men de kan aktiveras på andra sätt – t.ex. ultraljud eller radiofrekventa elektromagnetiska vågor."
Den största fördelen med nanopartiklarna är att de är helt ogiftiga och lätt utsöndras. De kan också binda till specifika ämnen eller biomolekyler (t.ex. antikroppar), tillåter läkare att rikta in dem på cancerceller och därigenom öka effektiviteten i diagnostiken. Enligt Victor Timosjenko, i framtiden kan dessa nanopartiklar också binda till läkemedel som inte bara kommer att upptäcka cancer, men också bedriva lokal kemoterapi eller strålbehandling på cellnivå.