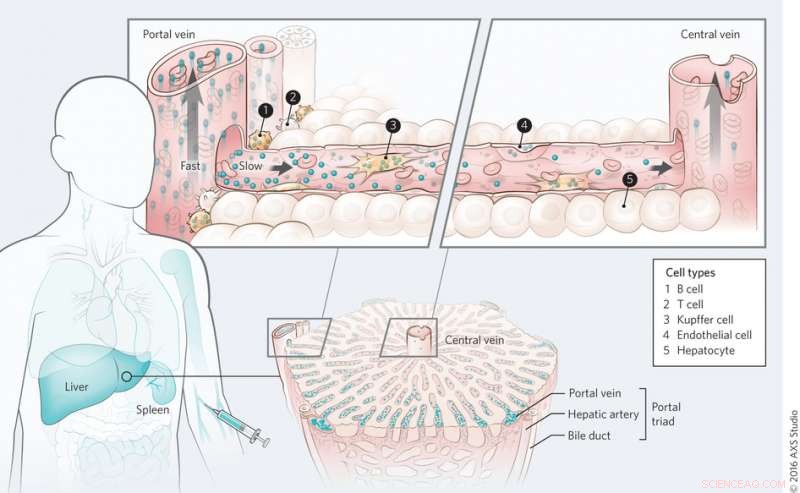
Mekanism för nanomaterialtransport i levern. Upphovsman:(c) Kim M. Tsoi, et al. Naturmaterial (2016) doi:10.1038/nmat4718
(Phys.org)—En av de största utmaningarna för att förverkliga potentialen hos riktade terapier är att förhindra att nanomaterial samlas i levern eller mjälten. Levern och mjälten är en del av det mononukleära fagocytsystemet. Dess uppgift är att filtrera gifter från blodomloppet. Tyvärr, i att göra sitt jobb, det hindrar också nanoterapier från att nå sitt mål.
För att övervinna detta hinder har en grupp forskare från flera institutioner i Toronto genomfört beräkningar på organnivå och underorgannivå, in vitro, och in vivo-studier med kvantprickar, guld nanopartiklar, och silikananopartiklar för att bättre förstå det mononukleära fagocytsystemet och mekanismen genom vilken nanopartiklar sekvestreras. De fann att blodflödet, cellulär fenotyp, och fysisk position i levern spelar alla en roll för nanopartikelupptaget. De föreslår att framtida arbete inte bara bör involvera nanopartikeldesign, men någon form av leverförkonditionering. Deras arbete visas i Naturmaterial .
Nanopartiklar kan funktionaliseras på ett sådant sätt att partikeln riktar sig mot en viss celltyp. Detta lovar mycket för cancer och andra riktade terapier. Dock, när nanoterapier testas i kroppen, nanopartikeln rensas från blodomloppet via det mononukleära fagocytsystemet (MPS). Detta gäller för alla typer av nanopartiklar.
Tsoi, et al. genomförde helorgan- och underorgananalyser för att bättre förstå hur MPS-systemet avlägsnar nanopartiklar. För sina experiment, de fokuserade på icke-nedbrytbara "hårda" nanopartiklar:kvantprickar, guld nanopartiklar, och nanopartiklar av kiseldioxid.
På hela orgelnivån, Tsoi, et al. fann att kvantprickar först rensas av cellerna nära portaltriaden och att det finns en clearancegradient genom leversinusformen under det första passet. Blod rinner in i levern genom portaltriaden och ut genom den centrala venen. Detta observerades också med guldnanopartiklar oavsett ytfunktionalisering, även om proteinadsorption tycktes spela en roll för nanopartikelupptag.
Nästa undersökningsområde är om blodflödeshastigheten spelar en roll vid lagring av nanopartiklar. Blodflödet saktar ner när det träffar levern (från 10-100 cm s -1 till 200-800 μm s -1 ). Tsoi, et al. utvecklat en matematisk modell för att beskriva blodflödet i levern och sannolikheten för nanopartikelbindning. De jämförde sedan sina beräkningsresultat med resultaten från cytometristudier med råttorna som behandlades med kvantprickar i testet för nanopartikelackumulering. I synnerhet, medan advektion är den dominerande inverkan på blodflödet i kroppen, diffusion är det dominerande inflytandet i levern. De fann att levern var 10 2 till 10 3 gånger mer sannolikt att binda nanomaterial och att partikelstorleken spelade en roll – ju större partikeln, desto mer sannolikt absorberades det av levern.
På underorgannivå, Tsoi, et al. tittat på vilka celltyper som spelar störst roll för nanopartikelupptaget. Studier för att fastställa cellupptaget av kvantprickar visade att Kupffer-celler adsorberade den största volymen kvantprickar, som förväntat. Dock, det som var överraskande var antalet partiklar som internaliserades av B-celler. B-celler verkar spela en mycket större roll i nanopartikelupptaget än vad man en gång trodde, även om Kupffer-celler fortfarande är nyckelcellerna för att ta bort nanopartiklar. Andra celltyper, inklusive endotelceller, spelade också en roll för att ta bort nanopartiklar.
Nästa, Tsoi, et al. testade om organarkitektur påverkar nanopartikelupptaget i levern genom att studera sekvestreringsprocessen i mjälten. De fann att av nanopartiklarna som togs bort av mjälten, nästan alla av dem var belägna i den röda massaregionen. Det är här blodflödet minskar jämfört med flödet i hela kroppen. Medan vissa nanopartiklar fanns i mjälten, mjältmakrofager internaliserade färre nanopartiklar än Kupffer-celler i levern. Detta bekräftades med jämförande in vitro- och in vivo -studier, och visar att organarkitektur celltyp spelar en roll i nanopartikelupptag.
Denna forskning ger viktiga insikter i hur man kan övervinna nanopartikelupptag av MPS. Typiskt fokuserar forskare på nanopartikeldesign, men den här studien tyder på att den kroppsliga miljön spelar en viktig roll vid lagring av nanopartiklar. Författarna föreslår att man manipulerar värdmiljön som en kompletterande strategi för optimering av nanopartiklar. Preliminära tester visar att två möjliga vägar är att ändra blodflödet genom levern och ändra fenotypen hos vissa celler så att de inte är benägna att ta upp nanomaterial.
© 2016 Phys.org