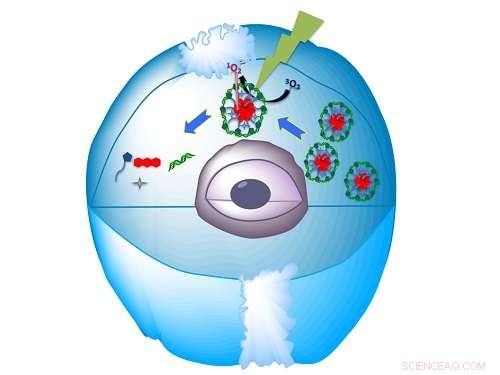
Det självmonterade biokompatibla nanomaterialet levererar miRNA in i cellen och släpper det sedan när det träffas av ljus. Kredit:KAUST
Ett litet terapeutiskt leveranssystem som kan kontrollera kroppens förmåga att tillverka proteiner har utvecklats av Saudiarabiens forskare från King Abdullah University of Science and Technology (KAUST).
Gener innehåller instruktioner för tillverkning av proteinerna som utgör vår kropp. Genetisk information översätts till de proteiner som behövs för att bygga levande celler genom en transkriptionsprocess där DNA:s genetiska kod kopieras till en stor molekyl som kallas budbärar-RNA (mRNA).
Denna transkriptionsprocess kan förändras genom att introducera korta dubbelsträngar av RNA, kallas litet interfererande RNA (siRNA), som binder till mRNA och hämmar uttrycket av särskilda gener. Att utnyttja denna RNA-interferens för terapeutiska tillämpningar är svårt och kräver ett material som kan skydda siRNA när det färdas genom blodomloppet, hjälper den att penetrera cellens yttre membran och leverera den till sin målplats.
"Leverans av RNA är mycket knepigt eftersom det lätt kan smältas av celler. Bättre vehiklar behövs så att mer RNA kan levereras för att redigera gener, "säger Niveen Khashab från KAUST Smart Hybrid Materials Laboratory.
Khashab och hennes kollegor har nu visat biokompatibla nanostrukturer för att leverera siRNA och effektivt tysta gener1. De kombinerade makromolekylen histidin-capped-9, 10-dialkoxi-antracen (HDA) och siRNA i vatten. De observerade självmontering av sfäriska nanopartiklar när vattnet var lätt surt, men inte när det var pH-neutralt.
Khashab förklarar att dessa nanosfärer skapas av den elektrostatiska interaktionen mellan den positivt laddade HDA och negativt laddade RNA, och sedan sveper de två långa armarna av HDA supramolekylärt siRNA för att skydda det.
"Vår organiska länkare kan interagera med genetiskt material genom vätebindningar och bilda en leveransvehikel, " förklarar Khashab. "Tillvägagångssättet är skalbart och skapar reproducerbara mängder av inkapslat RNA; det är också biokompatibelt och säkert."
Nanopartiklarna kunde också aktiveras med synligt ljus. När den bestrålas med grön strålning i närvaro av en sur fluorescerande förening, känd som eosin, sfären demonterar och frigör siRNA.
Teamet visade effektiviteten av nanopartikeln för läkemedelsleverans på B-cellslymfom 2, en mRNA -molekyl som skapar proteiner för att reglera celldöd. De visade att deras nanostrukturer förbättrar genljudseffekten och ledde till gennedbrytning av mer än 90 procent efter exponering för synligt ljus.
"Nästa steg är att justera designen för att leverera andra lastmolekyler som protein och förbättra ljusresponsen till högre våglängd i det nära infraröda, säger Khashab.