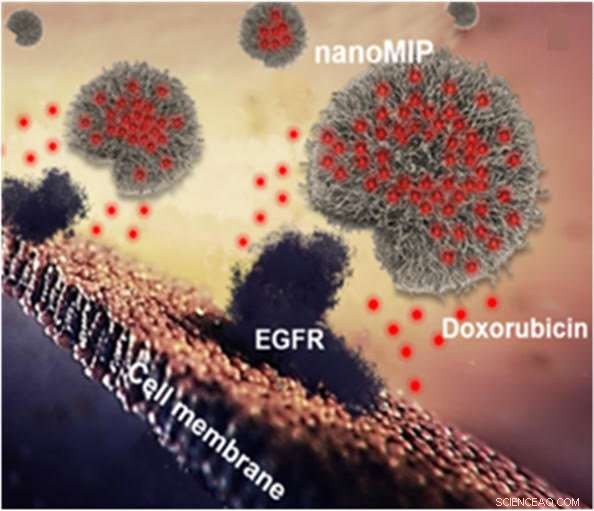
Figur 1. Syntetiska polymer -nanopartiklar, eller nanoMIP, binda till cellytan via den epidermala tillväxtfaktorreceptorn (EGFR). De röda prickarna representerar det cytotoxiska medlet doxorubicin, som levereras av nanoMIP och penetrerar cellmembranet. Upphovsman:F. Canfarotto et al./ Nano bokstäver
Ett gemensamt forskargrupp från Ryssland och Storbritannien har visat möjligheten att utveckla en ny typ av antineoplastiska läkemedel baserade på nanoMIP, eller "plastantikroppar". NanoMIP är syntetiska polymerer som kan fungera som antikroppar, selektivt bindande till målproteiner på ytan av cancerceller. Detta tillvägagångssätt kan leda till ett paradigmskifte i utvecklingen av nya metoder för cancerbehandling. Forskningen utfördes av ett internationellt team från University of Leicester, University College London, institutet för cytologi vid ryska vetenskapsakademien, och Moskva institutet för fysik och teknik. Resultaten av studien publicerades i Nano bokstäver .
De största nackdelarna med de flesta läkemedel mot cancer är deras låga specificitet och de därtill hörande biverkningarna. Konventionell kemoterapi riktar sig till alla delande celler utan undantag, så påverkas både friska celler och cancerceller.
Dock, framstegen inom cancerforskning har lett till en bättre förståelse av de molekylära mekanismerna och de primära agenterna som är ansvariga för tumörutveckling. Nya fynd har möjliggjort nya anti-neoplastiska läkemedel som kan skilja mellan friska och cancerceller genom att agera på specifika molekylära mål.
Eftersom cellerna i tumörer genomgår snabb uppdelning, de förlitar sig på en konstant tillgång på ämnen som stimulerar celltillväxt och proliferation. Dessa ämnen, känd som tillväxtfaktorer, komma utanför cellen, och kan identifieras med motsvarande receptorproteiner på cellytan. Dessa yttre faktorer aktiverar intracellulär signalering, stimulerar cancercellernas spridning. Det visade sig att receptorproteinerna på cellytan ofta överuttrycks - det vill säga syntetiseras i överskott - i olika fasta tumörer.
Under de senaste två decennierna har terapeutiska läkemedel som verkar på tillväxtfaktorer har utvecklats och kliniskt testats. De nya medicinerna undertrycker bindningen av tillväxtfaktorer till receptorerna, och direkt påverka deras enzymaktivitet. Det är inte förvånande att utvecklingen av nya syntetiska läkemedel mot denna typ av mål är ett lovande område inom molekylär farmakologi som lockar stor uppmärksamhet hos forskare över hela världen.
Den internationella forskargruppen som leds av professor Nickolai Barlev, chef för Laboratory of Cell Signaling Regulation vid MIPT, har visat att det är möjligt att utveckla en ny klass av antineoplastiska läkemedel baserade på ett slags partiklar som kallas nanosiserade molekylärt präglade polymerer (nanoMIP). NanoMIP är ett syntetiskt polymeralternativ till antikroppar med en 3D-struktur som gör att de endast kan binda till ett visst fragment av ett målprotein. Detta säkerställer deras höga specificitet. Till skillnad från antikroppar, nanoMIP kan också bära ytterligare anticancermedel. I sin forskning, författarna bevisade för första gången att det är möjligt att syntetisera nanoMIP som kan selektivt binda till aminosyrasekvenserna för deras målproteiner. Studien har också visat potentialen för nanoMIP -tillämpning vid riktad läkemedelsleverans (figur 2).
NanoMIP syntetiseras i närvaro av ett målprotein, som lämnar ett "märke" på nanopartikeln. Denna process kallas imprinting, och det kan jämföras med formgjutning - slutprodukten får formen av den ursprungliga mallen. Genom denna process, nanoMIP förvärvar förmågan att selektivt känna igen målmolekylen och binda till den.
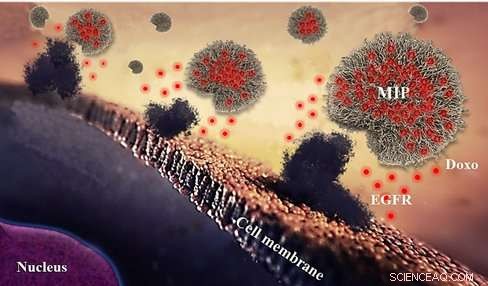
Figur 2. Syntetiska polymer -nanopartiklar, eller nanoMIP, binda till cellytan via den epidermala tillväxtfaktorreceptorn (EGFR). De röda prickarna representerar det cytotoxiska medlet doxorubicin, som levereras av nanoMIP och penetrerar cellmembranet. Upphovsman:Canfarotto et al./Nano Letters
Målet som används av studieförfattarna är den epidermala tillväxtfaktorreceptorn (EGFR). Detta protein överuttrycks i många typer av tumörer i samband med kolorektal, lunga, hjärn- och bröstcancer, inklusive dess mest aggressiva form, trippelnegativ bröstcancer. Av denna anledning, EGFR fungerade som ett av de första målen för antikroppsbaserade antineoplastiska läkemedel.
Teamet arbetade med nanopartiklar som erhållits med hjälp av en dubbelpräglad metod mot två målmolekyler:ett cytotoxiskt läkemedel som kallas doxorubicin och en linjär epitop av EGFR. (En epitop är den del av en målmolekyl som känns igen av antikroppen som binder till den.) Därför, den slutliga produkten både binder EGFR och levererar läkemedel till cancerceller.
"Även om de är effektiva vid klinisk användning, antikroppsbaserade läkemedel är svåra att utforma och dyra att producera. Tumörer med EGFR -överuttryck behandlas framgångsrikt med specifika monoklonala antikroppar riktade mot denna receptor (cetuximab, eller Erbitux). Dock, eftersom läkemedlet är instabilt, nya doser av antikroppar måste administreras under hela behandlingsperioden. Och den totala kostnaden för en terapikurs kan vara så hög som $ 100, 000. Alternativ för syntetiska antikroppar, såsom nanoMIP, har inte dessa begränsningar. Dessutom, till skillnad från biomolekyler, deras stabilitet beror inte på temperatur och surhet, vilket innebär att de har ett mycket bredare utbud av potentiella applikationer. Ser fram emot, de kan utöka utbudet av alternativ för diagnostik och behandling av många sjukdomar, säger Barlev, vem är seniorförfattare till studien.
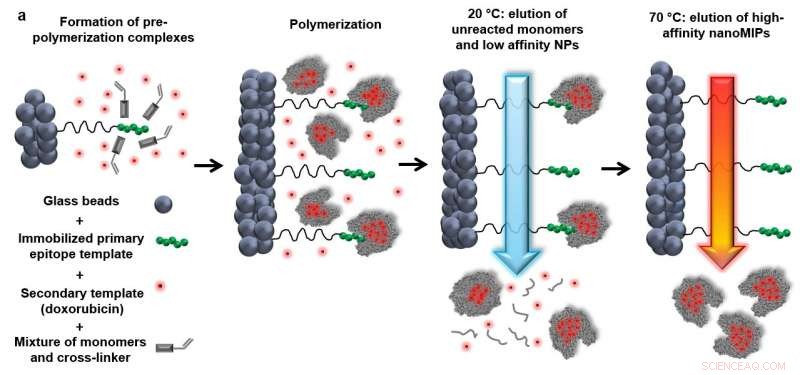
Figur 3. NanoMIP -syntes med ett EGFR -fragment immobiliserat på glaspärlor. Upphovsman:F. Canfarotto et al./Nano Letters
Vad är mer, syntesen av selektiva nanoMIP:er behöver inte nödvändigtvis prägla hela cellen. Snarare, bara en specifik del behöver präglas. Denna lilla del - en kort oligopeptid - fästs på glaspärlor via kovalenta kemiska bindningar. Pärlorna blandas sedan med akrylamidmonomerer och doxorubicin. Polyakrylamid, till skillnad från dess monomerer, är biologiskt ofarlig, och används för att producera mjuka kontaktlinser, bland annat. När temperaturen höjs, monomererna börjar polymerisera, bildar partiklar som är 100–200 nanometer stora, införliva doxorubicin, och bära ett molekylärt avtryck av målproteinet. Oreagerade monomerer och ospecifika nanopartiklar elueras, medan de syntetiserade "plastantikropparna" förblir bundna till glaspärlorna (figur 3).
"För första gången, Vi har tagit fram polyfunktionella nanoMIP som kan selektiva målproteinigenkänning och lämpar sig för specifik läkemedelsleverans. Det här var förr omöjligt, eftersom den tillgängliga tekniken för nanoMIP -syntes inte tillät oss att standardisera de förhållanden under vilka partiklarna erhölls, så slutproduktens effektivitet var oförutsägbar. Vi löste detta problem genom att använda fastfassyntes. Vårt nästa mål är att skapa ferromagnetiska nanoMIP, vilket avsevärt skulle utöka den diagnostiska och terapeutiska potentialen för våra plastantikroppar, Säger Barlev.
Resultaten av studien har också avslöjat måttlig och specifik toxicitet av nanopartiklar mot tumörceller. I synnerhet, toxiciteten berodde helt på att doxorubicin införlivades under polymerisationsprocessen, som kontrollnanopartiklar, som inte innehöll läkemedlet mot cancer, hade ingen effekt på cellerna. Dessutom, när terapeutiska nanoMIP administrerades, cellerna utvecklade flera DNA -brytningar, som är en karakteristisk reaktion på effekten av doxorubicin. Till sist, bindningen av "plastantikropparna" till EGFR ledde till en minskning av densiteten av receptorer på cellytan.
De potentiella terapeutiska effekterna av nanoMIP för behandling av EGFR-beroende tumörer kan slutligen hänföras till tre faktorer:den direkta cytotoxiska effekten av det anti-neoplastiska läkemedlet som levereras till cellen, maskeringen av receptorn från liganden, och minskning av EGFR -koncentration på cellytan. Framgångsrika in vitro -experiment tyder på att nanoMIPs lovar som fordon för riktad läkemedelsleverans och kräver ytterligare forskning.