
En falskfärgad skanningsmikroskopbild av en 10-FET transistoruppsättning. Röd:Silikonelastomer; Grön:PI; Ljusblå:SU8; Gult guld; Grå:Silikon. Kredit:Gu et al.
Djurceller kan använda element eller joner för att generera elektriska impulser. Dessa impulser överförs sedan från en cell till en annan och färdas över cellulära nätverk.
Förmågan att exakt registrera elektriska signaler som utbyts av celler kan hjälpa forskning och förbättra metoder inom många hälsorelaterade områden, inklusive kardiologi och neurologi. De flesta befintliga teknologier är dock begränsade både vad gäller avkänningsnoggrannhet och skalbarhet.
Forskare vid University of California San Diego har nyligen utvecklat en mycket känslig avkänningsenhet som kan användas för att registrera cellers elektriska signaler med större precision. Denna enhet, introducerad i en artikel publicerad i Nature Nanotechnology , består av flera sensorer, som tillsammans kan mäta utbredningen av elektriska signaler som utbyts av olika celler eller inuti individuella.
Den senaste studien leddes av Dr Yue Gu medan han arbetade i Prof. Sheng Xus labb vid UC San Diego. Dr Gu, är nu postdoktor vid Yale University.
"Etableringen av vår 3D-struktur, även känd som en "pop-up"-arkitektur, är baserad på en unik metod, den kompressiva buckling-tekniken som jag utvecklade under mina postdoktorala studier 2015, säger Prof. Xu, en av författarna till den senaste tidningen, berättade för Phys.org. "Den kompressiva bucklingstekniken drar fördel av konventionella och mångsidiga mikrotillverkningstekniker för renrum för att generera sofistikerade 3D-strukturer."
De 3D-popup-strukturer som används av Prof. Xu och hans kollegor kan byggas med ett brett utbud av material som är kompatibla med mikrotillverkningstekniker. Materialen de är gjorda av kan i sin tur bestämma deras funktion, vilket kan vara elektromagnetisk vågdämpning, mekanisk vibration, tryck- och töjningsavkänning eller elektrisk signalavkänning.

Fotografi av en 128-FET transistoruppsättning. Kredit:Gu et al.
I sin studie tänkte forskarna bygga dessa 3D-strukturer så att de kunde användas för att exakt spela in elektriska signaler som genereras och utbyts av celler. Deras huvudmål var att effektivt utnyttja mångsidigheten hos den kompressiva bucklingstekniken för att bygga en enhet som skulle samla in korrekta intra- och intercellulära inspelningar.
"Att bädda in halvledande material och tekniska transistorer i denna popup-arkitektur utökar tillämpningen av tekniken," förklarade Prof. Xu. "Vår beslutsamhet att tillämpa denna struktur på celler, särskilt hjärtmuskelceller, utlöstes av diskussioner som Dr Gu och jag hade med kardiologer och neurologer redan 2015, som klagade över svårigheterna med att registrera intracellulära signaler med hjälp av de befintliga verktygen, som t.ex. som patch-clamp, som är guldstandarden för inspelning av cellulära elektriska signaler."
Efter att de fick veta om de utmaningar som medicinska forskare upplevde när de försökte samla in exakta inspelningar av cellulära elektriska signaler, började Dr. Xu och Dr. Gu att experimentera med unika tekniska tillvägagångssätt som kunde förenkla deras arbete. I slutändan ledde detta till utvecklingen av den nya sensormatrisen som introducerades i deras senaste tidning.
"Ett annat mål med vår studie var implementeringen av intracellulära sensorer i 3D-konstruerade hjärtvävnader," sa prof. Xu. "Det är välkänt att de elektrofysiologiska egenskaperna hos celler varierar när de är i levande djur, isolerade från de levande djuren och odlade i skålar. Att registrera signalerna in vivo är alltid det viktigaste och ändå utmanande steget."
Prof. Xu och hans kollegor var de första som samlade in exakta intracellulära inspelningar av celler i den konstruerade hjärtvävnaden. Deras studie skulle alltså kunna vara ett första steg mot insamlingen av pålitliga, in vivo cellulära inspelningar.
"Cellmembranpotential som förspänner grindterminalen på enskilda transistorer resulterar i en förändring i strömmen från drain till source terminalen på transistorerna," förklarade prof. Xu. "Därför reflekterar strömfluktuationer de momentana membranpotentialerna. De multipla transistorerna i arrayen vi utvecklade kan samtidigt spela in signaler från olika positioner i en cell eller olika celler."
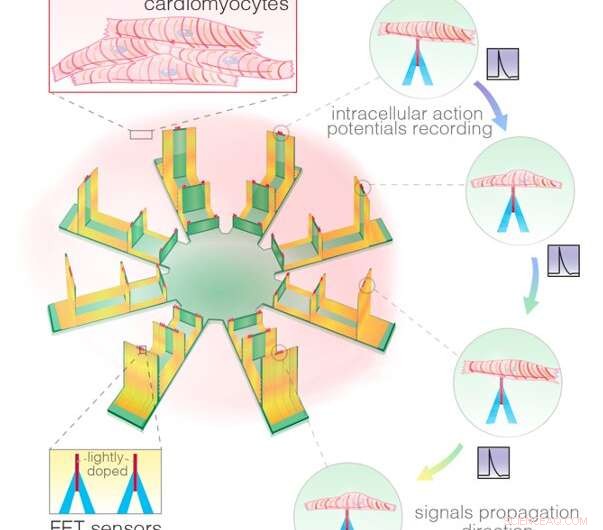
En schematisk bild visar den intracellulära avkänningen av en 128-FET transistoruppsättning och registrerar signalutbredning mellan celler. Kredit:Gu et al.
För att övervaka signalutbredningsbeteende inuti och mellan celler, sekvenserar forskarnas enhet signalerna som plockas upp av dess många transistorer. I motsats till andra tidigare föreslagna metoder för att samla in cellulära inspelningar, kan den nya enheten övervaka flera celler samtidigt. Dessutom kan dess transistorer behålla intakta cellmembranpotentialer med full amplitud utan att drabbas av dämpningar eller impedanser som är förknippade med den process genom vilken den kommer åt celler.
"Funktionaliserade transistorytor av fosfolipid-dubbelskiktsmaterial kan också kamouflera de oorganiska transistorerna till celler, vilket i hög grad underlättar deras införande i cellkroppen," förklarade Prof. Xu. "Under sådana förhållanden beskrivs internalisering som en spontan fusionsprocess, som lämnar minimal till och med ingen invasivitet till cellen."
Avkänningsenheten som utvecklats av prof. Xu och hans kollegor kan också övervaka den elektriska signalens ledningshastighet inuti en kardiomyocyt. Denna mätning kan vara av avgörande betydelse för kardiologernas arbete, eftersom en jämförelse med ledningshastigheten mellan närliggande celler kan hjälpa till att upptäcka och förstå vissa hjärtsjukdomar, inklusive hjärtfibros.
"Som en del av vår studie distribuerade vi transistormatrisen i 3D-hjärtvävnad och registrerade de intracellulära elektriska signalerna från enstaka celler för första gången," sa Xu. "I processen registrerade vi också ledning av elektriska signaler och beräknade deras hastighet."
Hittills har forskarna i första hand testat sin transistorbaserade avkänningsenhet på hjärtvävnad och uppnått mycket lovande resultat. Deras första resultat tyder på att det så småningom skulle kunna användas för att samla in exakta inspelningar av elektriska signaler som produceras och utbyts av celler, både i laboratoriemiljöer och in vivo, på hjärnan eller hjärtan hos levande djur eller mänskliga patienter.
"Vi strävar nu efter flera nya mål," tillade Xu. "Den första är att använda våra transistorer för att utföra in vivo-tester på intakta hjärtan eller hjärnor. Den andra är att registrera nervcellers intracellulära aktiviteter på olika neuronala platser. Slutligen, eftersom vissa endokrina celler också är elektrogena, vilket betyder att deras elektriska aktiviteter är relaterade till andra fysiologiska händelser, de är också av stort intresse." + Utforska vidare
© 2022 Science X Network