Vacciner och terapier baserade på budbärar-RNA skulle kunna levereras lättare tack vare en icke-toxisk polymer som skyddar RNA och kontrollerar dess frisättning inuti celler.
Tillkomsten av vacciner som använder budbärar-RNA (mRNA) för att styra immunogen proteinsyntes, mest känd i vacciner mot covid-19, stimulerar forskare att hitta bättre sätt att hålla mRNA stabilt och leverera det effektivt.
Ett team vid University of Tokyo, med samarbetspartners i Japan och Kina, har nu utvecklat polymerer som kan interagera med, stabilisera och innesluta mRNA, vilket möjliggör mycket effektiv leverans till odlade mänskliga celler och celler från levande möss. De har publicerat sitt arbete i tidskriften Science and Technology of Advanced Materials .
"Utöver vacciner för infektionssjukdomar, erbjuder mRNA lovande vägar för oöverträffade behandlingar som proteinersättningsterapier, genredigering och immunterapier", säger Horacio Cabral från University of Tokyo-teamet. "Men för att frigöra den fulla potentialen hos dessa avancerade terapier är utvecklingen av säkra och effektiva bärarsystem av största vikt."
Forskarna undersökte sätt att finjustera strukturen på sina polymermolekyler så att de kan interagera med mRNA för att skydda det. De biokompatibla och icke-toxiska polymererna var av en typ som kallas blocksampolymerer, byggda av alternerande segment av olika kemiska grupper, i detta fall polyetylenglykol och polyglycerol.
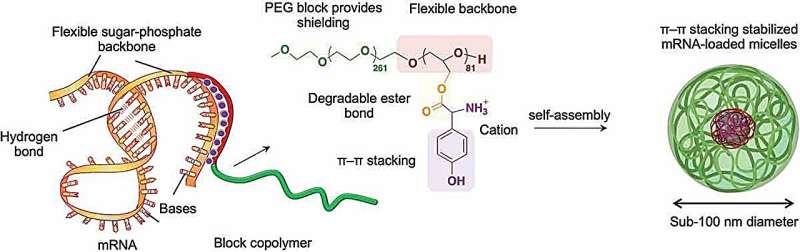
Men nyckeln till att uppnå lämplig interaktion med mRNA var att fästa specifika positivt laddade aminosyragrupper till den långa polymerryggraden. Den positiva laddningen lockar i allmänhet polymeren till negativt laddat RNA, och de valda aminosyrorna kunde också interagera med delar av mRNA i en process som kallas pi–pi (π–π) stapling. Detta involverar interaktioner mellan elektroner i en egenskap som kallas pi-bindningar i cykliska molekylära ringar staplade sida vid sida i de interagerande molekylerna.
"Detta är ett mycket anpassningsbart tillvägagångssätt som tillåter finjustering av vår polymers interaktioner med mRNA", säger Cabral. Som ett resultat stabiliserades mRNA:t mycket effektivt och övervann en stor nackdel med instabilitet som hittats med alternativa tillvägagångssätt.
Polymeren och mRNA:t sammanfogades spontant till sfäriska buntar - miceller - som effektivt levererade mRNA-lasten till odlade celler och även in i musceller efter intramuskulär injektion. mRNA:t frisattes lätt inuti celler för att generera proteinerna det kodade för med hög effektivitet och under en betydligt längre tid än alternativa tillvägagångssätt.
"Detta arbete var mycket utmanande på grund av den känsliga naturen hos mRNA, en mycket ömtålig molekyl som behöver skydd utanför målcellerna men omedelbar exponering för cellmaskineriet väl inuti", säger Cabral. Han tillägger, "Vår framgång är spännande på grund av dess potential att transformera mRNA-leveransteknologier, möjliggöra precis ingenjörskonst, innovativa frisättningsstrategier och övervinna kritiska barriärer för att förbättra stabiliteten och effektiviteten i mRNA-baserade terapier."
Mer information: Wenqian Yang et al, Blockkatiomerer med flankerande hydrolyserbara tyrosinatgrupper förbättrar in vivo mRNA-leverans via π–π staplingsassisterad micellär sammansättning, Science and Technology of Advanced Materials (2023). DOI:10.1080/14686996.2023.2170164
Journalinformation: Vetenskap och teknik för avancerade material
Tillhandahålls av National Institute for Materials Science