Proteinspjälkande enzymer spelar en viktig roll i många fysiologiska processer. Sådana proteaser är i allmänhet närvarande i ett inaktivt tillstånd och aktiveras endast under vissa förhållanden. Vissa är kopplade till sjukdomar som infektioner eller cancer, vilket gör det viktigt att ha metoder som selektivt kan detektera aktiva proteaser.
I en artikel publicerad i tidskriften Angewandte Chemie International Edition , har forskare introducerat en ny klass av proteasaktivitetssensorer:guldnanopartiklar utrustade med peptid-DNA.
Under ledning av Devleena Samanta och Anna Capasso (The University of Texas i Austin, USA), har teamet visat att dessa nanosonder kan känna av flera aktiva proteaser parallellt (multiplexmätning). Metoden fungerar vid rumstemperatur och kräver ingen komplicerad provberedning eller komplicerade instrument.
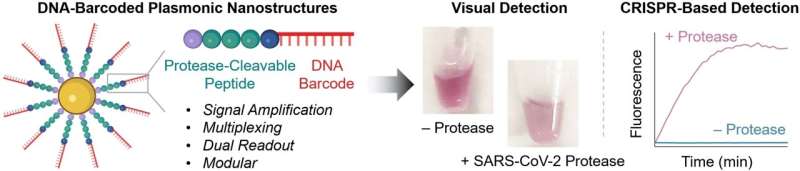
I kärnan av de nya sonderna finns guldnanopartiklar utrustade med kedjor gjorda av en peptid och ett DNA-fragment. Peptidstrukturen är designad att vara en som delas av proteaset som detekteras. DNA:t fungerar som en unik streckkod för att identifiera peptiden och förstärker även signalen. Om det önskade proteaset är närvarande i sin aktiva form i provet delar peptiden det. Detta frigör DNA-streckkoden i lösningen, där den kan detekteras baserat på dess sekvens.
För att utföra denna upptäckt använder teamet ett CRISPR/Cas12a-test:enzymet Cas12a är bundet till ett guide-RNA (gRNA) för att bilda ett inaktivt komplex. gRNA:t innehåller ett segment som specifikt binder till streckkodens DNA. Detta aktiverar Cas12a, så att det nu kan "klippa upp" enkelsträngat DNA (ssDNA).
För testet lägger forskarna till ssDNA-molekyler med en fluorescerande grupp (fluorofor) i ena änden och en släckare, som "stänger av" fluorescensen hos fluoroforen (så länge de är tillräckligt nära), i den andra. Om ssDNA skärs upp, flyttar fluoroforen och släckaren längre isär. Detta resulterar i stark fluorescens som indikerar att proteaset som testas för är närvarande (detektionsgräns på cirka 58 pM).
Om inga instrument finns tillgängliga på plats och testet måste gå snabbt är det möjligt att detektera med blotta ögat:om proteaset delar peptiden på sonden förändras guldnanopartiklarnas ytladdning och de aggregerar. Färgen på dessa så kallade "plasmoniska nanostrukturer" beror avsevärt på deras aggregeringsgrad. Det är möjligt att detektera nanomolära proteaskoncentrationer baserat på färgförändringen i testlösningen.
Multiplex detektering av proteaserna 3CL och caspase3 gjorde att teamet kunde demonstrera den höga känsligheten och selektiviteten hos deras nya metod. 3CL är en markör för aktiv coronavirusinfektion och covid-patienter har ofta också förhöjd aktivitet av apoptosmarkören caspase3. Den kliniska potentialen för detta test visades också genom detektering av cathepsin B, ett proteas relaterat till kolorektal cancer, i tre olika tumörcellinjer erhållna från patienter.
Dessa nanoprober ger 100 gånger högre fluorescenssignaler jämfört med kommersiella fluorescensbaserade proteassensorer. Dessutom kan praktiskt taget vilket proteas som helst detekteras om peptiden det delar är känd. Tillsammans kan dessa nanosonder potentiellt möjliggöra tidig upptäckt av sjukdomar och förbättra precisionen och tillförlitligheten för diagnostiska tester genom multiplexering.
Mer information: Subrata Pandit et al, DNA-streckkodade plasmoniska nanostrukturer för aktivitetsbaserad proteasavkänning, Angewandte Chemie International Edition (2023). DOI:10.1002/anie.202310964
Journalinformation: Angewandte Chemie International Edition
Tillhandahålls av Wiley