Hälsovårdsrelaterade infektioner är ett vanligt problem vid suppurerande sårvård, liksom ökningen av multiresistenta bakterier. För att effektivt och selektivt kunna bekämpa bakterieinfektioner har ett team av forskare utvecklat ett bakteriedödande nanomaterial utrustat med en fotokemisk "ljusomkopplare" som kan riktas mot antingen grampositiva eller gramnegativa bakterier.
Som laget rapporterar i sin studie publicerad i Angewandte Chemie , kan dess effektivitet mot MRSA utökas till andra selektiva bakterieinfektioner.
Antibiotikaresistenta infektioner har blivit ett akut folkhälsoproblem, särskilt på sjukhusmiljöer. Många av de aktuella bakteriearterna är utbredda i naturen, men kan orsaka mycket allvarligare, ibland obehandlade, infektioner hos patienter med nedsatt immunförsvar.
Baktericida material erbjuder ett nytt tillvägagångssätt för att bekämpa vårdrelaterade infektioner som inte är beroende av antibiotika. Mrinmoy De och kollegor från Indian Institute of Science i Bengaluru, Indien, har nu lyckats producera ett UV-synligt-ljusreagerande nanomaterial som kan ställas om för att rikta in sig på antingen Gram-positiva eller Gram-negativa bakterier.
Båda bakterietyperna har mycket olika struktur och sammansättning av yttre membran. Grampositiva bakterier, inklusive meticillinresistenta Staphylococcus aureus (MRSA), har ett bakteriemembran som huvudsakligen består av peptidoglykaner.
Däremot har gramnegativa bakterier, inklusive Pseudomonas aeruginosa, en annan sjukvårdsassocierad bakterie med problematisk resistens mot bredbandsantibiotika, både inre och yttre membran som huvudsakligen består av fosfolipider med ett tunt peptidoglykanskikt. "Det är viktigt att uppnå stamselektiv bakteriedödande aktivitet", säger De.
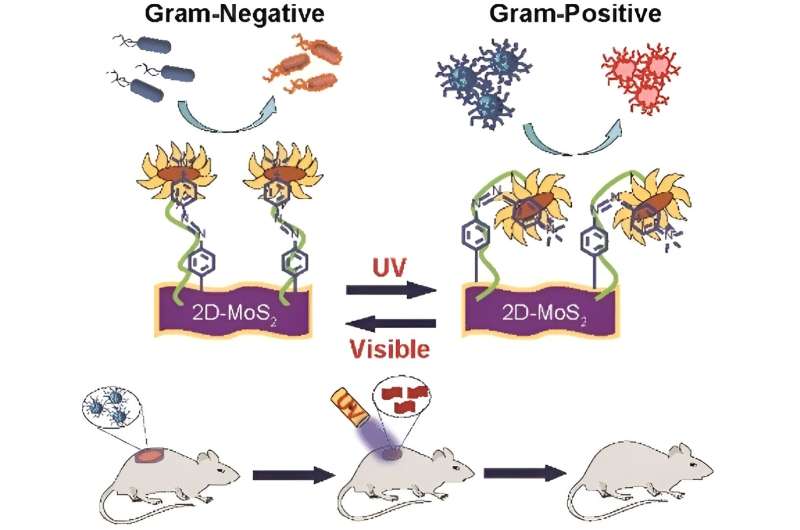
För att uppnå ett bakteriedödande medel som selektivt kan interagera med båda kemiska ytorna, designade teamet ett funktionaliserat nanomaterial tillverkat av molybdendisulfid (MoS2 med azobensendelar till vilka positivt laddade kvartära aminogrupper var fästa. Medan MoS2 är en baktericid och de kvartära aminogrupperna tillåter membrandepolarisering, introducerar azobensenenheterna en ljusdriven switch i nanostrukturen från en långsträckt trans till en krökt cis-form för att skapa selektiva ytinteraktioner.
Teamet använde flera kemiska sonder och optiska mätningar för att fastställa att både cis- och trans-formerna av nanomaterialet dödade bakterier, om än på väldigt olika sätt.
För den gramnegativa P. aeruginosa depolariserade transformen bakteriemembranet och genomborrade det ordentligt. Detta tillät MoS2 nanomaterial för att generera intracellulära reaktiva syrearter och döda bakterierna. Omvänt svarade den grampositiva MRSA-stammen på cis-formen mer effektivt. I det här fallet var cellväggen skadad och sprucken av specifika interaktioner.
Genom att helt enkelt "vända" UV-omkopplaren från trans-grundtillståndet till cis-tillståndet kunde teamet kontrollera selektiviteten för båda bakterietyperna. De visade effekten av deras nanomaterial genom att framgångsrikt läka MRSA-infekterade sår i mössmodeller. Såren stängdes helt efter 10 dagar när de behandlades med cis-reagenset, snabbare än den vanliga antibiotikabehandlingen med vankomycin.
Mer information: Jagabandhu Sahoo et al, Photo-Controlled Gating of Selective Bacterial Membrane Interaction and Enhanced Antibacterial Activity for Wound Healing, Angewandte Chemie International Edition (2023). DOI:10.1002/anie.202314804
Journalinformation: Angewandte Chemie International Edition , Angewandte Chemie
Tillhandahålls av Wiley