Forskare från Northwestern Medicine har utvecklat ett mer effektivt sätt att skapa nanoterapeutiska vacciner och läkemedel, enligt en ny studie publicerad i ACS Nano .
"Under det senaste decenniet har teknologin för sfärisk nukleinsyra, eller SNA, vuxit fram som en bred terapeutisk plattform för en mängd olika sjukdomar, inklusive cancer och andra sjukdomar", säger Chad Mirkin, Ph.D., professor i medicin vid avdelningen i hematologi och onkologi, George B. Rathmann professor i kemi vid Northwesterns Weinberg College of Arts and Sciences och chef för International Institute for Nanotechnology, som var huvudförfattare till studien.
I Mirkin-laboratoriet har utredare utnyttjat denna SNA-teknik i sitt arbete med att designa precisionsnanomediciner för användning i genreglering och cancerimmunterapi med begränsade oönskade biverkningar genom en systematisk utvecklingsprocess som kallas rationell vaccinologi.
"I utvecklingen av vacciner har historiskt sett väldigt lite uppmärksamhet ägnats åt vaccinets struktur", säger Mirkin, som också är medlem i Robert H. Lurie Comprehensive Cancer Center vid Northwestern University. "All tonvikt har lagts på komponenterna. Utgångspunkten för rationell vaccinologi är att även om komponenter är kritiska är strukturen lika viktig. Hur du presenterar vaccinkomponenter inom en modulär nanoskalaarkitektur kan ha en dramatisk inverkan på vaccinets effektivitet, oavsett om det är behandling av infektionssjukdomar eller cancer."
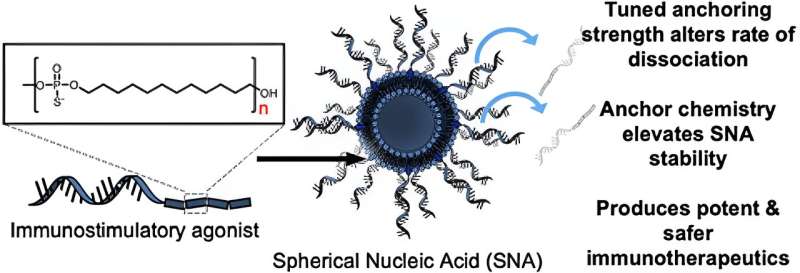
I studien testade utredarna först effekterna av att använda olika kemiska förankringsgrupper för att fästa oligonukleotiderna - korta strängar av DNA eller RNA - till ytan av liposomerna för att förbereda SNA. De fann att när alltmer hydrofoba dodekanbaserade förankringsgrupper användes, förbättrades nanostrukturens stabilitet avsevärt. När de introducerades till benmärgshärledda dendritiska celler från möss, uppvisade dessa mer stabila SNA-konstruktioner förbättrat cellulärt upptag jämfört med andra versioner av SNA som framställdes med andra typer av förankringsgrupper, med olika kemi.
"Vi upptäckte ett sätt att förankra oligonukleotiderna till ytan av partikeln som förändrar den övergripande stabiliteten hos SNA-konstruktionen, vilket är avgörande", säger Jasper Dittmar, en Ph.D. student i Mirkinlaboratoriet och medförfattare till studien. "Det fina med SNA-arkitekturen är att den känns igen av nästan alla celltyper, inklusive immunceller, och snabbt internaliserad. Du får vaccinet att komma in i cellerna som spelar roll vid den stökiometri du vill ha, med önskat antal antigener och adjuvansmolekyler."
Forskare i Mirkin-labbet laddade sedan SNA-vaccinet med OVA1 (en modellpeptid som härrör från äggprotein som ofta används vid vaccinutveckling) och administrerade det till möss med lymfom. De OVA1 SNA-behandlade mössen hade inte bara ett större antal polyfunktionella T-celler (som anses vara potenta mot kroniska infektioner och tumörer), de visade också en 21-faldig minskning av tumörvolymerna jämfört med saltlösningsbehandlade möss, enligt studera.
För att bedöma de inflammatoriska biverkningarna av vaccinet studerade forskarna sedan SNA för att se om det aktiverade överdrivet immunsvar hos möss. Möss som fick behandlingen producerade ingen cytokinstorm, en ibland dödlig bieffekt av immunterapier.
Eftersom cytokinstormar är förknippade med allvarliga fall av covid-19, skapade Mirkin och hans forskargrupp också ett SNA-vaccin där OVA1-peptiden byttes ut mot en peptid från viruset som orsakar covid-19 (CoV-peptid) och administrerade den till människor celler och i slutändan möss. Utredarna fann att vaccinet förbättrade antigenspecifika, anti-COVID-immunsvar med minimala negativa biverkningar.
"Sammantaget lägger resultaten av denna studie en grund för ett nytt sätt att utveckla och leverera vacciner och andra precisionsbehandlingar, oavsett målsjukdomen", säger Michael Evangelopoulos, en Ph.D. student i Mirkin-labbet och medförfattare till studien.
Resultaten visar också vikten av vaccinkonstruktion, sa Mirkin.
"Struktur spelar roll," sa Mirkin. "På ett område där vi har ägnat väldigt lite tid åt att fokusera på strukturen av vacciner, kan vi ha saknat skogen för träden. Det är en kombinerad förståelse av komponenterna och den strukturella presentationen som leder till en effektiv medicin eller inte ."
Framöver kommer Mirkin-gruppen att fortsätta att ta fram olika konfigurationer av SNA-vacciner för att bedöma vilka som är mest effektiva, sa han.
"Vi spenderar mycket tid på att använda SNA-plattformen för att ta reda på de strukturer som är mest effektiva, och sedan försöka ta reda på varför det är, vad som fungerar och sedan också varför det fungerar," sa Mirkin. "Vi tror att genom att göra det kommer vi att kunna skapa en helt ny generation av läkemedel baserade på detta koncept av rationell vaccinologi."
Mer information: Jasper W. Dittmar et al, Tuning DNA Dissociation from Spherical Nucleic Acids for Enhanced Immunostimulation, ACS Nano (2023). DOI:10.1021/acsnano.3c04333
Journalinformation: ACS Nano
Tillhandahålls av Northwestern University