Utredare vid Icahn School of Medicine vid Mount Sinai har utformat en innovativ RNA-baserad strategi för att aktivera dendritiska celler – som spelar en nyckelroll i immunsvaret – som utrotade tumörer och förhindrade att de återkommer i musmodeller av melanom.
Fynden, som tyder på att tillvägagångssättet har potential att vara effektivt mot tumörer som redan har spridit sig till andra delar av kroppen och mot olika cancertyper, rapporterades i 27 juli-numret av Nature Nanotechnology .
Cancerceller använder strategier för att stänga av olika stadier av cancer-immunitetscykeln, den process genom vilken dendritiska celler utbildar T-celler att döda cancerceller. Denna immunsuppressiva miljö som hindrar aktivering av cancerdödande T-celler tillåter tumörer att växa, säger forskarna.
"De flesta tillvägagångssätt för att förstärka denna kritiska roll för dendritiska celler - eller adoptiv cellterapier - syftar till att öka aktiveringssignalerna som ges till dendritiska celler när specifika molekyler på deras yta binder till tumörceller. Dessa har dock inte varit lika framgångsrika i kliniska prövningar som hoppades detta beror på att tumörer har en tendens att utvecklas på olika sätt för att stänga av varje stadium av cancer-immunitetscykeln, säger Yizhou Dong, Ph.D., motsvarande författare till studien.
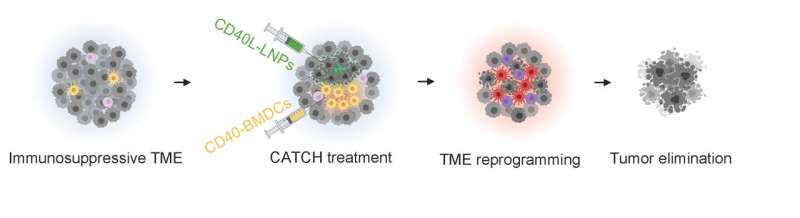
Forskarna döpte sin metod till CATCH. Som en del av regimen använde forskarna nya typer av lipidnanopartiklar för att leverera två mRNA-terapier - en process som liknar den som framgångsrikt används för COVID-19-vacciner - för att säkerställa att de dendritiska cellerna var tillräckligt aktiverade för att förbättra cancer-immunitetscykeln i etablerade tumörer.
Genom att använda flera bioanalyser för att få insikter om effekterna av CATCH-regimen på olika typer av immunceller, visade forskarna att deras strategi inte bara återaktiverade cykeln utan också tog bort hinder i andra stadier. Detta orsakade en förändring i tumörens mikromiljö, vilket förändrade den från att ha celltyper som försvagar T-cellers förmåga att bekämpa cancer till att ha celltyper som faktiskt stöder och förbättrar deras förmåga att bekämpa tumörer.
Utöver de positiva fynden i mössmodeller av melanom, genomförde forskarna ytterligare tester för att utvärdera effektiviteten av CATCH-kuren för att återuppta cancerimmunitetscykeln mer brett. Deras undersökningar visade uppmuntrande resultat, eftersom behandlingen minskade tumörer i musmodeller av B-cellslymfom med 83 %. De testade det också i mössmodeller av bröstcancer, där ungefär hälften av mössen svarade positivt.
Därefter planerar forskarna genomförbarhets- och säkerhetstester för användning av CATCH-regimen i tidig fas av kliniska prövningar för patienter.
"Dendritiska celler har varit ett nyckelfokus för utvecklingen av nya cancerterapier eftersom dessa celler organiserar cancer-immunitetscykeln. I teorin har CATCH-regimen som använder denna speciella RNA-baserade teknologi potential att ge ett mycket mer effektivt tillvägagångssätt för att använda dendritiska celler för cancerimmunterapi för att behandla ett brett spektrum av solida tumörer", säger Brian Brown, Ph.D., chef för Icahn Genomics Institute och biträdande direktör för Marc och Jennifer Lipschultz Precision Immunology Institute vid Icahn Mount Sinai.
Uppsatsen har titeln "Stäng cancer-immunitetscykeln genom att integrera lipid nanopartikel-mRNA-formuleringar och dendritisk cellterapi."
Mer information: Stäng cancer-immunitetscykeln genom att integrera lipid-nanopartikel-mRNA-formuleringar och dendritisk cellterapi, Nature Nanotechnology (2023). DOI:10.1038/s41565-023-01453-9. www.nature.com/articles/s41565-023-01453-9
Journalinformation: Nanoteknik
Tillhandahålls av Mount Sinai Hospital