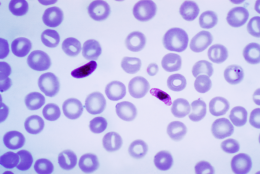
Detta mikrofotografi av ett blodutstryk innehåller en makro- och mikrogametocyt av parasiten Plasmodium falciparum. Kredit:Wikipedia.
Forskare vid University of California San Diego School of Medicine, med kollegor över hela landet och runt om i världen, har använt helgenomanalyser och kemogenetik för att identifiera nya läkemedelsmål och resistensgener i 262 parasitcellinjer av Plasmodium falciparum —Protozopatogener som orsakar malaria — som är resistenta mot 37 olika antimalariaföreningar.
Studien, publicerades i numret 12 januari av Vetenskap , bekräftade tidigare kända genetiska modifieringar som väsentligt bidrar till parasiternas läkemedelsresistens, men avslöjade också nya mål som fördjupar förståelsen för parasiternas underliggande biologi.
"Denna utforskning av P. falciparum resistome – samlingen av antibiotikaresistensgener – och dess läkemedelsbara genom kommer att hjälpa till att vägleda nya läkemedelsupptäcktsinsatser och främja vår förståelse av hur malariaparasiten utvecklas för att slå tillbaka, " sa seniorförfattaren Elizabeth Winzeler, PhD, professor i farmakologi och läkemedelsupptäckt vid avdelningen för pediatrik vid UC San Diego School of Medicine.
P. falciparum är en encellig protozo som överförs till människor genom bett av infekterade Anopheles-myggor. Det är ansvarigt för ungefär hälften av alla malariafall. Malarias enormt oproportionerliga inverkan på människors hälsa – Världshälsoorganisationen uppskattar att det fanns 216 miljoner fall över hela världen och 445, 000 dödsfall under 2016 – beror delvis på parasiternas speciella skicklighet att ändra genom för att undvika och motstå läkemedelsbehandling och det mänskliga immunsystemet.
"En enda mänsklig infektion kan resultera i att en person innehåller uppemot en biljon asexuella parasiter i blodstadiet, ", sa Winzeler. "Även med en relativt långsam slumpmässig mutationshastighet, dessa siffror ger extraordinär anpassningsförmåga. På bara några få replikeringscykler, de P. falciparum genomet kan förvärva en slumpmässig genetisk förändring som kan göra minst en parasit resistent mot aktiviteten hos ett läkemedel eller en antikropp som kodas av människor."
En sådan snabb utveckling innebär betydande utmaningar för att kontrollera sjukdomen, sa forskare, men det kan också utnyttjas in vitro att dokumentera exakt hur parasiten utvecklas i närvaro av kända antimalariamedel för att skapa läkemedelsresistens. Det kan också användas för att avslöja nya läkemedelsmål.
Snarare än att fokusera på interaktionen mellan parasiter och enskilda föreningar eller undersöka enstaka misstänkta gener i P. falciparum , Winzeler och kollegor använde helgenomsekvensering och en mångsidig uppsättning antimalariaföreningar. Den resulterande datamängden avslöjade en mångfald av mutationer. Resistenta parasiter innehöll ofta en mutation i en presumtiv målgen och ytterligare mutationer i andra, orelaterade gener.
"Våra resultat visade och underströk den utmanande komplexiteten hos utvecklad läkemedelsresistens i P. falciparum , sa Winzeler, "men de identifierade också nya läkemedelsmål eller resistensgener för varje förening för vilken resistenta parasiter genererades. Det avslöjade det komplicerade kemogenetiska landskapet hos P. falciparum , men gav också en potentiell guide för att designa nya små molekylhämmare för att bekämpa denna patogen."