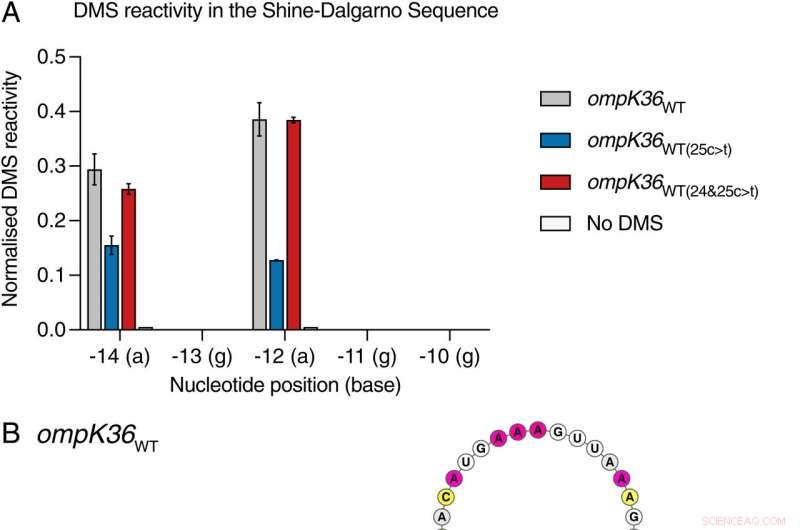
Position 25 i ompK36WT(25c> t) RNA inducerar en stam som involverar SDS. (A) Side-by-side normaliserad DMS-signal per nukleotid i SDS från fullängds in vitro-transkriberad och återvikt ompK36WT , ompK36WT(25c> t) , ompk36WT(24&25c> t) , och DMS-obehandlad ompK36WT . Högre värden motsvarar ökad bastillgänglighet. DMS-signal (± SD) av 2 biologiska upprepningar för nukleotider -14a till -10g visas. (B–D). DMS-begränsade strukturmodeller av 5′-änden av ompK36WT (B), ompK36WT(24&25c> t) (C) och ompK36WT(25c> t) (D). Nukleotider färgas av normaliserad DMS-signal. SDS i RNA-strukturer är markerade i grått. Pilar indikerar −14-positionen och 25c> t-positionen i ompK36WT(25c> t) . Kredit:Proceedings of the National Academy of Sciences (2022). DOI:10.1073/pnas.2203593119
Forskare har upptäckt ett nytt sätt att sjukhusförvärvade infektioner motstår antibiotika, genom en "tyst" genetisk mutation.
Bakterier kan förvärva resistens mot antibiotika genom slumpmässiga mutationer i deras DNA som ger dem en fördel som hjälper dem att överleva. Att hitta genetiska mutationer och upptäcka hur de hjälper bakterier att överleva antibiotikaangrepp är nyckeln till att hjälpa oss slå tillbaka med nya läkemedel.
Forskarna har nu upptäckt en "tyst" mutation i den genetiska koden som leder till antibiotikaresistens. Vanligtvis skulle mutationer av detta slag förbises, och de kan redan finnas i andra smittsamma bakterier.
Teamet, ledd av forskare vid Imperial College London och inklusive internationella medarbetare, publicerade sina resultat idag i tidskriften Proceedings of the National Academy of Sciences .
Stigande motstånd
Forskarna tittade på bakterien Klebsiella pneumoniae, som orsakar infektioner i lungor, blod och sår hos patienter på sjukhus, där patienter som har nedsatt immunförsvar, som de på intensivvårdsavdelningar, är särskilt sårbara.
Liksom många bakterier blir K. pneumoniae alltmer resistenta mot antibiotika, särskilt en familj av läkemedel som kallas karbapenemer. Dessa viktiga läkemedel som sista utväg används på sjukhus när andra antibiotika redan har misslyckats.
Eftersom ökad resistens mot karbapenemer dramatiskt kan påverka vår förmåga att behandla infektioner, klassificeras karbapenemresistenta K. pneumoniae som "kritiska" organismer från Världshälsoorganisationen Priority 1.
För att vara effektiva behöver antibiotika komma in i bakterier och vid K. pneumoniae sker detta via en kanal i bakteriens yttre membran, bildad av ett protein som heter OmpK36. Teamet upptäckte en genetisk mutation som gör att bakterierna producerar mindre av proteinet, vilket effektivt stänger några av dessa kanaler och håller karbapenemantibiotika ute.
"Tysta" mutationer
Denna mutation fungerar dock annorlunda än standardmutationer som resulterar i antibiotikaresistens. Vanligtvis ändrar mutationer den genetiska koden så att när den "läses" av ribosomer och omvandlas till ett protein, producerar den en annan kedja av aminosyror med olika funktioner.
Denna mutation producerar fortfarande samma aminosyrakedja, men förändrar strukturen hos en viktig mRNA-mellanprodukt, vilket förhindrar att ribosomer läser koden och producerar protein från den.
När man letar efter mutationer söker genomiska tekniker vanligtvis efter förändringar i aminosyrasekvensen. Men eftersom denna mutation förändrar en struktur, snarare än själva sekvensen, kan den ses som en "tyst" mutation.
Första författaren Dr. Joshua Wong, från Institutionen för livsvetenskaper vid Imperial, sa:"I en tid av big data och genomik kan mutationer som vi har upptäckt anses vara "tysta" eftersom den genetiska koden resulterar i samma proteinsekvens .
"Denna upptäckt borde förändra hur vi ser på den genetiska koden i bakterier och indikerar potentiellt att vi i forskarsamhället har förbisett andra liknande mutationer som kan ha viktiga effekter. Vårt arbete fokuserar på en enda mutation men förändrar i grunden hur vi tolkar mutationer, särskilt de som ansågs vara tysta."
Drift av antibiotikaanvändning
Teamet vid Imperial, som karakteriserade mutationen, arbetade med team vid University of Oxford, University of Florence och Harvard University för att identifiera distributionen av mutationen globalt, bedöma resistensnivåer och för att bestämma hur mutationen påverkade det mellanliggande mRNA:t struktur.
Med hjälp av data från resistenta bakterieprover som samlats in globalt visade teamet att mutationen hade uppstått flera gånger oberoende av varandra. Detta tyder på att det inte är slumpmässigt, utan istället drivs av bakteriernas behov av att försvara sig igen antibiotikan.
Ledande forskare professor Gad Frankel, från Institutionen för livsvetenskaper vid Imperial, sa:"Mutationen har utvecklats vid flera tillfällen oberoende av varandra, och detta säger oss att denna nya mekanism inte är en engångsföreteelse, utan istället driven av antibiotikakonsumtion. Detta tyder på att mutationen sker under antibiotikatryck och framhäver biverkningarna av överdriven antibiotikaanvändning på sjukhus och andra miljöer."
Teamet hoppas nu att deras upptäckt kommer att införlivas i bioinformatiska verktyg som analyserar genetiska sekvenser för att identifiera närvaron av mutationen, vilket gjordes med en tidigare mekanism som teamet upptäckte.
De kommer också att fortsätta att arbeta med sina medarbetare för att leta efter andra viktiga mutationer i denna nyckelpatogen. + Utforska vidare