En grupp forskare har utökat den konventionella kunskapen om ett kritiskt enzym som styr cellmigration. I en publikation i tidskriften Nature Communications , rapporterade de att fosfoinositid 3-kinas (PI3K) inte bara fungerar som en accelerator för att stimulera cellmotilitet, utan den har också en inbyggd bromsmekanism som hindrar migration.
"PI3K är ett viktigt signaleringsenzym som har studerats omfattande i över 30 år på grund av dess roller i grundläggande cellulära funktioner som tillväxt, överlevnad, rörelse och metabolism", säger Hideaki Matsubayashi, huvudförfattare till studien och biträdande professor vid Tohoku University's Frontier Forskningsinstitutet för tvärvetenskapliga vetenskaper (FRIS).
"Det spelar en kritisk roll i cellmigration och invasion, något som, när det är dysregulerat, kan orsaka många patologier. Vårt arbete avslöjade att PI3K också aktivt kan begränsa samma migrationsprocesser genom en separat icke-katalytisk endocytisk mekanism som härrör från dess p85β-subenhet. "
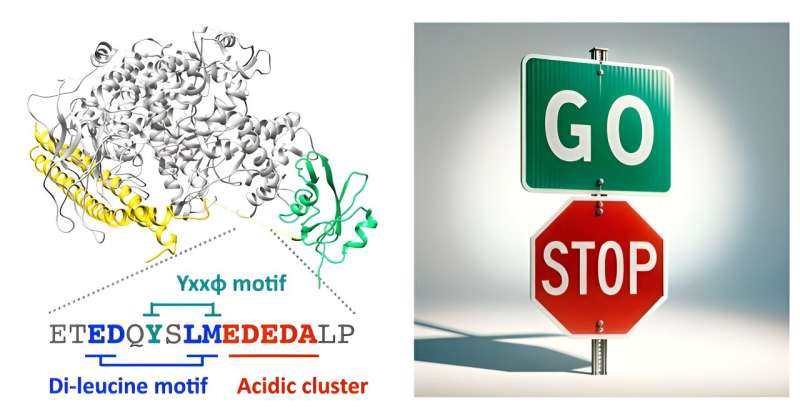
Med hjälp av en kombination av bioinformatik, molekylär modellering, biokemiska bindningsanalyser och levande cellavbildning, visar Matsubayashi och hans kollegor att en oordnad region inom p85βs inter-SH2-domän binder direkt till det endocytiska proteinet AP2. Denna del av PI3K kan aktivera en cellulär process som drar in vissa molekyler i cellen, och den gör det utan att behöva enzymets typiska lipidmodifierande funktion.
När forskarna störde bindningen fungerade inte den muterade p85β som den skulle. Istället för att reglera cellens rörelse genom sin bromsmekanism byggdes den upp på specifika platser i cellen. Detta leder till att cellerna rör sig snabbare och mer ihållande, vilket tyder på att bromsmekanismens kontroll över cellmigrering förloras.
"Anmärkningsvärt nog har detta enda PI3K-enzym motsatta gas- och bromspedaler inbyggda i dess molekylära ramverk", tillägger Matsubayashi. "Den endocytiska mekanismen hjälper till att reglera PI3K:s aktivitet för att säkerställa att cellrörelser kontrolleras vid rätt tidpunkter och på rätt platser för viktiga biologiska processer."
Denna bromsningsroll visade sig vara specifik för bara p85β-subenheten. Och eftersom p85β-subenheten av PI3K är kopplad till cancerfrämjande egenskaper, kan en djupare förståelse av PI3K-reglering och dess isoformspecificitet leda till nya terapeutiska strategier, såsom sådana som selektivt hämmar canceraspekten av PI3K samtidigt som de normala funktionerna hos PI3K bevaras. i friska celler.
Mer information: Hideaki T. Matsubayashi et al, Non-catalytic role of phosphoinositide 3-kinase in mesenkymal cell migration through non-canonical induction of p85β/AP2-medied endocytosis, Nature Communications (2024). DOI:10.1038/s41467-024-46855-y
Journalinformation: Nature Communications
Tillhandahålls av Tohoku University