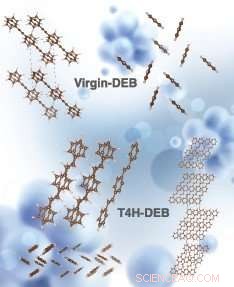
Simulerade kristallstrukturer av virgin-DEB och T4H-DEB (kemiskt känd som 1, 4-distyrylbensen, en trans-isomer av DEB-mellanprodukt efter infångning av första 4 atomära väte med 2 CH-bindningar på motsatta sidor av kolkedjan). De övre vänstra och övre högra strukturerna motsvarar sidovy och ovanifrån av jungfrulig DEB, respektive. Mitten till höger, strukturer längst ner till höger och nedre till vänster motsvarar sidovy, ovanifrån och en enhetscell (sidovy) av T4H-DEB, respektive. Kredit:Simuleringen utfördes av Hom Sharma. Konstnärlig återgivning av bilden gjordes av Alexandria Holmberg Diaz, Lawrence Livermore National Laboratory.
Överskott av väte kan orsaka problem i en mängd olika industrier. Det kan korrodera halvledare, elektronik, och kärnbränsle sitter i lagring. Det utgör också en explosionsrisk. För att ta bort detta extra väte, kemister kan använda en organisk förening som kallas en vätegetter som kemiskt binder till flera väteatomer.
Men ibland, under denna bindningsprocess – kallad katalytisk hydrering – blir de delvis hydrerade produkterna flyktiga, smälter och förångas bort innan de kan binda till fler väteatomer. Nu, forskare har undersökt hur och varför denna flyktighet varierar under hydrogenering, vilket tyder på att en tidigare underskattad effekt från kol-vätebindningar i molekylen är den främsta boven.
Den nya analysen, publicerad i The Journal of Chemical Physics , kan hjälpa kemister att identifiera de ideala förhållandena som behövs för katalytisk hydrogenering så att de bättre kan ta bort överskott av väte.
"Detta skapar en modell för beteendet hos andra organiska getters, tillåter oss att förutsäga deras optimala driftstemperaturer och miljöer, "sa Long Dinh, en fysiker vid Lawrence Livermore National Laboratory.
Dinh och hans kollegor fokuserade på en getter som heter 1, 4 bis(fenyletynyl)bensen, eller DEB. För att ta bort väte, kristallflingor av DEB blandas med katalysatorer i form av fasta pellets. Pelletarna är gjorda av aktivt kol - vars porösa struktur ger riklig yta - belagd med palladiumnanopartiklar. Palladiumkatalysatorn delar vätemolekyler till väteatomer, som sedan kan binda till DEB och bilda kol-vätebindningar.
DEB är en getter med hög kapacitet, kan binda med upp till åtta väteatomer. De flesta forskare trodde att när getters som DEB binder med fler väteatomer och förstoras, de blir mer flyktiga. Vid höga driftstemperaturer, de kan sedan förångas, driver långt från de katalytiska pellets där det inte finns några väteatomer att binda med. "Du stoppar hydrogeneringsprocessen i förtid, " sa Dinh.
Men forskarna fann att i de två första stegen av hydrering, när DEB bildar två kol-vätebindningar per steg (kol-vätebindningarna skapas på motsatta sidor av molekylens kolkedja), molekylen minskar faktiskt i flyktighet. Endast i efterföljande hydrogeneringssteg blir DEB mer flyktig.
För att studera hur och varför DEB förändras i volatilitet, forskarna mätte egenskaper som ångtryck och smältpunkter, sonderad molekylstruktur, och körde kvantmekaniska datorsimuleringar för att modellera hydreringsprocessen. Deras analys tyder på att kol-vätebindningarna i DEB spelar en nyckelroll i molekylens flyktiga beteende.
Under hydrering, väte binder till kolatomer i DEB. Enligt konventionell tanke, den resulterande kol-vätebindningen är opolär-ingen av ändarna på skivstångsstrukturen är mer negativt eller positivt laddad än den andra. Men det visar sig att koländen är något mer negativ, och kol-vätebindningen bildar en svag dipol, Dinh förklarade.
Som en dipol, en kol-vätebindning kan attrahera eller stöta bort andra kol-vätebindningar i andra DEB-molekyler. Beroende på hur kol-vätebindningarna är ordnade och hur många det finns i de mellanliggande DEB-produkterna, molekylerna kan antingen attrahera eller stöta bort varandra, och därmed vara mindre eller mer flyktig, respektive. Tidigare forskning hade förbisett dessa kollektiva interaktioner mellan kol-vätebindningar i organiska kristaller, Sade Dinh.
Från deras analys, forskarna fastställde att de optimala förhållandena för DEB-hydrering är under cirka 175 grader Fahrenheit, om det görs i ett bra vakuum. "Våra resultat, Dinh sa, "kan appliceras analogt med andra katalytiska organiska vätegettersystem också."