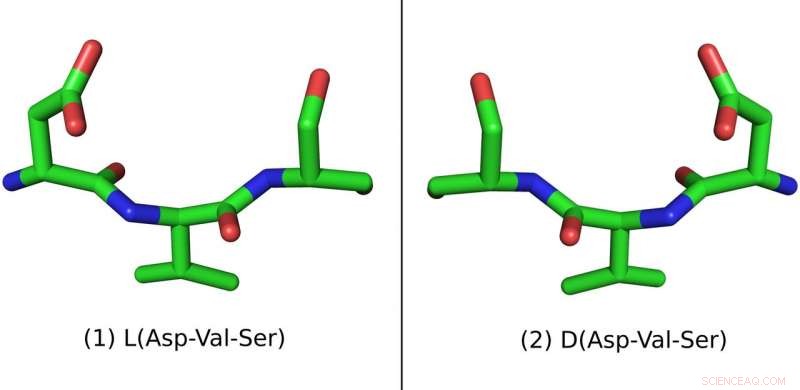
Denna peptid består av tre aminosyror:asparaginsyra (Asp), Valin (Val) och Serine (Ser). Den naturliga L-formen är till vänster och den syntetiska D-formen är till höger Credit:Pablo Gainza
Forskare vid University of Toronto har utvecklat en ny teknik för att skapa mer hållbara sjukdomsbekämpande molekyler som kan leda till läkemedel med längre varaktiga effekter.
Spegelbildsversion av befintliga läkemedel skulle hålla längre i kroppen tack vare deras förmåga att undvika nedbrytning av enzymer i magen och blodomloppet. För patienter, detta skulle innebära mindre frekventa läkemedelsinjektioner och fler läkemedel skulle potentiellt kunna göras tillgängliga som piller.
Att designa dessa droger har varit knepigt, dock.
Nu är ett team av forskare ledda av Philip Kim, en professor i datavetenskap och molekylär genetik vid University of Torontos Donnelly Center for Cellular and Biomolecular Research, har utvecklat en ny teknik för att göra spegelbildspeptider, som binder och aktiverar receptorer på cellytan. De skapade spegelbildsversioner av storsäljande läkemedel glykogenliknande peptid 1 (GLP1) och bisköldkörtelhormon (PTH). GLP1 används ofta för att behandla diabetes, och PTH är en behandling för hypoparatyreos, ett tillstånd där kroppen producerar för lite PTH och påverkar muskelfunktionen, och osteoporos. Båda spegelbildade motsvarigheterna hade längre effekter på celler än de befintliga läkemedlen.
Resultaten beskrivs i den tidiga onlineupplagan av den 29 januari Förfaranden från National Academy of Sciences .
"Spegelbildspeptider känns inte igen och bryts ned av enzymer i magen eller blodomloppet och har därför en långvarig effekt, " säger Kim. Den andra fördelen, han sa, är att spegelbildspeptider också förbises av immunsystemet, som ofta misstar naturliga peptider för främmande inkräktare och därmed begränsar läkemedlets effektivitet.
Peptider är gjorda av molekyler som kallas aminosyror. Av skäl som inte är helt förstådda och som går tillbaka till livets ursprung, nästan alla aminosyror i den naturliga världen förekommer i en geometrisk form. Deras atomer är ordnade på ett sådant sätt att hela aminosyramolekylen verkar vänsterhänt, eller "L" för kort. Som ett resultat, naturliga peptider är också vänsterhänta. Eftersom peptider som produceras av mikrober, växter och djur kan vara skadliga, människokroppen har utvecklat effektiva sätt att rensa dem.
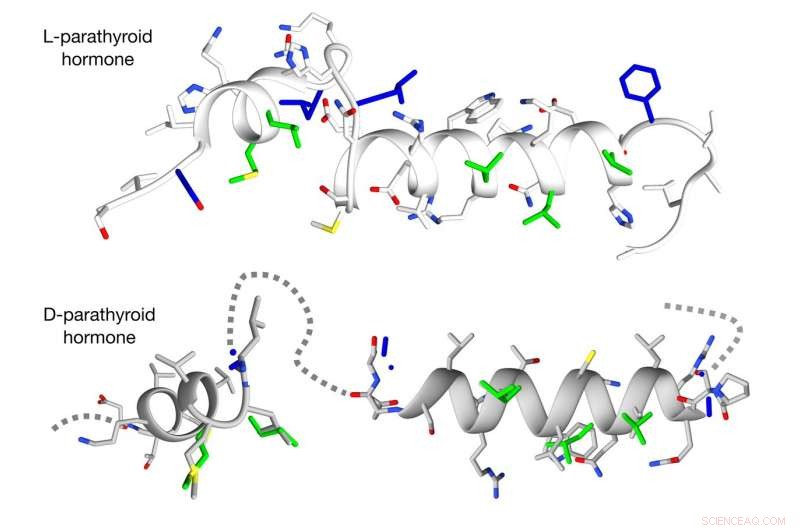
Den nya metoden övervinner hinder för att designa D-versioner av komplexa spiralformade peptider. Kredit:Michael Garton, University of Toronto
Men om du inverterar en peptids geometriska orientering, genom att göra en spegelbild av det, det kan fortfarande binda korrekta receptorer samtidigt som det glider obemärkt förbi kroppens försvarsmekanismer. Spegelbildspeptider kan tillverkas i labbet av syntetiska högerhänta aminosyror, som också är kända som "D" för dextrorotary.
Till skillnad från raka L-peptider, som ganska enkelt kan konverteras till en D-form, de flesta biologiskt aktiva peptider vrids till spiraler, och hittills har det inte funnits något bra sätt att designa sina spegelvända motsvarigheter i stor skala, sa Kim.
Med en rent beräkningsmetod, Kims team kunde klara detta hinder. De började med den största offentliga databasen som innehåller strukturell information för tre miljoner spiralformade peptider. De skapade sedan en algoritm för att vända dessa peptider till sina D-motsvarigheter. Till sist, teamet letade i detta nya virtuella bibliotek av spegelbildspeptider efter de som bäst matchade GLP1 och PTH.
När de väl hittat matchen, forskarna lät syntetisera D-peptiderna och testa deras förmåga att aktivera sina receptorer på cellens yta. De fann att både D-GLP1 och D-PTH framkallade cellulära svar som liknar deras naturliga motsvarigheter men hade en längre varaktig effekt.
"Vi undersöker nu om D-PTH skulle kunna levereras oralt eftersom det undviker nedbrytning i magen", säger Kim. "För ofta doserad medicin, detta är av stort intresse, eftersom det är mycket lättare att ta ett piller än att få en injektion. Detta kan leda till att många fler peptidläkemedel tas som piller”.
För närvarande, patienter som tar GLP1, som upptäcktes vid U of T av professor Daniel Drucker, vid institutionen för medicin, eller PTH, måste injicera dessa läkemedel dagligen.
Kim arbetar med U of Ts patentbyrå för att skydda sin teknologi när han utforskar möjligheter att samarbeta med läkemedelsindustrin för att kommersialisera forskningen. Han utvecklar också spegelbildsversioner av peptider som fungerar mot Dengue- och Zika-virusen för att göra dem mer hållbara i blodomloppet.
"Vi testar vårt tillvägagångssätt på så många intressanta peptider vi kan, " sa Kim.