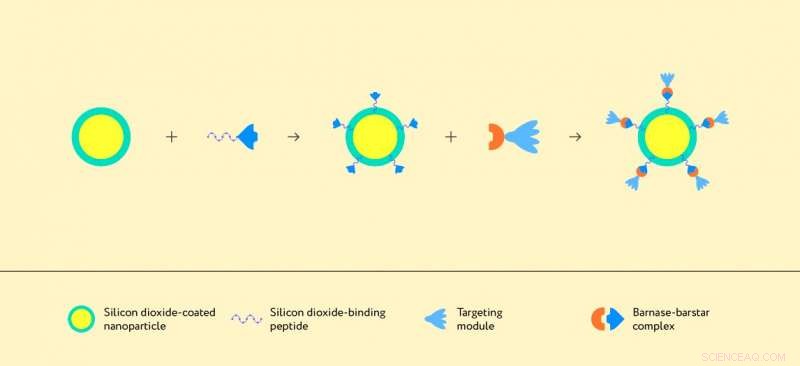
Illustration av sammansättningen av strukturen baserad på en nanopartikel och proteinkomplexet barnas-barstar. Upphovsman:Tidningsförfattare och Lion_on_helium, MIPT
Biofysiker har utvecklat en metod för att ändra ytan på mikro- och nanopartiklar- små strukturer som mäter mellan en tusendel och en miljonedel av en millimeter- genom att täcka dem med biologiska molekyler. Konstruerad på detta sätt, partiklarna kan fungera som både terapeutiska och diagnostiska medel, leverera läkemedel till cancerceller.
Tidningen publicerades i tidningen ACS -tillämpade material och gränssnitt . Dess författare är forskare från Moscow Institute of Physics and Technology (MIPT), institutet för bioorganisk kemi vid Ryska vetenskapsakademien (IBCh RAS), National Research Nuclear University MEPhI, Sechenov universitet, och Macquarie University (Australien).
Omkring 1900, Paul Ehrlich, vinnaren av Nobelpriset i fysiologi eller medicin 1908, tänkt läkemedel som skulle ha en komponent som känner igen patogener i kroppen och en annan komponent som verkar på målet. Vanligtvis, sådana läkemedel riktar sig mot receptorer på ytan av de skadade cellerna. Dessa receptorer tillåter också medlet att känna igen cellen. Ett sådant universellt system kan användas för diagnostik, terapi, eller båda. När terapi och diagnostik kombineras, detta är känt som teranostik.
För att skapa ett system som innehåller en terapeutisk och en diagnostisk komponent, ett "molekylärt lim" behövs för att hålla ihop de två delarna. Detta lim kan realiseras som proteiner som kan bilda ett stabilt komplex genom att binda till varandra. Ett av de mest stabila komplexen av detta slag är proteinet barnas-barstar. Det finns ett värde som kallas bindningskonstanten som kännetecknar hur starkt molekylerna i ett komplex är kopplade. Bindningskonstanten för barnas-barstar-komplexet är 1, 000 till 1 miljon gånger större än för antigen-antikroppskomplexen, som är grunden för vårt immunsvar.
Barnase och barstar kan användas för att konstruera olika funktionella moduler för teranostik. Till exempel, barnas kan bindas till terapeutiska medel - antikroppar, läkemedel, fluorescerande molekyler, etc. - medan barstar kan smälta ihop med ett inriktningsagent. Detta koncept föreslogs av Sergey Deyev, chef för Molecular Immunology Laboratory för IBCh RAS. De två modulerna kombineras sedan, bildar en bifunktionell förening, som har terapeutiska och diagnostiska egenskaper, och möjliggör riktad läkemedelsleverans. Genom att smälta barnase och barstar med olika terapeutiska och diagnostiska molekyler, forskare kan utveckla en rad olika teranostiska medel baserade på samma princip. Dessa molekylära strukturer kan bäras på ytan av nano- eller mikropartiklar. Partiklarna själva kan ha hjälpegenskaper, inklusive fluorescens eller förmågan att förstöras när den utsätts för strålning, dödar de omgivande skadliga cellerna, som cancerceller. Dussintals molekylstrukturer av olika typer kan deponeras på en liten partikel, potentiellt öka dess terapeutiska effekter.

Illustration av den teranostiska strukturens arbetsprincip. Upphovsman:Tidningsförfattare och Lion_on_helium, MIPT
Molekylär monteringssats
Tanken att använda nano- och mikropartiklar för att leverera läkemedel forskas aktivt i många laboratorier. De ryska och australiensiska forskarna utvecklade ett nanopartikelbaserat teranostiskt medel som använde barnas-barstar proteinkomplex och studerade dess egenskaper.
"De flesta av de metoder som för närvarande används för att kemiskt koppla biomolekyler till nanopartiklar har allvarliga brister, "säger huvudförfattaren Victoria Shipunova, en forskare vid MIPT:s Nanobiotechnology Lab och en senior forskare vid Molecular Immunology Lab vid Institute of Bioorganic Chemistry. "Biomolekylernas rumsliga orientering är dåligt kontrollerad, och de stöter på problem när de binder sig till sina mål. Densiteten hos de kopplade molekylerna är ganska låg, och proceduren är tidskrävande. "
"Vi utvecklade en metod baserad på barnas-barstar-proteinparet som inte förändrar den molekylära molekylens rumsliga struktur. Två ytterligare fördelar är dess höga specificitet och snabba koppling:Det tar bara flera minuter för alla moduler att binda, "förklarar hon.
Forskarna använde kiseldioxidbelagda partiklar som bärare för deras molekylära komplex. De primära målen för biostrukturerna som beskrivs i tidningen är cancerceller, identifierbar av HER2/neu -onmarkören på deras yta, visas som en röd utväxt i figur 2. HER2/neu är ett protein som ansvarar för celltillväxt och delning och finns i friska celler. I cancerceller, dock, detta protein är i överskott - eller överuttryckt - vilket gör att de kan växa och dela sig okontrollerbart.
Forskarna använde en molekyl från klassen av designade ankyrin -repetitionsproteiner, eller DARPins, som målmedlet som känner igen HER2/neu -proteinet. Visas som ljusblå klockblommformade strukturer i figur 1 och 2, DARPins är små och mycket stabila proteiner som kan selektivt binda till målmolekylen. Förutom en DARPin -molekyl, som känner igen cancerceller, strukturen måste införliva en molekyl som kan binda till bärarpartikelns yta - det vill säga till kiseldioxid. För detta, forskarna använde en kiseldioxidbindande peptid erhållen genom rationell design vid Macquarie University. Som ett resultat, de skapade följande struktur:En nano- eller mikropartikel är belagd med kiseldioxid, till vilken barnas-DARPin-modulen är ansluten via den kiseldioxidbindande peptiden smält med barstar (figur 1). Viktigt, var och en av de inblandade elementen kan ändras eller till och med ersättas, modifiera egenskaperna hos den övergripande strukturen. På ett sätt, det liknar ett molekylärt kit av byggstenar, som kan monteras på många sätt, producerar olika terapeutiska medel.
I själva verket, forskarna har skapat en universell monteringsmetod, vilket gör det möjligt att enkelt kombinera ett antal molekyler med terapeutisk och diagnostisk potential, samtidigt som deras rumsliga struktur och egenskaper bevaras.